摘要:善于不断的总结和归纳.是自主学习的重要方法之一.请你参与下面一系列关于化学反应的讨论. 问题1:从不同的角度.化学反应可以有不同的分类方法.四种基本反应类型是从反应的形式上进行的分类.氧化还原反应和离子反应则是从反应的本质和参加反应的微粒的角度和层面进行的分类.请在右图的方框内.用Venn图表示离子反应.分解反应和氧化还原反应之间的关系. 问题2:化学化应的速率和限度是化工生产中考虑的两个主要的因素.请你按照表中的要求完成下表. 序号 实际生产中采取的措施 工业生产实例 (1) 使用热交换器 (2) 生产中采取循环操作提高原料利用率 问题3:化学反应的发生是有条件的.反应物相同.反应条件不同.反应的原理不同.如: 点燃 4Na+O2=2Na2O,2Na+O2=Na2O2.请用离子方程式表示下列事实: 反应物相同.试剂添加的顺序不同.反应的原理不同. . .
网址:http://m.1010jiajiao.com/timu_id_1720603[举报]
(共5分)麻醉剂的发现和使用,是人类医疗史上了不起的一项成就,它可使患者在接受治疗时感觉不到疼痛。
⑴笑气(N2O)是应用于医疗的麻醉剂之一,它可由NH4NO3在微热下产生,此反应如下,请先配平反应式并标出电子转移方向和数目:
NH4NO3 = N2O + H2O
⑵另一种常用麻醉剂氯仿,常因保存不慎而被氧化,产生剧毒光气(COCl2):
2CHCl3 + O2 = 2HCl + 2COCl2,为了防止事故,使用前可用于检验氯仿是否变质的试剂是 。
A.带火星的木条 B.NaOH溶液
C.酚酞溶液 D.HNO3酸化的AgNO3溶液
查看习题详情和答案>>化学是一门以实验为基础的科学,化学实验是化学学习的重要内容.
(1)根据你掌握的知识,下列描述正确的是
①将沸水滴加到0.2mol?L-1 FeCl3溶液中,然后继续加热并不断搅拌可制得氢氧化铁胶体;②将95g蒸馏水倒入盛有5g氯化钠的烧杯中,搅拌溶解,配制5%的食盐水;
③配制溶液时俯视定容,所得溶液的浓度偏小;
④使用容量瓶、滴定管、分液漏斗时,首先应检验仪器是否漏水;
⑤向某溶液中加入Ba(NO3)2溶液有白色沉淀产生,加盐酸沉淀不消失,则原溶液中一定含有SO42-.
(2)实验室中配制480mL0.4mol?L-1 NaOH溶液,应称取NaOH的质量是
查看习题详情和答案>>
(1)根据你掌握的知识,下列描述正确的是
②④
②④
(填序号)①将沸水滴加到0.2mol?L-1 FeCl3溶液中,然后继续加热并不断搅拌可制得氢氧化铁胶体;②将95g蒸馏水倒入盛有5g氯化钠的烧杯中,搅拌溶解,配制5%的食盐水;
③配制溶液时俯视定容,所得溶液的浓度偏小;
④使用容量瓶、滴定管、分液漏斗时,首先应检验仪器是否漏水;
⑤向某溶液中加入Ba(NO3)2溶液有白色沉淀产生,加盐酸沉淀不消失,则原溶液中一定含有SO42-.
(2)实验室中配制480mL0.4mol?L-1 NaOH溶液,应称取NaOH的质量是
8.0
8.0
g;所用玻璃仪器有量筒、玻璃棒、胶头滴管外,还缺少的仪器是500mL容量瓶、烧杯
500mL容量瓶、烧杯
;NaOH固体加适量蒸馏水溶解冷却后,将溶液转移到容量瓶中,然后继续加蒸馏水定容,这样所配得溶液的浓度会偏低
偏低
(填“偏高、偏低或无影响”).(2010?丰台区二模)有机物A是重要的合成原料,在医药、染料、香料等行业有着广泛的应用.由A可以制得麻黄碱和其他很多物质.现有如下转化关系图(略去了由A→G,G→麻黄碱的反应条件和部分反应物):

请回答下列问题:
(1)关于麻黄碱下列说法正确的是
a.麻黄碱的分子式为C10H15NO
b.具有止咳平喘作用,是从中药麻黄中提取的生物碱
c.属于国际奥委会严格禁止的兴奋剂
d.麻黄碱属于芳香烃
(2)有机物A的相对分子质量为106,A中含碳、氢、氧三种元素的质量分数之比为42:3:8,则A的含氧官能团名称是
(3)反应①~⑤中属于取代反应的是
(4)写出D→B的化学方程式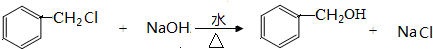
 .
.
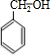
(5)F可作多种香精的定香剂,请写出B和C反应生成F的化学方程式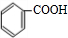 +
+
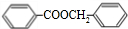 +H2O
+H2O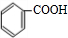 +
+
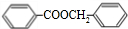 +H2O.
+H2O.
(6)写出符合下列条件的同分异构体的结构简式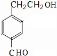
 .
.
①与中间产物G 互为同分异构体
②既能发生消去反应,又能发生酯化反应
③苯环上的一氯取代物只有两种,分子结构中没有甲基
(7)已知:
A可以由E制取,制取工艺中得到的是A、E混合物,分离该混合物的合理方法是
查看习题详情和答案>>

请回答下列问题:
(1)关于麻黄碱下列说法正确的是
abc
abc
(填字母).a.麻黄碱的分子式为C10H15NO
b.具有止咳平喘作用,是从中药麻黄中提取的生物碱
c.属于国际奥委会严格禁止的兴奋剂
d.麻黄碱属于芳香烃
(2)有机物A的相对分子质量为106,A中含碳、氢、氧三种元素的质量分数之比为42:3:8,则A的含氧官能团名称是
醛基
醛基
;检验该官能团的方法是在新制的银氨溶液中滴加A的溶液,振荡后将试管放在热水浴中温热,产生银镜
在新制的银氨溶液中滴加A的溶液,振荡后将试管放在热水浴中温热,产生银镜
.(3)反应①~⑤中属于取代反应的是
①②⑤
①②⑤
(填序号).(4)写出D→B的化学方程式


(5)F可作多种香精的定香剂,请写出B和C反应生成F的化学方程式
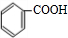 +
+
| 浓硫酸 |
| △ |
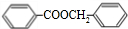 +H2O
+H2O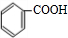 +
+
| 浓硫酸 |
| △ |
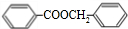 +H2O
+H2O(6)写出符合下列条件的同分异构体的结构简式


①与中间产物G 互为同分异构体
②既能发生消去反应,又能发生酯化反应
③苯环上的一氯取代物只有两种,分子结构中没有甲基
(7)已知:
| 溶解性 | 沸点 | |
| A | 微溶于水 | 179.0℃ |
| E | 不溶于水 | 110.8℃ |
蒸馏
蒸馏
.(8分)工业甲醇的质量分数可以用下列方法测定:
①在稀H2SO4中甲醇被Cr2O72—氧化成CO2和H2O,
反应式为:CH3OH+Cr2O72—+8H+=CO2↑+2Cr3++6H2O;
②过量的Cr2O72—可用Fe2+与之完全反应:
___Cr2O72—+___Fe2++____H+ —_____Cr3++____Fe3++____H2O
现有0.12 g工业甲醇,在H2SO4溶液中与25 mL 0.2 mol·L-1K2Cr2O7溶液反应,多余的K2Cr2O7再用1 mol·L—1FeSO4与其反应,结果用去FeSO4溶液9.6 mL。
(1)配平第②步的离子方程式___________________________
(2)计算工业甲醇的质量分数。