摘要:23.已知NO2和N2O4可以相互转化:2NO2(g)N2O4(g),△H<0.现将一定量NO2和N2O4的混合气体通入一体积为1 L的恒温密闭容器中.反应物浓度随时间变化关系如下图所示. 根据上图.回答下列问题: (1)图中共有两条曲线X和Y.其中曲线 表示N2O4浓度随时间的变化,a.b.c.d四个点中.表示化学反应处于平衡状态的点是 . (2)25 min~30 min内用NO2表示的平均化学反应速率v(NO2)= mol/,反应进行至25 min时.曲线发生变化的原因是 . (3)若要达到与最后相同的化学平衡状态.在25 min时还可以采取的措施是 . A.升高温度 B.缩小容器体积 C.加入催化剂 D.加入一定量的N2O4
网址:http://m.1010jiajiao.com/timu_id_1719386[举报]
已知NO2和N2O4可以相互转化: N2O4 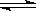 2NO2,某温度时,把1mol N2O4气体通入体积为10L的真空密闭容器中,立即出现棕色,反应进行4s时NO2的浓度为0.04mol/L,再经过一定时间后,反应到达平衡,这时容器内压强为开始时的1.8倍。
2NO2,某温度时,把1mol N2O4气体通入体积为10L的真空密闭容器中,立即出现棕色,反应进行4s时NO2的浓度为0.04mol/L,再经过一定时间后,反应到达平衡,这时容器内压强为开始时的1.8倍。
(1)前4s中以N2O4的浓度变化表示的平均反应速度为 mol/L·s
(2)在4s时容器内的压强为开始时的 倍
(3)在平衡时容器内含N2O4 mol
(4)在平衡时容器内NO2的浓度为 mol/L
(5)平衡时N2O4的转化率为
已知NO2和N2O4可以相互转化: N2O4 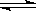 2NO2,某温度时,把1mol
N2O4气体通入体积为10L的真空密闭容器中,立即出现棕色,反应进行4s时NO2的浓度为0.04mol/L,再经过一定时间后,反应到达平衡,这时容器内压强为开始时的1.8倍。
2NO2,某温度时,把1mol
N2O4气体通入体积为10L的真空密闭容器中,立即出现棕色,反应进行4s时NO2的浓度为0.04mol/L,再经过一定时间后,反应到达平衡,这时容器内压强为开始时的1.8倍。
(1)前4s中以N2O4的浓度变化表示的平均反应速度为 mol/L·s
(2)在4s时容器内的压强为开始时的 倍
(3)在平衡时容器内含N2O4 mol
(4)在平衡时容器内NO2的浓度为 mol/L
(5)平衡时N2O4的转化率为
查看习题详情和答案>>
 已知NO2和N2O4可以相互转化:2NO2(g)?N2O4(g)△H<0.在恒温条件下将一定量NO2和N2O4的混合气体通入一容积为2L的密闭容器中,反应物浓度随时间变化关系如图所示.下列说法正确的是( )
已知NO2和N2O4可以相互转化:2NO2(g)?N2O4(g)△H<0.在恒温条件下将一定量NO2和N2O4的混合气体通入一容积为2L的密闭容器中,反应物浓度随时间变化关系如图所示.下列说法正确的是( )
查看习题详情和答案>>
 已知NO2和N2O4可以相互转化:2NO2(g)?N2O4(g)△H<0.在恒温条件下将一定量NO2和N2O4的混合气体通入一容积为2L的密闭容器中,反应物的浓度随时间变化关系如图.下列说法正确的是( )
已知NO2和N2O4可以相互转化:2NO2(g)?N2O4(g)△H<0.在恒温条件下将一定量NO2和N2O4的混合气体通入一容积为2L的密闭容器中,反应物的浓度随时间变化关系如图.下列说法正确的是( )| A、a、b、c、d四个点中,只有b、d点的化学反应处于平衡状态 | B、前10min内用v(NO2)表示的化学反应速率为0.06mol(L?min) | C、25min时,导致平衡移动的原因是将密闭容器的体积缩小为1L | D、图中的两条曲线,X是表示N2O4浓度随时间变化的曲线 |
 N2O4(g);Q>0现将一定量NO2和N2O4的混合气体通入体积为1L的恒温密闭容器中,反应物浓度随时间变化关系如图.下列说法正确的是( )
N2O4(g);Q>0现将一定量NO2和N2O4的混合气体通入体积为1L的恒温密闭容器中,反应物浓度随时间变化关系如图.下列说法正确的是( )