摘要:22.该伴孢晶体蛋白中含有的肽键数是 A 123 B 124 C 125 D 126
网址:http://m.1010jiajiao.com/timu_id_1718399[举报]
已知A、B、C、D四种分子所含原子的数目依次为1、3、6、2,且都含有18个电子,B、C是由两种元素的原子组成,且分子中两种原子的个数比均为1:2。D元素的氢化物能刻蚀玻璃。
(1)A的分子式是 ,写出A原子的价层电子排布式 。
(2)B分子的中心原子的杂化类型是 ,分子空间构型是 ,
该分子属于 分子(填“极性”或“非极性”)。
(3)C的化学式是 ,分子中含有的化学键类型是 。
A. D元素氢化物的沸点比HCl的沸点高,其主要原因是 。
查看习题详情和答案>>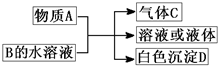 (2011?崇文区模拟)A、B、C、D均为中学化学常见物质,它们之间的反应关系如图所示.
(2011?崇文区模拟)A、B、C、D均为中学化学常见物质,它们之间的反应关系如图所示.(1)若A是碳化钙,A与B的水溶液反应时只生成气体C、CaCO3和H2O.则B(只含两种元素)的化学式为
CO2
CO2
,其固态时的晶体为分子
分子
晶体;C分子中含有的化学键类型是极性键和非极性键
极性键和非极性键
.(2)若A是短周期中原子半径最大的元素的单质,D既可溶于NaOH溶液又可溶于盐酸.请写出:
①D溶于盐酸的离子方程式
Al(OH)3+3H+=Al3++3H2O
Al(OH)3+3H+=Al3++3H2O
.②工业上冶炼A的化学方程式
2NaCl
2Na+Cl2↑
| ||
2NaCl
2Na+Cl2↑
.
| ||
③实验室用惰性电极电解100mL 0.1mol/L A的氯化物的水溶液(滴有酚酞),一段时间后,若阴阳两极均得到112mL气体(标准状况),则所得溶液的pH为
13
13
(忽略反应前后溶液的体积变化).某电极附近溶液颜色变红,原因是氢离子在阴极得到电子生成氢气,水的电离平衡被破坏,使得阴极附近氢氧根离子浓度大于氢离子浓度
氢离子在阴极得到电子生成氢气,水的电离平衡被破坏,使得阴极附近氢氧根离子浓度大于氢离子浓度
,则该电极与外接直流电源的负
负
极相连接(填“正”、或“负”).(3)若A是可溶性强碱,B是正盐,D不溶于稀硝酸,则反应的化学方程式是
Ba(OH)2+(NH4)2SO4=BaSO4↓+2NH3↑+2H2O
Ba(OH)2+(NH4)2SO4=BaSO4↓+2NH3↑+2H2O
.(4)若A常温下为红棕色气体,B是含氧酸盐,D不溶于盐酸,则D的化学式是
H2SiO3
H2SiO3
. 元素周期表中第四周期的金属元素在生产和科研中有非常重要的使用价值.
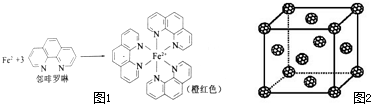
元素周期表中第四周期的金属元素在生产和科研中有非常重要的使用价值.(1)测定土壤中铁的含量时需先将三价铁还原为二价铁,再采用邻啡罗啉作显色剂,用比色法测定,若土壤中含有高氯酸盐时会对测定有干扰.相关的反应如下:
4FeCl3+2NH2OH?HCl→4FeCl2+N2O↑+6HCl+H2O
①Fe2+在基态时,核外电子排布式
②羟胺中(NH2OH)采用SP3杂化的原子有
③Fe2+与邻啡罗啉形成的配合物中,配位数为
(2)向硫酸铜溶液中加入过量氨水,然后加入适量乙醇,溶液中析出深蓝色的[Cu(NH3)4]SO4晶体,该晶体中含有的化学键类型是
(3)往硫酸铜溶液中加入过量氨水,可生成[Cu(NH3)4]2+,已知NF3与NH3的空间构型都是三角锥形,但NF3 不易与Cu2+形成配离子,其原因是
(4)配合物Ni(CO)4常温下呈液态,易溶于CCl4、苯等有机溶剂.固态Ni(CO)4属于
(5)如果把晶胞顶点与最近三个面心所围成的空隙叫做四面体空隙,第四周 期电负性最小的原子可作为容体掺入C60 晶体的空隙中,形成具有良好的超导性的掺杂C60 化合物.现把C60抽象成质点,该晶体的晶胞结构如图2所示,若每个四面体空隙填入一个原子,则全部填满C60 晶体的四面体空隙后,所形成的掺杂C60 化合物的化学式为
【化学-物质结构与性质】
钛和钛的合金已被广泛用于制造电讯器材、人造骨骼、化工设备、飞机等航天航空材料,被誉为“未来世界的金属”.试回答下列问题:
(1)钛有2248和2250Ti两种原子,它们互称为
 (2)偏钛酸钡在小型变压器、话筒和扩音器中都有应用.偏钛酸钡晶体中晶胞的结构如右图所示,它的化学式是
(2)偏钛酸钡在小型变压器、话筒和扩音器中都有应用.偏钛酸钡晶体中晶胞的结构如右图所示,它的化学式是
(3)现有含Ti3+的配合物,化学式为[TiCl(H2O)5]Cl2?H2O.配离子[TiCl(H2O)5]2+中含有的化学键类型是
查看习题详情和答案>>
钛和钛的合金已被广泛用于制造电讯器材、人造骨骼、化工设备、飞机等航天航空材料,被誉为“未来世界的金属”.试回答下列问题:
(1)钛有2248和2250Ti两种原子,它们互称为
同位素
同位素
.Ti元素在元素周期表中的位置是第四
四
周期,第IVB
IVB
族;基态原子的电子排布式为Is22s22p63S23p63d24s2(或[Ar]3d24s2)
Is22s22p63S23p63d24s2(或[Ar]3d24s2)
按电子排布Ti元素的元素周期表分区中属于d
d
区元素. (2)偏钛酸钡在小型变压器、话筒和扩音器中都有应用.偏钛酸钡晶体中晶胞的结构如右图所示,它的化学式是
(2)偏钛酸钡在小型变压器、话筒和扩音器中都有应用.偏钛酸钡晶体中晶胞的结构如右图所示,它的化学式是BaTiO3
BaTiO3
.(3)现有含Ti3+的配合物,化学式为[TiCl(H2O)5]Cl2?H2O.配离子[TiCl(H2O)5]2+中含有的化学键类型是
极性共价键(或共价键)、配位键
极性共价键(或共价键)、配位键
,该配合物的配体是H2O、Cl-
H2O、Cl-
.(2011?宝鸡三模)[化学一选修3物质结构与性质]
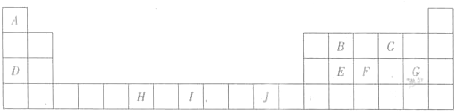
下表为长式周期表的一部分,其中的字母A--J分别代表对应的10种元素.
请回答下列问题:
(1)元素I的原子结构示意图为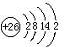
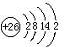 .
.
(2)B、E两元素分别与元素C按原子个数比为1:2形成化合物时,中心原子的杂化方式分别为
 (3)H3+离子在一定条件下能形成结构复杂的配离子[HG(A2C)5]2+形成该配离子时,H3+离子接受了配体提供的
(3)H3+离子在一定条件下能形成结构复杂的配离子[HG(A2C)5]2+形成该配离子时,H3+离子接受了配体提供的
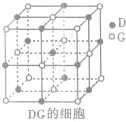
(4)元素D与元素G形成的化合物DG的晶胞结构如图所示,每个D离子周围与之最近的D离子的个数为
g/cm3
g/cm3.
查看习题详情和答案>>
下表为长式周期表的一部分,其中的字母A--J分别代表对应的10种元素.

请回答下列问题:
(1)元素I的原子结构示意图为
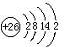
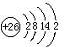
(2)B、E两元素分别与元素C按原子个数比为1:2形成化合物时,中心原子的杂化方式分别为
sp
sp
和sp3
sp3
,这两种化合物的熔沸点差别很大的原因是SiO2为原子晶体,CO2为分子晶体
SiO2为原子晶体,CO2为分子晶体
. (3)H3+离子在一定条件下能形成结构复杂的配离子[HG(A2C)5]2+形成该配离子时,H3+离子接受了配体提供的
(3)H3+离子在一定条件下能形成结构复杂的配离子[HG(A2C)5]2+形成该配离子时,H3+离子接受了配体提供的孤电子对
孤电子对
.该配离子中含有的化学键类型是共价键和离子键
共价键和离子键
,其中G的核外电子排布式为1s22s22p63s23p5
1s22s22p63s23p5
.(4)元素D与元素G形成的化合物DG的晶胞结构如图所示,每个D离子周围与之最近的D离子的个数为
12
12
.若设该晶胞的棱长为a cm,阿伏加德罗常数的值为NA,则该化合物的密度为| 234 |
| a3NA |
| 234 |
| a3NA |