摘要:28.有a.b.c.d.e五种水溶液.每种溶液的溶质中都含有下列阴.阳离子各一种.阳离子:Na+.NH4+.Ag+.Mg2+.Al3+, 阴离子:OH-.Cl-.SO42-.NO3-. ①加入氨水.则a.c.d均有沉淀产生,氨水过量时.c中沉淀溶解得无色溶液. ②加NaOH于上述a.d的沉淀中.a中的沉淀又溶解. ③在b中.加入NaOH并加热. 有使湿润的红色石蕊试纸变蓝的气体产生 ④用铂丝蘸e的溶液.灼烧后火焰呈黄色. ⑤加BaCl2溶液于上述五种溶液中.a.b.c都生成白色沉淀.加入硝酸沉淀不溶. ⑥d与c混合.生成白色沉淀.加入硝酸沉淀不溶. 通过实验事实推断这五种水溶液种各有哪些离子: 溶液 a b c d e 阳离子 阴离子
网址:http://m.1010jiajiao.com/timu_id_1717510[举报]
有a、b、c、d、e五种水溶液,每种溶液的溶质中都含有下列阴、阳离子各一种,阳离子:Na+、NH4+、Ag+、Mg2+、Al3+, 阴离子:OH-、Cl-、SO42-、NO3-。
①加入氨水,则a、c、d均有沉淀产生;氨水过量时,c中沉淀溶解得无色溶液。
②加NaOH于上述a、d的沉淀中,a中的沉淀又溶解。
③在b中,加入NaOH并加热, 有使湿润的红色石蕊试纸变蓝的气体产生
④用铂丝蘸e的溶液,灼烧后火焰呈黄色。
⑤加BaCl2溶液于上述五种溶液中,a、b、c都生成白色沉淀,加入硝酸沉淀不溶。
⑥d与c混合,生成白色沉淀,加入硝酸沉淀不溶。
通过实验事实推断这五种水溶液种各有哪些离子(填化学式):

有A、B、C、D、E五种元素,其中A、B、C、D为短周期元素,A元素的周期数、主族数、原子序数相同;B原子核外有3种能量不同的原子轨道且每种轨道中的电子数相同;C原子的价电子构型为csccpc+1,D元素的原子最外层电子数比次外层电子数少2个,D的阴离子与E的阳离子电子层结构相同,D和E可形成化合物E2D.
(1)上述元素中,第一电离能最小的元素的原子结构示意图为 ;D的价电子排布式图为 ;
(2)下列分子结构图中的●和○表示上述元素的原子中除去最外层电子的剩余部分,小黑点表示没有形成共价键的最外层电子,短线表示共价键.
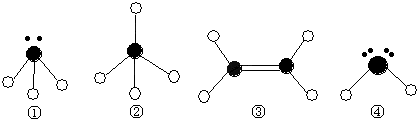
则在以上分子中,中心原子采用sp3杂化形成化学键的是 (填写分子的化学式); 在③的分子中有 个σ键和 个π键.
(3)A、C、D可形成既具有离子键又具有共价键的化合物,其化学式可能为 ;足量的C的氢化物水溶液与CuSO4 溶液反应生成的配合物,其化学式为 ,请说出该配合物中中心原子与配位体及内界与外界之间的成键情况: .
查看习题详情和答案>>
(1)上述元素中,第一电离能最小的元素的原子结构示意图为
(2)下列分子结构图中的●和○表示上述元素的原子中除去最外层电子的剩余部分,小黑点表示没有形成共价键的最外层电子,短线表示共价键.

则在以上分子中,中心原子采用sp3杂化形成化学键的是
(3)A、C、D可形成既具有离子键又具有共价键的化合物,其化学式可能为
 Ⅰ有A、B、C、D、E五种短周期元素,它们的原子序数依次增大,A元素的原子是半径最小的原子.B元素的最高价氧化物的水化物与其氢化物反应生成一种盐X,D与A同族,且与E同周期,E元素的最外层电子数是次外层电子数的
Ⅰ有A、B、C、D、E五种短周期元素,它们的原子序数依次增大,A元素的原子是半径最小的原子.B元素的最高价氧化物的水化物与其氢化物反应生成一种盐X,D与A同族,且与E同周期,E元素的最外层电子数是次外层电子数的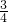 倍.A、B、D、E这四种元素,每一种都能与C元素形成原子个数比不相同的多种化合物.回答下列问题:
倍.A、B、D、E这四种元素,每一种都能与C元素形成原子个数比不相同的多种化合物.回答下列问题:
(1)写出相应元素符合,A______B______ C______ E______
(2)由A、C、D、E四种元素所组成的一种中学常见的化合物,它既能与盐酸反应,又能与NaOH溶液反应,在这种化合物的水溶液中,滴入紫色石蕊试液出现红色,则溶液中离子浓度由大到小的排列顺序为:______.
(3)将铝片和镁片.插入由A、C、D三种元素组成物质的稀溶液中构成原电池,则负极的电极反应式为______.
Ⅱ已知X是一种盐,H是常见金属单质,F、I是常见非金属单质,E、G都是工业上重要的碱性物质,它们有右图所示的关系.
试回答下列问题
(1)G的化学式为:______.
(2)写出下列反应的化学方程式
①______ ②______.
查看习题详情和答案>>
有A、B、C、D、E五种元素,其中A、B、C、D为短周期元素,A元素的周期数、主族数、原子序数相同;B原子核外有3种能量不同的原子轨道且每种轨道中的电子数相同;C原子的价电子构型为csccpc+1,D元素的原子最外层电子数比次外层电子数少2个,D的阴离子与E的阳离子电子层结构相同,D和E可形成化合物E2D。
(1)上述元素中,第一电离能最小的元素的原子结构示意图为_______;D的电子排布式为__________;
(2)下列分子结构图中的 和
和 表示上述元素的原子中除去最外层电子的剩余部分,小黑点表示没有形成共价键的最外层电子,短线表示共价键。
表示上述元素的原子中除去最外层电子的剩余部分,小黑点表示没有形成共价键的最外层电子,短线表示共价键。
(1)上述元素中,第一电离能最小的元素的原子结构示意图为_______;D的电子排布式为__________;
(2)下列分子结构图中的
 和
和 表示上述元素的原子中除去最外层电子的剩余部分,小黑点表示没有形成共价键的最外层电子,短线表示共价键。
表示上述元素的原子中除去最外层电子的剩余部分,小黑点表示没有形成共价键的最外层电子,短线表示共价键。 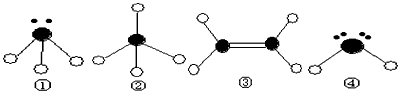
则在以上分子中,中心原子采用sp3杂化形成化学键的是__________(填写分子的化学式); 在③的分子中有__________个σ键和__________个π键。
(3)A、C、D可形成既具有离子键又具有共价键的化合物,其化学式可能为__________;C的氢化物水溶液与足量AgNO3溶液反应生成的配合物,其化学式为__________,请说出该配合物中中心原子与配位体及内界与外界之间的成键情况:__________。
查看习题详情和答案>>
(3)A、C、D可形成既具有离子键又具有共价键的化合物,其化学式可能为__________;C的氢化物水溶液与足量AgNO3溶液反应生成的配合物,其化学式为__________,请说出该配合物中中心原子与配位体及内界与外界之间的成键情况:__________。
A、B、C、D、E五种短周期元素,它们的原子序数依次增大;A元素的原子是半径最小的原子;B元素的最高价氧化物对应的水化物与其氢化物反应生成一种盐X;D与A同主族,且与E同周期;E元素的最外层电子数是其次外层电子数的
倍.A、B、D、E这四种元素,每种与C元素都能形成元素的原子个数比不相同的若干种化合物.请回答下列问题:
(1)写出B、C、D、E元素的元素符号:B
(2)A、B、C、E四种元素可形成两种酸式盐,这两种酸式盐的化学式为
(3)由A、C、D三种元素形成化合物的电子式为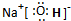
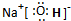 ,其中含有的化学键为
,其中含有的化学键为
(4)用电子式表示化合物A2E的形成过程
 .
.
查看习题详情和答案>>
| 3 | 4 |
(1)写出B、C、D、E元素的元素符号:B
N
N
;CO
O
;DNa
Na
;ES
S
(2)A、B、C、E四种元素可形成两种酸式盐,这两种酸式盐的化学式为
NH4HSO4
NH4HSO4
、NH4HSO3
NH4HSO3
;这两种酸式盐在溶液中相互反应的离子方程式为HSO3-+H+=SO2↑+H2O
HSO3-+H+=SO2↑+H2O
(3)由A、C、D三种元素形成化合物的电子式为
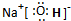
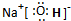
离子键、共价键
离子键、共价键
(4)用电子式表示化合物A2E的形成过程

