网址:http://m.1010jiajiao.com/timu_id_1717489[举报]
《有机化学基础》模块试题
1.有机黏合剂的黏合过程是液态的小分子黏合剂经化学反应转化为大分子或高分子而固化。
(1)“502胶”是一种快干胶,其主要成分为α氰基丙烯酸乙酯( ),请写出“502胶”发生黏合作用的化学方程式:_____________________________;反应类型是_____________。
),请写出“502胶”发生黏合作用的化学方程式:_____________________________;反应类型是_____________。
(2)厌氧胶( )也是一种黏合剂,工业上用丙烯酸和某物质在一定条件下反应可制得这种黏合剂,该物质的名称是_____________;请写出这一制取过程的化学方程式_________________。
)也是一种黏合剂,工业上用丙烯酸和某物质在一定条件下反应可制得这种黏合剂,该物质的名称是_____________;请写出这一制取过程的化学方程式_________________。
(3)白乳胶是常用的黏合剂,其主要成分为醋酸乙烯酯(CH3COOCH=CH2),它有多种同分异构体,如 、
、 、
、 。已知含有
。已知含有![]() 结构的物质不能稳定存在。请另外写出3种含—CH=CH—结构的链状同分异构体的结构简式:______________、______________、______________。
结构的物质不能稳定存在。请另外写出3种含—CH=CH—结构的链状同分异构体的结构简式:______________、______________、______________。
(4)已知醇和醛可以发生反应:2CH3OH+HCHO![]() CH3OCH2OCH3+H2O,聚乙烯醇可用做普通胶水,它的羟基可全部与丁醛(CH3CH2CH2CHO)缩合脱水,得到含六原子环的强力黏合剂聚乙烯缩丁醛。请写出制取聚乙烯缩丁醛的化学方程式:________________。
CH3OCH2OCH3+H2O,聚乙烯醇可用做普通胶水,它的羟基可全部与丁醛(CH3CH2CH2CHO)缩合脱水,得到含六原子环的强力黏合剂聚乙烯缩丁醛。请写出制取聚乙烯缩丁醛的化学方程式:________________。
《物质结构与性质》模块试题2.如下图是Na、Cu、Si、H、C、N等元素单质的熔点高低的顺序,其中c、d均是热和电的良导体。

(1)请写出上图中d单质对应元素原子基态时的电子排布式_____________。
(2)单质a、f、b对应的元素以原子个数比1∶1∶1形成的分子中含_____________个σ键,_____________个π键。
(3)a与b的元素形成的10电子中性分子X的空间构型为_____________;将X溶于水后的溶液滴入到含d元素高价离子的溶液中至过量,生成的含d元素离子的化学式为________
_______,其中X与d的高价离子之间以_____________键结合。
(4)上述六种元素中的一种元素形成的含氧酸的结构为:![]() ,该含氧酸的分子式为_____________,请简要说明该物质易溶于水的原因__________________________。
,该含氧酸的分子式为_____________,请简要说明该物质易溶于水的原因__________________________。
某化学小组探究液体有机物样品A(C3 H8O2)的结构,进行如下实验。
实验I:用右图实验装置,通过Na与A反应确定羟基个数。
试回答下列问题:
(1)有机物A从 (填仪器名称)中加入;检验装置甲的气密性的方法是 。
(2)实验前预先将小块钠在二甲苯中熔化成若干个小球并冷却后再与有机物A反应,其目的是 。
(3)实验数据记录如下:p=l.038 g·mL-1
| 实验编号 | 有机样品的体积 | 有机样品的质量 | 生成气体的体积(标准状况下) |
| I | 3.65mL | 3.8g | 1120mL |
| II | 7.30mL | 7.6g | 2240mL |
| III | 14.60mL | 15.2g | 4000mL |
①不能选第组数据来计算A中羟基个数,这组数据出现错误的原因可能是 ,(填两条)。
②有机物A中羟基个数为 。
实验Ⅱ:
欲确定有机物A中含氧官能团的位置,进行如下实验:
①取7.30 mL A,Cu作催化剂,经氧化后完全转化成液态有机物B。
②取一质量为m1g的洁净试管,向其中加入足量银氨溶液,滴人化合物B,并水浴加热,待充分反应后,静置,小心倒出上层清液,向试管中小心滴加蒸馏水,倒出,再加入蒸馏水,再倒出,最后将试管烘干并称量。重复2次,试管质量均为m2g。
试回答下列问题:
(1)步骤②中小心滴加蒸馏水的目的是 。
(2)若![]() 则有机物A的结构简式是 。
则有机物A的结构简式是 。
(3)步骤②中,不宜将银氨溶液换成新制氢氧化铜溶液的原因是 。
查看习题详情和答案>>
 2CO2+N2
2CO2+N2研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率.为了分别验证温度、催化剂比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中:
| 实验编号 | T/℃ | NO初始浓度 mol?L-1 |
CO初始浓度 mol?L-1Com] |
催化剂的比表面积 ㎡?g-1 |
| Ⅰ | 280 | 1.2×10-3 | 5.8×10-3 | 82 |
| Ⅱ | 124 | |||
| Ⅲ | 350 | 124 |
②设计实验Ⅱ、Ⅲ的目的是
(2)工业尾气中氮的氧化物常采用氨催化吸收法,原理是NH3与NOx反应生成无毒的物质.某同学采用以下装置和步骤模拟工业上氮的氧化物处理过程.提供的装置:
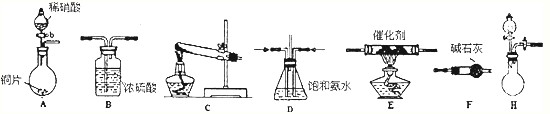
步骤一、NH3的制取
①所提供的装置中能快速、简便制取NH3的装置是:
②若采用C装置制取氨气(控制实验条件相同),情况如下表:
| 试剂组合序号 | 固体试剂(g) | NH3体积(ml) | |
| a | 12.0gCa(OH)2(过量) | 10.8gNH4Cl | 2688 |
| b | 10.8g(NH4)2SO4 | 2728 | |
| c | 12.0gNaOH(过量) | 10.8gNH4Cl | 3136 |
| d | 10.8g(NH4)2SO4 | 3118 | |
| e | 12.0gCaO(过量) | 10.8gNH4Cl | 3506 |
| f | 10.8g(NH4)2SO4 | 3584 | |
步骤二、模拟尾气的处理:
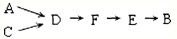
选用上述部分装置,按下列顺序连接成模拟尾气处理装置:
③A中反应的离子方程式:
④D装置作用有:使气体混合均匀、调节气流速度,还有一个作用是:
⑤D装置中的液体可换成
a.CuSO4溶液 b.H2O c.CCl4 d.浓H2SO4
⑥该同学所设计的模拟尾气处理实验还存在的明显缺陷是:
| ||
研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率.为了分别验证温度、催化剂比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中:
| 实验编号 | T/℃ | NO初始浓度 mol?L-1 |
CO初始浓度 mol?L-1 |
催化剂的比表面积 ㎡?g-1 |
| Ⅰ | 280 | 1.2×10-3 | 5.8×10-3 | 82 |
| Ⅱ | 124 | |||
| Ⅲ | 350 | 124 |
②设计实验Ⅱ、Ⅲ的目的是
(2)工业尾气中氮的氧化物常采用氨催化吸收法,原理是NH3与NOx反应生成无毒的物质.某同学采用以下装置和步骤模拟工业上氮的氧化物处理过程.提供的装置如图:
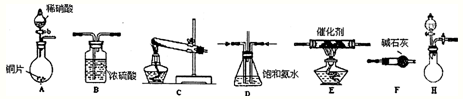
步骤一、NH3的制取
①所提供的装置中能快速、简便制取NH3的装置是:
②若采用C装置制取氨气(控制实验条件相同),情况如下表:
| 试剂组合序号 | 固体试剂(g) | NH3体积(mL) | |
| a | 12.0g Ca(OH)2(过量) | 10.8g NH4Cl | 2688 |
| b | 10.8g(NH4)2SO4 | 2728 | |
| c | 12.0g NaOH(过量) | 10.8g NH4Cl | 3136 |
| d | 10.8g(NH4)2SO4 | 3118 | |
| e | 12.0g CaO(过量) | 10.8g NH4Cl | 3506 |
| f | 10.8g(NH4)2SO4 | 3584 | |
步骤二、模拟尾气的处理选用上述部分装置,按下列顺序连接成模拟尾气处理装置:
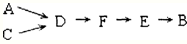
①A中反应的离子方程式:
②D装置作用有:使气体混合均匀、调节气流速度,还有一个作用是:
③D装置中的液体可换成
a.CuSO4溶液 b.H2O c.CCl4 d.浓H2SO4
④该同学所设计的模拟尾气处理实验还存在的明显缺陷是:
 转化成
转化成 ,可选用的试剂是 ( )
,可选用的试剂是 ( )