摘要:(2)MnO2+4H++2Cl-Mn2++Cl2↑+2H2O Al2O3+2OH-=2AlO2-+H2O (3)Cl2+H2O2=2HCl+O2
网址:http://m.1010jiajiao.com/timu_id_170163[举报]
在实验室中用二氧化锰跟浓盐酸反应制备干燥纯净的氯气.进行此实验,所用仪器如图: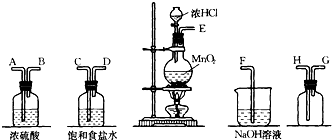
(1)连接上述仪器的正确顺序是(填各接口处的字母):E 接
(2)在装置中:①饱和食盐水起的作用是
②浓硫酸起的作用是
(3)化学实验中检验是否有Cl2产生常用湿润的淀粉-KI试纸.如果有Cl2产生,可观察到的现象是
(4)写出下列化学反应的离子方程式:
①气体发生装置中进行的反应:
②尾气吸收装置中进行的反应:
查看习题详情和答案>>

(1)连接上述仪器的正确顺序是(填各接口处的字母):E 接
C
C
,D
D
接A
A
,B
B
接H
H
,G
G
接 F.(2)在装置中:①饱和食盐水起的作用是
除去挥发出的氯化氢气体,抑制氯气在水中的溶解度
除去挥发出的氯化氢气体,抑制氯气在水中的溶解度
,②浓硫酸起的作用是
吸收水蒸气干燥氯气
吸收水蒸气干燥氯气
.(3)化学实验中检验是否有Cl2产生常用湿润的淀粉-KI试纸.如果有Cl2产生,可观察到的现象是
试纸变蓝
试纸变蓝
,写出反应方程式2KI+Cl2=2KCl+I2
2KI+Cl2=2KCl+I2
.(4)写出下列化学反应的离子方程式:
①气体发生装置中进行的反应:
MnO2+4H++2Cl-=Mn2++Cl2↑+2H2O
MnO2+4H++2Cl-=Mn2++Cl2↑+2H2O
;②尾气吸收装置中进行的反应:
Cl2+2OH-=Cl-+ClO-+H2O
Cl2+2OH-=Cl-+ClO-+H2O
.(2012?菏泽二模)大型有色金属冶炼工厂剩下的废料中,含有金、银、铂、钯等贵重金属,为提高经济效益,厂部科技小组要从废料中提取金、银、铂、钯等贵重金属,步骤设计如下图甲,试回答下列问题:

(1)实验步骤中,浓硫酸浸煮产生尾气的主要成分是
a.H2 b.NO2 c.SO2 d.灼热的氧化铜 e.NaOH溶液 f.品红试剂
(2)操作I是
(3)实验过程中所需的氯气在制备中,会混有杂质(H2O和HCl),科技小组设计了图乙所示的实验装置,证明水蒸气和HCl杂质的存在,请根据设计示意图完成下列有关问题:
写出制氯气的离子方程式:
①实验装置的接口顺序为:b接
②装置D的作用是
③在实验中,一组员认为该实验设计存有缺陷:不能证明最终通入AgNO3溶液中的气体只有一种.
为了确保实验结论的可靠性,证明最终通入AgNO3溶液的气体只有一种,他们提出在某两个装置之间再加装置E,如下图所示.你认为装置E应加在

查看习题详情和答案>>

(1)实验步骤中,浓硫酸浸煮产生尾气的主要成分是
c
c
(填写代号,下同),欲进行尾气处理,最理想的试剂是e
e
.a.H2 b.NO2 c.SO2 d.灼热的氧化铜 e.NaOH溶液 f.品红试剂
(2)操作I是
过滤
过滤
,操作中需要的玻璃仪器有漏斗、烧杯、玻璃棒
漏斗、烧杯、玻璃棒
.(3)实验过程中所需的氯气在制备中,会混有杂质(H2O和HCl),科技小组设计了图乙所示的实验装置,证明水蒸气和HCl杂质的存在,请根据设计示意图完成下列有关问题:
写出制氯气的离子方程式:
MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O
| ||
MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O
| ||
①实验装置的接口顺序为:b接
e
e
,f
f
接d
d
,c
c
接a;②装置D的作用是
吸收氯气
吸收氯气
;③在实验中,一组员认为该实验设计存有缺陷:不能证明最终通入AgNO3溶液中的气体只有一种.
为了确保实验结论的可靠性,证明最终通入AgNO3溶液的气体只有一种,他们提出在某两个装置之间再加装置E,如下图所示.你认为装置E应加在
BD
BD
之间(填装置序号),并且在广口瓶中放入湿润的KI淀粉试纸(或湿润的有色布条)
湿润的KI淀粉试纸(或湿润的有色布条)
(填写所用试剂或用品名称).
根据如图所示的转化关系回答问题.
(1)写出下列物质的化学式:E
(2)写出下列反应的离子方程式
A+B→
C+D→
F+G→
D+AgNO3→
查看习题详情和答案>>

(1)写出下列物质的化学式:E
KCl
KCl
FBr2
Br2
GKI
KI
XI2
I2
(2)写出下列反应的离子方程式
A+B→
MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O
| ||
MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O
;
| ||
C+D→
Cl2+2Br-═2Cl-+Br2
Cl2+2Br-═2Cl-+Br2
;F+G→
Br2+2I-═2Br-+I2
Br2+2I-═2Br-+I2
;D+AgNO3→
Br-+Ag+=AgBr↓
Br-+Ag+=AgBr↓
.(2013?青岛一模)某化学课外活动小组以海带为原料获得少量碘水,并以四氯化碳(沸点76.8℃)为溶剂将碘从碘水中提取出来,具体过程如图所示.

请回答下列问题:
(1)操作①的名称为
(2)操作②中用到氯气,请写出实验室制取氯气反应的离子方程式
(3)向含碘单质的水溶液中加入CCl4 振荡、静置后,观察到的现象是
(4)操作③中,将含碘单质的水溶液与CCl4在分液漏斗中混合、振荡摇匀放在铁架台的铁圈上,分液漏斗的下端尖嘴处紧贴在承接的烧杯内壁上静置后,下面的操作步骤是
(5)从含碘的有机溶剂中经过蒸馏可以提取碘和回收有机溶剂,该实验需要的主要玻璃仪器除酒精灯、烧杯、温度计、锥形瓶外,还需要
查看习题详情和答案>>

请回答下列问题:
(1)操作①的名称为
溶解
溶解
、过滤
过滤
;(2)操作②中用到氯气,请写出实验室制取氯气反应的离子方程式
MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O
| ||
MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O
;
| ||
(3)向含碘单质的水溶液中加入CCl4 振荡、静置后,观察到的现象是
溶液分层,上层为水层接近无色;下层为CCl4层呈紫红色
溶液分层,上层为水层接近无色;下层为CCl4层呈紫红色
;(4)操作③中,将含碘单质的水溶液与CCl4在分液漏斗中混合、振荡摇匀放在铁架台的铁圈上,分液漏斗的下端尖嘴处紧贴在承接的烧杯内壁上静置后,下面的操作步骤是
打开分液漏斗的玻璃塞(或将分液漏斗玻璃塞上的凹槽对准漏斗颈的小口),再转动打开活塞,使下层液体缓慢流下后,关闭活塞,将上层液体从上口倒出.
打开分液漏斗的玻璃塞(或将分液漏斗玻璃塞上的凹槽对准漏斗颈的小口),再转动打开活塞,使下层液体缓慢流下后,关闭活塞,将上层液体从上口倒出.
;(5)从含碘的有机溶剂中经过蒸馏可以提取碘和回收有机溶剂,该实验需要的主要玻璃仪器除酒精灯、烧杯、温度计、锥形瓶外,还需要
带铁圈的铁架台、蒸馏烧瓶、冷凝管、牛角管
带铁圈的铁架台、蒸馏烧瓶、冷凝管、牛角管
,实验中温度计水银球所处位置为蒸馏烧瓶支管口处
蒸馏烧瓶支管口处
,锥形瓶中收集到物质的名称为四氯化碳
四氯化碳
.(2012?青浦区二模)许多物质的氧化能力受溶液酸碱性的影响.高锰酸钾在不同条件下发生的还原反应如下:
MnO4-+5e+8H+→Mn2++4H2O MnO4-+3e+2H2O→MnO2+4OH-
MnO4-+e→MnO42-(溶液呈绿色)
MnO2的还原反应可表示如下:MnO2+4H++2e→Mn2++2H2O
(1)MnO2 与稀盐酸不能制取氯气,其原因是
(2)将SO2通入KMnO4溶液中,发生还原反应的过程为
(3)将PbO2投入到酸性MnSO4溶液中搅拌,溶液变为紫红色.下列叙述正确的是
a.氧化性:PbO2>KMnO4 b.还原性:PbO2>KMnO4 c.该反应可以用盐酸酸化
(4)将高锰酸钾溶液逐滴加入到硫化钾溶液中可发生如下反应,其中K2SO4和S的物质的量之比为3:2.完成并配平该反应的化学方程式.
反应若生成5.44g单质硫,反应过程中转移电子的物质的量为
查看习题详情和答案>>
MnO4-+5e+8H+→Mn2++4H2O MnO4-+3e+2H2O→MnO2+4OH-
MnO4-+e→MnO42-(溶液呈绿色)
MnO2的还原反应可表示如下:MnO2+4H++2e→Mn2++2H2O
(1)MnO2 与稀盐酸不能制取氯气,其原因是
MnO2在溶液酸性较强的环境中才有制取氯气的氧化能力
MnO2在溶液酸性较强的环境中才有制取氯气的氧化能力
.(2)将SO2通入KMnO4溶液中,发生还原反应的过程为
MnO4-
MnO4-
→Mn2+
Mn2+
(用化学式或离子符号表示).(3)将PbO2投入到酸性MnSO4溶液中搅拌,溶液变为紫红色.下列叙述正确的是
a
a
(选填编号).a.氧化性:PbO2>KMnO4 b.还原性:PbO2>KMnO4 c.该反应可以用盐酸酸化
(4)将高锰酸钾溶液逐滴加入到硫化钾溶液中可发生如下反应,其中K2SO4和S的物质的量之比为3:2.完成并配平该反应的化学方程式.
28
28
KMnO4+5
5
K2S+24KOH
24KOH
→28
28
K2MnO4+3
3
K2SO4+2
2
S↓+12H2O
12H2O
反应若生成5.44g单质硫,反应过程中转移电子的物质的量为
2.38mol
2.38mol
.