摘要:16.3Cu2O+2 NO3-+14H+== 6Cu2+ + 2 NO+7H2O (2)酸性.氧化性
网址:http://m.1010jiajiao.com/timu_id_170159[举报]
 I.图1是中学教材中铜与稀硝酸反应的实验装置,请就此回答下列问题:
I.图1是中学教材中铜与稀硝酸反应的实验装置,请就此回答下列问题:(1)试管A中发生反应的离子方程式是
3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
.(2)试管A中观察到的现象是
固体溶解,溶液变为蓝色;有无色气体产生,在试管上方变为红棕色,一段时间后又变为无色.
固体溶解,溶液变为蓝色;有无色气体产生,在试管上方变为红棕色,一段时间后又变为无色.
.(3)试管B中盛装NaOH溶液的目的是
除去产生的NOx,防止污染空气
除去产生的NOx,防止污染空气
.II.上述装置存在明显的不足,为克服上述缺点,某课外小组的学生设计了如图2所示的装置.
实验步骤如下:
①检查装置的气密性;
②向试管中加入一定量碳酸钙固体;
③向试管中加入过量稀硝酸,并迅速盖上带铜丝和导管的橡皮塞;
④待反应完全后,将导管插入试管内接近液面(如图);
⑤将铜丝插入到溶液中;⑥反应一段时间后,用注射器向试管内推入氧气(或空气).
请回答下列问题:
(4)实验中加入CaCO3的作用是
除去装置内的空气,防止生成的NO被氧化而影响实验效果
除去装置内的空气,防止生成的NO被氧化而影响实验效果
.(5)实验④的实验目的是
因NO的密度小于CO2,只有导管插入到液面,才能使密度小的NO聚集于试管内
因NO的密度小于CO2,只有导管插入到液面,才能使密度小的NO聚集于试管内
.(6)实验⑥中推入氧气或空气的目的是
确认反应产生并收集了NO气体
确认反应产生并收集了NO气体
.几种短周期元素的原子半径及某些化合价见下表:
分析上表中有关数据,并结合已学过的知识,回答以下问题.涉及上述元素的答案,请用元素符号表示.
(1)E元素在周期表中位于
(2)A、H、J对应的离子半径由大到小的顺序是(填写离子符号)
(3)A与J所形成化合物中的化学键类型是
 .
.
(4)B与H所形成的化合物与J的最高价氧化物的水化物X的溶液发生反应的离子方程式为
查看习题详情和答案>>
| 元素代号 | A | B | D | E | G | H | I | J |
| 化合价 | -1 | -2 | +4、-4 | +6、-2 | +5、-3 | +3 | +2 | +1 |
| 原子半径/nm | 0.071 | 0.074 | 0.077 | 0.102 | 0.110 | 0.143 | 0.160 | 0.186 |
(1)E元素在周期表中位于
第三
第三
周期,ⅥA
ⅥA
族;(2)A、H、J对应的离子半径由大到小的顺序是(填写离子符号)
F-、Na+、Al3+
F-、Na+、Al3+
(3)A与J所形成化合物中的化学键类型是
离子键
离子键
,用电子式表示其形成过程

(4)B与H所形成的化合物与J的最高价氧化物的水化物X的溶液发生反应的离子方程式为
Al2O3+2OH-═2AlO2-+H2O
Al2O3+2OH-═2AlO2-+H2O
.下表是元素周期表的一部分,表中所列字母分别代表某一化学元素.
(1)i是铁元素,其原子的最外层电子数为2,请写出铁元素的原子结构示意图
 .
.
(2)由以上元素形成的金属单质中,熔点最低的是
(3)NH3?H2O的电离方程式为NH3?H2O NH4++OH-,试判断NH3溶于水后,形成的NH3?H2O的合理结构是
NH4++OH-,试判断NH3溶于水后,形成的NH3?H2O的合理结构是
 (4)1906年的诺贝尔化学奖授予为制备F2单质作出重要贡献的化学家莫瓦桑,请预测首先被用来与F2反应制备稀有气体化合物的元素是
(4)1906年的诺贝尔化学奖授予为制备F2单质作出重要贡献的化学家莫瓦桑,请预测首先被用来与F2反应制备稀有气体化合物的元素是
(5)利用稀有气体化合物,人们实现了许多制备实验上的突破.如用XeO3在碱性条件下与NaBrO3反应生成NaBrO4,同时放出Xe.写出上述反应方程式:
(6)a与g形成的化合物是
查看习题详情和答案>>
| a | b | ||||||||||||||||
| c | d | ||||||||||||||||
| e | f | g | h | ||||||||||||||
| i | |||||||||||||||||
| j | |||||||||||||||||


(2)由以上元素形成的金属单质中,熔点最低的是
Na
Na
.(填元素符号)(3)NH3?H2O的电离方程式为NH3?H2O
 NH4++OH-,试判断NH3溶于水后,形成的NH3?H2O的合理结构是
NH4++OH-,试判断NH3溶于水后,形成的NH3?H2O的合理结构是(b)
(b)
(填序号). (4)1906年的诺贝尔化学奖授予为制备F2单质作出重要贡献的化学家莫瓦桑,请预测首先被用来与F2反应制备稀有气体化合物的元素是
(4)1906年的诺贝尔化学奖授予为制备F2单质作出重要贡献的化学家莫瓦桑,请预测首先被用来与F2反应制备稀有气体化合物的元素是j
j
(填写字母).(5)利用稀有气体化合物,人们实现了许多制备实验上的突破.如用XeO3在碱性条件下与NaBrO3反应生成NaBrO4,同时放出Xe.写出上述反应方程式:
XeO3+3NaBrO3═3NaBrO4+Xe↑
XeO3+3NaBrO3═3NaBrO4+Xe↑
.(6)a与g形成的化合物是
共价
共价
(填“离子”或“共价”)化合物. I、(1)NaHCO3是一种
I、(1)NaHCO3是一种强
强
(填“强”或“弱”)电解质;(2)写出HCO3-水解的离子方程式:
HCO3-+H2?H2CO3+OH-
HCO3-+H2?H2CO3+OH-
;(3)常温下,0.1mol?L-1NaHCO3溶液的pH大于8,则溶液中Na+、HCO3-、H2CO3、CO32-、OH- 五种微粒的浓度由大到小的顺序为:
c(Na+)>c(HCO3-)>c(OH-)>c(H2CO3)>c(CO32-)
c(Na+)>c(HCO3-)>c(OH-)>c(H2CO3)>c(CO32-)
.Ⅱ、醋酸是一种弱电解质. 某温度下,相同pH值的盐酸和醋酸溶液分别加水稀释,平衡pH值随溶液体积变化的曲线如图所示.则图
Ⅱ
Ⅱ
(填“I”或“Ⅱ”)为醋酸稀释的图象.Ⅲ、Ba(OH)2是一种强电解质,现有25℃、pH=13的Ba(OH)2溶液.
(1)溶液中由水电离出c(OH-)=
10-13mol/L
10-13mol/L
;(2)与某浓度盐酸溶液按体积比(碱与酸之比)1:9混合后,所得溶液pH=11(假设混合溶液的体积等于混合前两溶液的体积和),该盐酸溶液的pH=
2
2
.I.在过氧化氢中加入乙醚后,再加入数滴K2Cr2O7的硫酸溶液,轻轻振荡后静置,乙醚层呈蓝色,这是由于生成的过氧化铬(CrO5)溶于乙醚的缘故.已知过氧化铬的结构简式为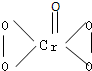 ?
?
(1)CrO5中氧元素的化合价为
(2)上述反应的离子方程式为
Ⅱ.下表是元素周期表的一部分,表中所列字母分别代表某一化学元素.
(1)i元素名称是
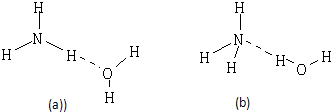
(2)NH3?H2O的电离方程式为NH3?H2O?NH4++OH-,试判断NH3溶于水后,形成的NH3?H2O的合理结构是
(3)用电子式表示e的过氧化物的形成过程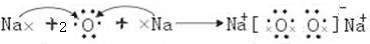
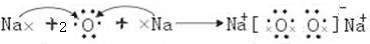 .
.
(4)利用稀有气体化合物,人们实现了许多制备实验上的突破.如XeO3在一定条件下与NaBrO3反应生成NaBrO4,同时放出Xe.写出上述反应方程式:
查看习题详情和答案>>
 ?
?(1)CrO5中氧元素的化合价为
一个O为-2价、4个O为-1价
一个O为-2价、4个O为-1价
.(2)上述反应的离子方程式为
Cr2O72-+4H2O2+2H+=2CrO5+5H2O
Cr2O72-+4H2O2+2H+=2CrO5+5H2O
.Ⅱ.下表是元素周期表的一部分,表中所列字母分别代表某一化学元素.
| a | b | ||||||||||||||||
| c | d | ||||||||||||||||
| e | f | g | h | ||||||||||||||
| i | j | ||||||||||||||||
锡
锡
.(2)NH3?H2O的电离方程式为NH3?H2O?NH4++OH-,试判断NH3溶于水后,形成的NH3?H2O的合理结构是
(b)
(b)
.(填序号)
(3)用电子式表示e的过氧化物的形成过程
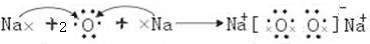
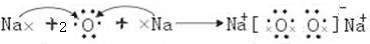
(4)利用稀有气体化合物,人们实现了许多制备实验上的突破.如XeO3在一定条件下与NaBrO3反应生成NaBrO4,同时放出Xe.写出上述反应方程式:
XeO3+3NaBrO3=3NaBrO4+Xe
XeO3+3NaBrO3=3NaBrO4+Xe
.