摘要:(1)图中所示反应是 反应△H是 E2-E1(用E1.E2表示).(2)已知热化学方程式:H2(g)+1/2 O2(g)=H2O(g) AH=-241.8 kJ?mol-1.该反应的活化能为
网址:http://m.1010jiajiao.com/timu_id_168956[举报]
 (1)图中所示反应是
(1)图中所示反应是放热
放热
(填“吸热”或“放热”)反应,该反应的△H=E2-E1
E2-E1
(用含E1、E2的代数式表示).(2)已知热化学方程式:H2(g)+
| 1 |
| 2 |
409.0kJ/mol
409.0kJ/mol
.(3)1L 1mol/L H2SO4溶液与2L 1mol/L NaOH溶液完全反应,放出114.6kJ的热量,由此推知H2SO4与NaOH反应的中和热的热化学方程式为
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
(4)向1L 1mol/L的NaOH溶液中加入:①浓H2SO4;②稀硝酸; ③稀醋酸,
恰好完全反应的热效应△H1、△H2、△H3的大小关系为
△H3>△H2>△H1
△H3>△H2>△H1
. 反应A(g)+B(g)?C(g)+D(g)过程中的能量变化如图所示,回答下列问题.
反应A(g)+B(g)?C(g)+D(g)过程中的能量变化如图所示,回答下列问题.(1)该反应是
放热
放热
(填“吸热”“放热”)反应.(2)当反应达到平衡时,升高温度,A的转化率
减小
减小
(填“增大”“减小”或“不变”),原因是该反应正反应为放热反应,升高温度使平衡向逆反应方向移动
该反应正反应为放热反应,升高温度使平衡向逆反应方向移动
.(3)反应体系中加入催化剂对反应热是否有影响并说明原因
不影响;催化剂不改变平衡的移动
不影响;催化剂不改变平衡的移动
.(4)在反应体系中加入催化剂,反应速率增大,E1和E2的变化是:?E1
减小
减小
,E2减小
减小
(填“增大”“减小”或“不变”).平衡向不会
不会
移动. 反应A(g)+B(g)?C(g)+D(g)过程中的能量变化如图所示,回答下列问题:
反应A(g)+B(g)?C(g)+D(g)过程中的能量变化如图所示,回答下列问题:(1)该反应是
放热
放热
反应(填“吸热”“放热”);△H<
<
(填“<0”或“>0”).(2)当反应达到平衡时,升高温度,A的转化率
减小
减小
(填“增大”“减小”“不变”),原因是该反应正反应为放热反应,升高温度使平衡向逆反应方向移动
该反应正反应为放热反应,升高温度使平衡向逆反应方向移动
.(3)反应体系中加入催化剂对反应热是否有影响?
不影响,催化剂不改变平衡的移动
不影响,催化剂不改变平衡的移动
.(4)在反应体系中加入催化剂,反应速率增大,E1和E2的变化是:E1
减小
减小
,E2减小
减小
(填“增大”“减小”、“不变”).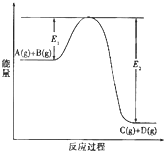 反应A(g)+B(g)?C(g)+D(g)过程中的能量变化如图所示,回答下列问题.
反应A(g)+B(g)?C(g)+D(g)过程中的能量变化如图所示,回答下列问题.(1)该反应是
(2)当反应达到平衡时,升高温度,正反应速率变化是
(3)在该反应体系中加入催化剂,反应速率增大,E1和E2的变化是:E1
(6分)反应物与生成物均为气态的某可逆反应在不同条件下的反应历程分别为A、B,如图所示。
(1)据图判断该反应是___①___(填“吸”或“放”)热反应,当反应达到平衡后,其他条件不变,升高温度,反应物的转化率__②__ (填“增大”、“减小”或“不变”)
(2)其中B历程表明此反应采用的条件为___③___ (选填下列序号字母),作出正确的判断的理由为__④____
A、升高温度 B、增大反应物的浓度 C、降低温度 D、使用了催化剂
(3)若△H的数值为200KJ/mol,则此反应在A反应历程中的正反应的活化能为___⑤___KJ/mol,x值应为 ___⑥___KJ/mol
查看习题详情和答案>>