摘要:(4)已知0.5mol被氧化成气态.放出49.15KJ热量.其热化学方程式为 .
网址:http://m.1010jiajiao.com/timu_id_168897[举报]
一.选择题(48分)
题号
1
2
3
4
5
6
7
8
答案
A
D
A
C
B
C
B
B
题号
9
10
11
12
13
14
15
16
答案
A
D
C
C
B
B
D
A
二.非选择题(52分)
17.(1) .
. (2)
(2) .
. (3)
(3)
(4) (每空2分,答错或少答1个扣1分,扣到0分为止)
(每空2分,答错或少答1个扣1分,扣到0分为止)
18.(1)验证锂.钠.钾的活泼性(或同一主族,从上到下元素的金属性逐渐增强)(2分);c(1分)
(2)① (各1分)
(各1分)
② (或
(或 (2分)
(2分)
19.(1)第三周期 ⅦA(1分)
(2) 氯碱(2分)
氯碱(2分)

(3)
(4) ;
; KJ/mol(2分)
KJ/mol(2分)
或 ;
; KJ/mol
KJ/mol
(5)离子晶体(1分)
20.(1)硫  离子键.非极性键(4分)
离子键.非极性键(4分)
(2) (2分)
(2分)
(3)① (2分)
(2分)
② (2分)
(2分)
21.(1)
(2)分液漏斗(1分)
(3)饱和食盐水(或饱和氯水)(1分)浓硫酸(1分)
(4) (1分)酒精(汽油.苯等有机溶剂或其他合理答案)(1分)
(1分)酒精(汽油.苯等有机溶剂或其他合理答案)(1分)
(5)使生成的 升华,与其他固体分离(2分)
升华,与其他固体分离(2分)
(6)吸收多余的 ,防止污染空气(1分)
,防止污染空气(1分)
(7)连接 的导管易被
的导管易被 固体堵塞(2分)
固体堵塞(2分)
22.(1)0.16 (2)0.03 0.05 (3)5.72
某校活动小组用图示的装置及所给药品(图中夹持仪器已略去)探究工业制硫酸接触室中的反应,并测定此条件下二氧化硫的转化率.已知C中的浓硫酸含溶质m mol,假设气体进入C和D时分别被完全吸收,且忽略装置内空气中的CO2.
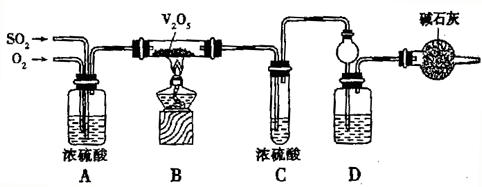
请回答下列问题:
(1)已知0.5mol SO2被O2氧化成气态SO3,放出49.15kJ热量,反应的热化学方程式为
(2)实验时装置A的作用是
①充分混合SO2和O2,②干燥作用,③通过流速控制两种气体的比例;
装置C中浓硫酸的作用为
装置D中盛放的溶液是足量的
a.BaCl2溶液 b.NaOH溶液 c.NaHSO3饱和溶液
(3)停止通入SO2,熄灭酒精灯后,为使残留在装置中的SO2、SO3被充分吸收,操作方法是
(4)实验结束,稀释装置C中的溶液,并向其中加入足量的BaCl2溶液,得到的沉淀质量为w g.若装置D增加的质量为a g,则此条件下二氧化硫的转化率是
×100%
×100%(用含字母的代数式表示,结果可不化简).
(5)以上实验方法存在一个严重的漏洞,导致转化率比实际值偏小,你认为是哪一个装置中的漏洞
A.A B.B C.C D.D
是什么漏洞?
查看习题详情和答案>>

请回答下列问题:
(1)已知0.5mol SO2被O2氧化成气态SO3,放出49.15kJ热量,反应的热化学方程式为
SO2(g)+
O2(g)?SO3(g)△H=-98.3kJ?mol-1
| 1 |
| 2 |
SO2(g)+
O2(g)?SO3(g)△H=-98.3kJ?mol-1
;| 1 |
| 2 |
(2)实验时装置A的作用是
②③
②③
,(填序号)①充分混合SO2和O2,②干燥作用,③通过流速控制两种气体的比例;
装置C中浓硫酸的作用为
吸收SO3
吸收SO3
;装置D中盛放的溶液是足量的
b
b
(填序号)a.BaCl2溶液 b.NaOH溶液 c.NaHSO3饱和溶液
(3)停止通入SO2,熄灭酒精灯后,为使残留在装置中的SO2、SO3被充分吸收,操作方法是
继续通入氧气一段时间
继续通入氧气一段时间
;(4)实验结束,稀释装置C中的溶液,并向其中加入足量的BaCl2溶液,得到的沉淀质量为w g.若装置D增加的质量为a g,则此条件下二氧化硫的转化率是
| ||||
|
| ||||
|
(5)以上实验方法存在一个严重的漏洞,导致转化率比实际值偏小,你认为是哪一个装置中的漏洞
C
C
,A.A B.B C.C D.D
是什么漏洞?
C装置中三氧化硫不一定被完全吸收
C装置中三氧化硫不一定被完全吸收
.为探究工业制硫酸接触室中的反应,并测定此条件下二氧化硫的转化率,甲同学设计了如图装置(图中部分夹持仪器已略去).已知SO3熔点为16.8℃,假设气体进入装置时分别被完全吸收,且忽略装置内空气中的CO2.

(1)开始进行实验时,首先应进行的操作是 .停止通入SO2,熄灭酒精灯后,为使残留在装置中的SO2、SO3被充分吸收,操作方法是 .
(2)已知0.5mol SO2被O2氧化成气态SO3,放出49.15kJ热量,反应的热化学方程式为 .
(3)实验结束后,若装置D增加的质量为a g,装置E增加的质量为b g,则此条件下二氧化硫的转化率是 (用含字母的代数式表示).
(4)为探究反应后E中的可能生成物,同学们提出了几种假设:
假设1:只有亚硫酸钠;
假设2:只有硫酸钠;
假设3: .
乙同学通过实验证明了假设3成立.请帮助乙同学完成实验操作和现象 .
查看习题详情和答案>>

(1)开始进行实验时,首先应进行的操作是
(2)已知0.5mol SO2被O2氧化成气态SO3,放出49.15kJ热量,反应的热化学方程式为
(3)实验结束后,若装置D增加的质量为a g,装置E增加的质量为b g,则此条件下二氧化硫的转化率是
(4)为探究反应后E中的可能生成物,同学们提出了几种假设:
假设1:只有亚硫酸钠;
假设2:只有硫酸钠;
假设3:
乙同学通过实验证明了假设3成立.请帮助乙同学完成实验操作和现象