摘要:c.微粒中价电子对数为:n=(中心原子的价电子数+每个配位原子提供的价电子数±微粒所带的电荷数)/2(微粒带负电荷时取“+ .带正电荷时取“- ).主族元素的价电子数等于最外层电子数.氢和卤素作为配位原子时.提供一个电子.当ⅥA族元素作为配位原子时.认为不提供电子(由价电子对数可确定中心原子的杂化形式:电子对数分别为2.3.4时.中心原子分别采取sp.sp2.sp3杂化).d.当配位原子不是氢.ⅥA.ⅦA族元素时.可运用等电子原理.寻找其熟悉的等电子体来判断其构型.④ 等电子原理a.具有相同原子数目和相同电子总数的分子或离子具有相同的结构特征.b.常见等电子体:N2.CO.CN?.C22?(电子总数为14e?.存在叁键),CO2.CS2.COS.BeCl2.N3?.OCN?.SCN?(价电子数为16e?.均为直线型),BCl3.CO32?.SiO32?.NO3?(价电子数为24e?.均为平面正三角形),NCl3.PCl3.NF3.PF3.SO32?(价电子数为24e?.均为三角锥形),SiCl4.CCl4.SiO44?.SO42?.PO43?(价电子数为24e?.均为正四面体形).(3)分子极性:分子中正.负电荷重心是否重合
网址:http://m.1010jiajiao.com/timu_id_162154[举报]
水是生命之源,也是一种常用的试剂。请回答下列问题:
(1)水分子中氧原子在基态时核外电子排布式为 。
(2)H2O分子中氧原子采取的是 杂化。
(3)水分子容易得到一个H+形成水合氢离子(H3O+)。对上述过程的下列描述不合理的是 。
A.氧原子的杂化类型发生了改变 B.微粒的空间构型发生了改变
C.微粒中的键角发生了改变
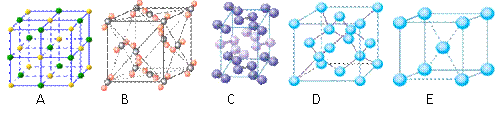
(4)下列是钠、碘、金刚石、干冰、氯化钠晶体的晶胞图(未按顺序排序)。与冰的晶体类型相同的是______。(请用相应的编号填写)
 |

(5)在冰晶体中,每个水分子与相邻的4个水分子形成氢键(如图所示),已知冰的升华热是51 kJ/mol,除氢键外,水分子间还存在范德华力(11 kJ/mol),则冰晶体中氢键的“键能”是_________kJ/mol。
(6)将白色的无水CuSO4溶解于水中,溶液呈蓝色,是因为生成了一种呈蓝色的配合离子。请写出生成此配合离子的离子方程式: 。
查看习题详情和答案>>下列说法正确的是()
- A.任何微粒,其核电荷数均等于核外电子数
- B.原子核都是由质子和中子构成的,且质子数与核外电子数相等
- C.任何微粒中一定含有质子可能不含有中子与电子
- D.主族元素的金属阳离子核外电子数一定与上一周期稀有气体元素的核外电子数相同
(08龙岩一中三模)学习化学时会遇到一些与“相等”有关的规律,下列有关“相等”的说法中正确的是()
A.溶液稀释前后,溶质的质量一定相等
B.中和反应中参加反应的酸和碱的质量一定相等
C.微粒中的质子总数和电子总数一定相等
D.物质发生化学变化前后,分子的总数一定相等
查看习题详情和答案>>[化学--物质结构与性质]
氮元素可以形成多种分子和离子,如NH3、N2H4、N3-、NH4+、N2H62+等.
回答以下问题:
(1)某元素原子与N3-含有相同的电子数,其基态原子的价电子排布式是 .
(2)C、N、O三种元素第一电离能从大到小的顺序是 .
(3)肼(N2H4)分子可视为NH3分子中的一个氢原子被一NH2(氨基)取代形成的另一种氮的氢化物.NH3分子的空间构型是 ; N2H4分子中氮原子轨道的杂化类型是
(4)胼能与硫酸反应生成N2H6S04.N2H6S04晶体类型与硫酸铵相同,则N2H6S04的晶体内不存在 (填标号)
a.离子键 b.共价键 c.配位键 d.范德华力
(5)NH3、N2H4、NH4+、N2H62+四种微粒中,能形成氢键的有 ;不能作为配位体的有 .
查看习题详情和答案>>
氮元素可以形成多种分子和离子,如NH3、N2H4、N3-、NH4+、N2H62+等.
回答以下问题:
(1)某元素原子与N3-含有相同的电子数,其基态原子的价电子排布式是
(2)C、N、O三种元素第一电离能从大到小的顺序是
(3)肼(N2H4)分子可视为NH3分子中的一个氢原子被一NH2(氨基)取代形成的另一种氮的氢化物.NH3分子的空间构型是
(4)胼能与硫酸反应生成N2H6S04.N2H6S04晶体类型与硫酸铵相同,则N2H6S04的晶体内不存在
a.离子键 b.共价键 c.配位键 d.范德华力
(5)NH3、N2H4、NH4+、N2H62+四种微粒中,能形成氢键的有