摘要:① Al3+(或Fe3+)与HCO3?.CO32?:Al3++3HCO3?Al(OH)3↓+3CO2↑
网址:http://m.1010jiajiao.com/timu_id_162095[举报]
A、B、C、D都是中学化学常见的物质,其中A、B、C均含有同一种元素.在一定条件下相互转化的关系知图所示.

请回答下列问题:
(1)若D为用量最大、用途最广的金属单质,加热蒸干B的溶液没有得到B的盐,则B的化学式可能为
(2)若通常情况下A、B、C、D都是气体,且B和D为空气的主要成分,则A的电子式为
 ,B的结构式为
,B的结构式为
(3)若D为氯碱工业的重要产品,反应(Ⅲ)的离子方程式为
(4)若A、B、C的溶液均显碱性,C为焙制糕点的发酵粉的主要成分之一,也可作为医疗上治疗胃酸过多症的药剂.
①25℃时,pH均为10的A、B两溶液中,由水电离出的氢氧根离子浓度之比为
②25℃时,0.1mol?L-1的A、B、C三种溶液,分别用水稀释不同的倍数后,溶液的pH相同,则稀释后溶液的物质的量浓度最大的是
③将等物质的量的B和C溶于水形成混合溶液,溶液中各种离子浓度由大到小顺序为
查看习题详情和答案>>

请回答下列问题:
(1)若D为用量最大、用途最广的金属单质,加热蒸干B的溶液没有得到B的盐,则B的化学式可能为
FeCl3或Fe(NO3)3
FeCl3或Fe(NO3)3
.(写出一种即可)(2)若通常情况下A、B、C、D都是气体,且B和D为空气的主要成分,则A的电子式为


N≡N
N≡N
.(3)若D为氯碱工业的重要产品,反应(Ⅲ)的离子方程式为
Al3++3AlO2-+6H2O=4Al(OH)3↓
Al3++3AlO2-+6H2O=4Al(OH)3↓
.(4)若A、B、C的溶液均显碱性,C为焙制糕点的发酵粉的主要成分之一,也可作为医疗上治疗胃酸过多症的药剂.
①25℃时,pH均为10的A、B两溶液中,由水电离出的氢氧根离子浓度之比为
10-6:1或1:106
10-6:1或1:106
②25℃时,0.1mol?L-1的A、B、C三种溶液,分别用水稀释不同的倍数后,溶液的pH相同,则稀释后溶液的物质的量浓度最大的是
NaHCO3
NaHCO3
溶液(填溶质的化学式).③将等物质的量的B和C溶于水形成混合溶液,溶液中各种离子浓度由大到小顺序为
c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+)
c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+)
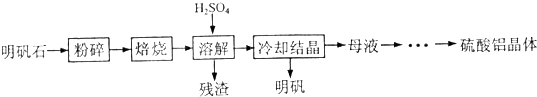
.以明矾石[主要成分为K2SO4?Al2(SO4)3?2Al2O3?6H2O]为原料生产硫酸铝晶体[Al2(SO4)3?18H2O]和明矾[KAl(SO4)2?12H2O]的实验流程如下:
两种不同形态的氧化铝的部分性质如下表:
Al2(SO4)3、明矾在不同温度下的溶解度如下表:
(1)①理论上得到硫酸铝晶体与明矾的物质的量之比为 .
②“焙烧”温度过高,会导致硫酸铝晶体产量降低,其原因是 .
(2)从“母液”制备硫酸铝晶体的实验步骤为:① ;② ;③过滤、洗涤、干燥.
(3)测定硫酸铝晶体样品中Al2(SO4)3?18H2O质量分数的实验步骤为(EDTA分别能与Al3+或Pb2+以物质的量之比1:1进行反应):
步骤1:准确称取硫酸铝晶体样品mg,溶于25mL水中.
步骤2:加入c1 mol?L-1EDTA溶液V1mL(过量),煮沸、冷却,稀释至100mL.
步骤3:取25.00mL上述稀释液,滴加指示剂,用c2 mol?L-1 Pb(NO3)2标准溶液滴定过量的EDTA溶液,达到终点时消耗v2mL Pb(NO3)2标准溶液.
①步骤2中“稀释至100mL”时,需要用到的玻璃仪器有烧杯、玻璃棒、量筒、 .
②根据上述数据计算,该样品中Al2(SO4)3?18H2O的质量分数为 (用含字母的代数式表示).
③若样品中含有可与EDTA反应的杂质离子,所测定的Al2(SO4)3?18H2O的质量分数将会 (填“偏高”、“偏低”或“不变”).
查看习题详情和答案>>

两种不同形态的氧化铝的部分性质如下表:
| 物质 | α-Al2O3 | γ-Al2O3 |
| 性质 | 不溶于水和酸 | 不溶于水,溶于强酸或强碱,加热至1200℃可转化为α-Al2O3 |
| 温度/℃ 溶解度/g |
0 | 20 | 40 | 60 | 80 | 100 |
| Al2(SO4)3 | 31.2 | 36.4 | 46.1 | 59.2 | 73.0 | 89.0 |
| 明矾 | 3.0 | 5.9 | 11.7 | 25 | 71 | 154 |
②“焙烧”温度过高,会导致硫酸铝晶体产量降低,其原因是
(2)从“母液”制备硫酸铝晶体的实验步骤为:①
(3)测定硫酸铝晶体样品中Al2(SO4)3?18H2O质量分数的实验步骤为(EDTA分别能与Al3+或Pb2+以物质的量之比1:1进行反应):
步骤1:准确称取硫酸铝晶体样品mg,溶于25mL水中.
步骤2:加入c1 mol?L-1EDTA溶液V1mL(过量),煮沸、冷却,稀释至100mL.
步骤3:取25.00mL上述稀释液,滴加指示剂,用c2 mol?L-1 Pb(NO3)2标准溶液滴定过量的EDTA溶液,达到终点时消耗v2mL Pb(NO3)2标准溶液.
①步骤2中“稀释至100mL”时,需要用到的玻璃仪器有烧杯、玻璃棒、量筒、
②根据上述数据计算,该样品中Al2(SO4)3?18H2O的质量分数为
③若样品中含有可与EDTA反应的杂质离子,所测定的Al2(SO4)3?18H2O的质量分数将会
