摘要:下列说法错误的是: A.Al的第一电离能的大小范围为Na<Al<Mg B.从上图分析可知.同一主族元素原子的第一电离能I1变化规律是从上到下依次增大 C.上图中第一电离能最小的元素在周期表中的位置是第五周期.IA族 D.根据对角线规则.Be.Al元素最高氧化物水化物的性质相似.它们都具有两性.
网址:http://m.1010jiajiao.com/timu_id_133285[举报]


本资料由《七彩教育网》www.7caiedu.cn 提供!
|
第一电离能I1是指气态原子X(g)处于基态时,失去一个电子成为气态阳离子X+(g)所需的能量.下图是部分元素原子的第一电离能I1随原子序数变化的曲线图(其中12号至17号元素的有关数据缺失).
下列说法错误的是: | |
A. |
Al的第一电离能的大小范围为Na<Al<Mg |
B. |
从上图分析可知,同一主族元素原子的第一电离能I1变化规律是从上到下依次增大 |
C. |
上图中第一电离能最小的元素在周期表中的位置是第五周期,IA族 |
D. |
根据对角线规则,Be、Al元素最高氧化物水化物的性质相似,它们都具有两性. |
I.下列描述中正确的是
A.CS2为V形的极性分子 B.Cl0-3 的空间构型为平面三角形
C.SF6中有6对完全相同的成键电子对 D.SiF4和SO2-3 的中心原子均为sp3杂化
Ⅱ.下列说法中错误的是:
A.SO2、SO3都是极性分子
B.在NH4+ 和[Cu(NH3)4]2+中都存在配位键
C.元素电负性越大的原子,吸引电子的能力越强
D.原子晶体中原子以共价键结合,具有键能大、熔点高、硬度大的特性
Ⅲ.雷尼镍(Raney-Ni)是一种历史悠久、应用广泛的催化剂,由镍-铝合金为原料制得.
(1)元素第一电离能:Al Mg(选填:“>”、“<”、“=”)
(2)雷尼镍催化的一实例为: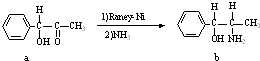
化合物b中进行sp3杂化的原子有: .
(3)一种铝镍合金的结构如图,与其结构相似的化合物是: (选填序号:a.氯化钠 b.氯化铯 c.石英 d.金刚石).
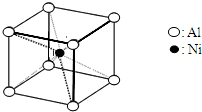
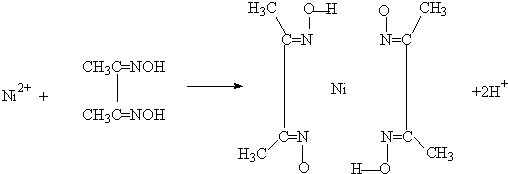
(4)实验室检验Ni2+可用丁二酮肟与之作用生成腥红色配合物沉淀.
①Ni2+在基态时,核外电子排布式为: .
②在配合物中用化学键和氢键标出未画出的作用力(镍的配位数为4).
 查看习题详情和答案>>
查看习题详情和答案>>
A.CS2为V形的极性分子 B.Cl0-3 的空间构型为平面三角形
C.SF6中有6对完全相同的成键电子对 D.SiF4和SO2-3 的中心原子均为sp3杂化
Ⅱ.下列说法中错误的是:
A.SO2、SO3都是极性分子
B.在NH4+ 和[Cu(NH3)4]2+中都存在配位键
C.元素电负性越大的原子,吸引电子的能力越强
D.原子晶体中原子以共价键结合,具有键能大、熔点高、硬度大的特性
Ⅲ.雷尼镍(Raney-Ni)是一种历史悠久、应用广泛的催化剂,由镍-铝合金为原料制得.
(1)元素第一电离能:Al
(2)雷尼镍催化的一实例为:

化合物b中进行sp3杂化的原子有:
(3)一种铝镍合金的结构如图,与其结构相似的化合物是:

(4)实验室检验Ni2+可用丁二酮肟与之作用生成腥红色配合物沉淀.
①Ni2+在基态时,核外电子排布式为:
②在配合物中用化学键和氢键标出未画出的作用力(镍的配位数为4).
 查看习题详情和答案>>
查看习题详情和答案>>
