摘要:解: x = 13g y = 32.2g 15g?13g== 2g
网址:http://m.1010jiajiao.com/timu_id_131283[举报]
 (2013?雨花台区一模)实验室欲用已配好的质量分数为10%的氢氧化钠溶液(密度为1.1g/cm3),配制100g质量分数为5%的氢氧化钠溶液,并用此溶液测定某硫酸溶液的溶质质量分数.
(2013?雨花台区一模)实验室欲用已配好的质量分数为10%的氢氧化钠溶液(密度为1.1g/cm3),配制100g质量分数为5%的氢氧化钠溶液,并用此溶液测定某硫酸溶液的溶质质量分数.(1)配制100g质量分数为5%的氢氧化钠溶液,需要10%的氢氧化钠溶液
50
50
g.(2)配制氢氧化钠溶液时,需要的玻璃仪器有
量筒
量筒
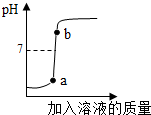
、滴管、烧杯、玻璃棒.(3)用配得的氢氧化钠溶液与待测溶质质量分数的硫酸溶液反应,实验过程中溶液的pH变化曲线如图所示:
①根据如图变化曲线,判断进行的操作是
B
B
(填字母).A.将硫酸溶液逐滴滴加到氢氧化钠溶液中
B.将氢氧化钠溶液逐滴滴加到硫酸溶液中
②b点对应的溶液中的溶质为
Na2SO4、NaOH
Na2SO4、NaOH
(写化学式).(4)若完全中和50g稀硫酸溶液,恰好消耗配得的氢氧化钠溶液80g.试计算该稀硫酸的溶质质量分数(请写出计算过程)
设该稀硫酸中溶质的质量为x
2NaOH+H2SO4 ═Na2SO4 +2H2O
80 98
80g×5% X
根据:
=
解得X=4.9g
该稀硫酸的溶质质量分数为:
×100%=9.8%.
2NaOH+H2SO4 ═Na2SO4 +2H2O
80 98
80g×5% X
根据:
| 80 |
| 98 |
| 80g×5% |
| X |
该稀硫酸的溶质质量分数为:
| 4.9g |
| 50g |
设该稀硫酸中溶质的质量为x
2NaOH+H2SO4 ═Na2SO4 +2H2O
80 98
80g×5% X
根据:
=
解得X=4.9g
该稀硫酸的溶质质量分数为:
×100%=9.8%.
.2NaOH+H2SO4 ═Na2SO4 +2H2O
80 98
80g×5% X
根据:
| 80 |
| 98 |
| 80g×5% |
| X |
该稀硫酸的溶质质量分数为:
| 4.9g |
| 50g |
现有一种不纯的氧化铜粉末样品(杂质为铜粉),小刚和小强通过实验测定样品中氧化铜的质量分数.(提示:CuO+CO
Cu+CO2)请你回答相关问题:
(1)小刚称取10g样品,利用下图所示装置进行实验,充分反应后,B装置增重4.4g,据此计算氧化铜样品中氧化铜的质量分数.
解:
答:
(2)小强同学用同样的装置进行实验,实验结果与小刚所得的正确结果比较,出现偏差,请你分析造成误差的可能原因
(3)小刚是利用还原氧化铜的原理进行测定,请你简要写出其他测定样品中氧化铜的质量分数的方法和要测定的数据.(用文字叙述,无需写出具体质量数值)
查看习题详情和答案>>
| ||
(1)小刚称取10g样品,利用下图所示装置进行实验,充分反应后,B装置增重4.4g,据此计算氧化铜样品中氧化铜的质量分数.
解:
B装置增重4.4g,为反应生成的二氧化碳的质量,设参见反应氧化铜的质量为x.
CuO+CO
Cu+CO2
8044
x 4.4g
=
解得x=8.0g
该样品中氧化铜的质量分数=
×100%=80%
CuO+CO
| ||
8044
x 4.4g
| 80 |
| 44 |
| x |
| 4.4g |
解得x=8.0g
该样品中氧化铜的质量分数=
| 8.0g |
| 10g |
B装置增重4.4g,为反应生成的二氧化碳的质量,设参见反应氧化铜的质量为x.
CuO+CO
Cu+CO2
8044
x 4.4g
=
解得x=8.0g
该样品中氧化铜的质量分数=
×100%=80%
CuO+CO
| ||
8044
x 4.4g
| 80 |
| 44 |
| x |
| 4.4g |
解得x=8.0g
该样品中氧化铜的质量分数=
| 8.0g |
| 10g |

答:
该样品中氧化铜的质量分数80%
该样品中氧化铜的质量分数80%
(2)小强同学用同样的装置进行实验,实验结果与小刚所得的正确结果比较,出现偏差,请你分析造成误差的可能原因
若过早停止通氢气,使氧化铜没有被完全还原
若过早停止通氢气,使氧化铜没有被完全还原
.(3)小刚是利用还原氧化铜的原理进行测定,请你简要写出其他测定样品中氧化铜的质量分数的方法和要测定的数据.(用文字叙述,无需写出具体质量数值)
先测出氧化铜样品的质量,再测出氧化铜样品和玻璃管的质量,然后通一氧化碳气体使其和氧化铜完全反应,实验结束后测固体和玻璃管的质量,根据质量减少的部分是氧化铜中氧元素的质量,计算出氧化铜的质量,再根据质量分数公式计算样品中氧化铜的质量分数
先测出氧化铜样品的质量,再测出氧化铜样品和玻璃管的质量,然后通一氧化碳气体使其和氧化铜完全反应,实验结束后测固体和玻璃管的质量,根据质量减少的部分是氧化铜中氧元素的质量,计算出氧化铜的质量,再根据质量分数公式计算样品中氧化铜的质量分数
.化学实验基本操作在化学学习和研究中具有重要作用.现有a试管、b漏斗、c酒精灯、d烧杯、e药匙、f胶头滴管、g量筒(10mL,50mL,100mL)等仪器,请回答下列问题.
(1)吸取或滴加少量液体使用
(2)可以直接在酒精灯火焰上加热的玻璃仪器是
(3)某同学欲用98%的浓硫酸(密度为1.84g/cm3),配制150g 10%的稀硫酸.
①完成本实验除以上提供的仪器外,还需要的玻璃仪器是
②配制溶液过程中,需要量取
(请写出计算过程
③量取浓硫酸时,该同学俯视量筒的刻度线读数(其他操作无误),则所配得溶液的溶质质量分数
查看习题详情和答案>>
(1)吸取或滴加少量液体使用
f
f
;(用序号填空)(2)可以直接在酒精灯火焰上加热的玻璃仪器是
a
a
;(用序号填空)(3)某同学欲用98%的浓硫酸(密度为1.84g/cm3),配制150g 10%的稀硫酸.
①完成本实验除以上提供的仪器外,还需要的玻璃仪器是
玻璃棒
玻璃棒
;②配制溶液过程中,需要量取
8.3
8.3
mL的浓硫酸,选用10
10
mL的量筒.(请写出计算过程
设需要浓硫酸体积为X则:150g×10%=X×1.84g/cm3×98%解得X=8.3mL
设需要浓硫酸体积为X则:150g×10%=X×1.84g/cm3×98%解得X=8.3mL
,计算结果保留一位小数)③量取浓硫酸时,该同学俯视量筒的刻度线读数(其他操作无误),则所配得溶液的溶质质量分数
偏小
偏小
(填“偏大”、“偏小”或“无影响”).(2013?江宁区一模)对牙膏的探究要用到许多化学知识.
(1)用作牙膏摩擦剂的轻质碳酸钙,工业上常用石灰石来制备,某实验小组同学设计了2种转化流程,如下图1所示.
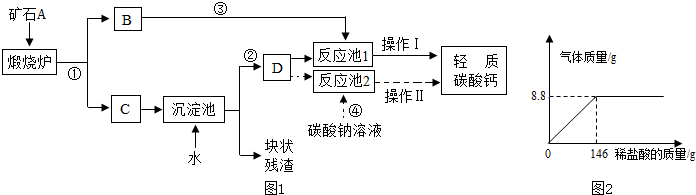 请回答下列问题:
请回答下列问题:
a.小王同学主张用流程①、②、④和操作Ⅱ的设计,认为其工艺简单.
请写出反应①和④的化学方程式:①
b.操作Ⅱ包括搅拌、
c.小李同学认为流程①、②、③和操作I比小王的主张更好,其理由是:
操作I包括搅拌和微热等工序.
(2)该实验小组为了测定某石灰石样品中碳酸钙的质量分数,取25g石灰石样品放在烧杯中,然后向其中逐滴加入一定量某质量分数的稀盐酸,使之与样品充分反应(杂质不参加反应).随着反应进行,加入稀盐酸的质量与反应得到气体的质量变化关系如图2所示.请完成下列计算内容:
①样品中碳酸钙的质量分数是多少?
②所用稀盐酸溶质的质量分数是多少?
(写出计算过程)
查看习题详情和答案>>
(1)用作牙膏摩擦剂的轻质碳酸钙,工业上常用石灰石来制备,某实验小组同学设计了2种转化流程,如下图1所示.
 请回答下列问题:
请回答下列问题:a.小王同学主张用流程①、②、④和操作Ⅱ的设计,认为其工艺简单.
请写出反应①和④的化学方程式:①
CaCO3
CaO+CO2↑
| ||
CaCO3
CaO+CO2↑
;④
| ||
Ca(OH)2+Na2CO3═CaCO3↓+2NaOH
Ca(OH)2+Na2CO3═CaCO3↓+2NaOH
;b.操作Ⅱ包括搅拌、
过滤
过滤
、洗涤、干燥等工序.c.小李同学认为流程①、②、③和操作I比小王的主张更好,其理由是:
利用产生的二氧化碳比另加碳酸钠溶液更经济,生成成本更低,若产生的二氧化碳不回收直接排放,不利于“节能减排”
利用产生的二氧化碳比另加碳酸钠溶液更经济,生成成本更低,若产生的二氧化碳不回收直接排放,不利于“节能减排”
;操作I包括搅拌和微热等工序.
(2)该实验小组为了测定某石灰石样品中碳酸钙的质量分数,取25g石灰石样品放在烧杯中,然后向其中逐滴加入一定量某质量分数的稀盐酸,使之与样品充分反应(杂质不参加反应).随着反应进行,加入稀盐酸的质量与反应得到气体的质量变化关系如图2所示.请完成下列计算内容:
①样品中碳酸钙的质量分数是多少?
②所用稀盐酸溶质的质量分数是多少?
(写出计算过程)
解:设样品中CaCO3的质量为x,参加反应的稀盐酸中HCl的质量为y
CaCO3+2HCl=CaCl2+CO2↑+H2O
1007344
xy8.8g
根据
=
解得x=20 根据
=
解得y=14.6g
样品中CaCO3的质量分数为:
×100%=80%
稀盐酸的溶质质量分数为:
×100%=10%
CaCO3+2HCl=CaCl2+CO2↑+H2O
1007344
xy8.8g
根据
| 100 |
| 44 |
| X |
| 8.8g |
| 73 |
| 44 |
| Y |
| 8.8g |
样品中CaCO3的质量分数为:
| 20g |
| 25g |
稀盐酸的溶质质量分数为:
| 14.6g |
| 146g |
解:设样品中CaCO3的质量为x,参加反应的稀盐酸中HCl的质量为y
CaCO3+2HCl=CaCl2+CO2↑+H2O
1007344
xy8.8g
根据
=
解得x=20 根据
=
解得y=14.6g
样品中CaCO3的质量分数为:
×100%=80%
稀盐酸的溶质质量分数为:
×100%=10%
.CaCO3+2HCl=CaCl2+CO2↑+H2O
1007344
xy8.8g
根据
| 100 |
| 44 |
| X |
| 8.8g |
| 73 |
| 44 |
| Y |
| 8.8g |
样品中CaCO3的质量分数为:
| 20g |
| 25g |
稀盐酸的溶质质量分数为:
| 14.6g |
| 146g |
在一个密闭容器中放人甲、乙、丙、丁四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表:[来源:Z*xx*k.Com]
|
物质 |
甲 |
乙 |
丙 |
丁 |
|
反应前质量/g |
18 |
1 |
2 |
32 |
|
反应后质量/g |
X(未知)[来源:ZXXK] |
26 |
2 |
12 |
下列说法中,不正确的是:( )
A.反应后X=13g B.物质丙可能是该反应的催化剂
C.乙是反应物 D.反应中乙、丁的质量比为5∶4
查看习题详情和答案>>