网址:http://m.1010jiajiao.com/timu_id_128901[举报]
1-5ADCAB 6-10CDACC 11-15ACDBD 16-20CCDBC 21-22DD
23.化学能 2.52×106 0.06 24.电流 焦耳定律(Q=I2Rt) 大功率用电器交叉使用或换电阻较小的输电线等 25.沿直线传播 折射 缩小
26.(1)B(2)电磁感应(3)三 为了防止用电器漏电造成的触电事故(4)电源线要符合要求;放置电磁炉的桌面要平整,电磁炉在使用中要注意防水防潮,长期不用要拔掉电源线等
27.浓硫酸的密度大于水的密度,浓硫酸溶于水的时候放出热量;将浓硫酸沿容器壁慢慢倒入水中,并不断搅拌
.files/image043.gif) 28.红棕色变浅或消失;漏斗内的液面上升;木炭具有吸附性,使集气瓶内的压强变小
28.红棕色变浅或消失;漏斗内的液面上升;木炭具有吸附性,使集气瓶内的压强变小
29.(1)BCA (2)A,C(3)冷却热饱和溶液
30.(1)3CO+Fe2O3.files/image045.gif) 2Fe+3CO2 (2)Fe3O4 (3)B
2Fe+3CO2 (2)Fe3O4 (3)B
31.(1)Fe H2O (2)Fe+H2SO4=FeSO4+H2↑ 置换反应
32.(1)如右图所示(2)4
33.(1)①相同的酒精灯对等质量的煤油和水加热相同的时间,比较煤油和水升高的温度;
②相同的酒精灯对等质量的煤油和水加热,使它们升高相同的温度比较加热的时间;
(2)为了判断电磁铁磁性的强弱可以让电磁铁去吸引大头针,通过观察电磁铁吸引大头针的个数判断。电磁铁吸引的大头针的数量越多,说明磁性越强
34.(1)弹簧测力计的示数 有刻度部分的长度 V/.files/image029.gif) F
F.files/image029.gif) /V (2)注射器活塞的重力
/V (2)注射器活塞的重力
35.(1)电压表的量程选错;电流表的正、负接线柱接反了;滑动变阻器没有处于最大值;(2)灯丝断开或小灯泡接线柱接触不良(3)右 (4)1.14(5)灯丝的电阻随温度的变化而变化
36.(1)CO2 CaCO3+2HCl=CaCl2+H2O+CO2↑ ①③④⑤ (2)O2 铁架台、酒精灯
37.实验一(1)成立(2)反应放出的热量使锥形瓶内的气体膨胀(3)反应放出热量温度达到脱脂棉的着火点,又有氧气生成
实验二(1)质量守恒定律,化学变化前后元素的种类不变;(2)稀盐酸
38.解:设
Fe + H2SO4 FeSO4 + H2↑
56
2
则:56 : 2= x :
钢样中铁的质量分数为: ×100% = 98.6% 答:钢样中铁的质量分数为98.6%。
39.(1)解:由p=F/S可知水泥板对地压强 p=F/S=5000N/
(2)起重机提升水泥板所做的功W=Fs=Gh=5000N×
功率P=W/t=2×105J/10s=2×103 W
.files/image051.jpg) (3)η=W有/W总= Gh / F′s=G/F′n=5000N/(4000N×2)=62.5%
(3)η=W有/W总= Gh / F′s=G/F′n=5000N/(4000N×2)=62.5%
增大 在额外功不变的情况下增大了有用功
40.(1)如右图
(2)处于加热状态时电热丝电阻R1=U2/P1=(220V)2/800W=60.5Ω
处于保温状态时电路总电阻R2= U2/P2=(220V)2/40W=1210Ω
保温元件R工作时的阻值R= R2- R1=1210Ω-60.5Ω=1149.5Ω
(3)电热水瓶内水的质量为m=ρV=1×
烧开一瓶
电热水瓶的热效率为90%,则需要的电能W=Q/η=1.68×106J/ 90%=1.87×106J
需要加热的时间t= W/P=1.87×106J /800W=2333 s
本资料由《七彩教育网》www.7caiedu.cn 提供!
(1)过氧化氢中氧元素的化合价为
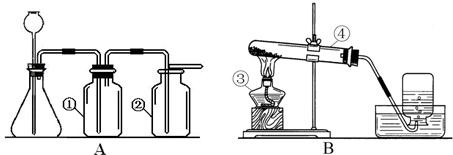
(2)过氧化氢溶液常用于实验室制取氧气.可供选择的仪器或装置如图所示.

①用过氧化氢溶液制取氧气时,氧气中会含有较多的水蒸气,为了收集干燥的氧气,整套装置的连接顺序为(由气体发生装置开始)
②加入药品通常采用“把过氧化氢溶液缓缓加入盛有少量MnO2的反应容器中”,优点是
③MnO2可以连续使用,理由是
④根据化学方程式计算获得的氧气理论值总是比实际实验操作收集到气体的数值大(假设装置不漏气且实验操作正确),原因是
(3)生产火箭燃料的工业废水中含有少量偏二甲肼X,可用双氧水处理排污,反应的化学方程式为X+8H2O2═2CO2↑+N2↑+12H2O,则X的化学式为
(4)85g过氧化氢溶液加入wg二氧化锰反应完全后,留下混合物质量仍为85g,则过氧化氢溶液中溶质的质量分数为
 |
 |
 |
 |
| A | B | C | D |
①证明其中含有水蒸气,选用
②验证并除去二氧化碳,装置的连接顺序是
(2)乙组:用上述装置(可以重复使用)组装一套完整装置,证明混合气体中含有二氧化碳、一氧化碳和水蒸气,装置连接的顺序是
(3)丙组:某气体可能是CH4,可能是CO,也可能是二者的混合物.丙组同学把该气体点燃后,依次通过
| B装置总质量 | C、D装置总质量 | |
| 反应前 | 156.6g | 356.8g |
| 反应后 | 158.4g | 359.0g |

(1)写出实验室制取二氧化碳的化学方程式
(2)自来水厂常将氯气通入水中(即氯水)消毒杀菌,已知氯气是一种密度大于空气的气体,则实验室收集氯气时应选用的装置是(填序号)
(3)按图F做细铁丝在氧气中燃烧的实验时,若事先未在瓶底装水或铺一层细沙,可能出现的后果是
(4)检验装置B气密性良好的方法是
(5)实验室用200g溶质的质量分数为8.5%过氧化氢溶液制取氧气,最多可制取多少氧气?(写出计算过程) 查看习题详情和答案>>
①称取x g胆矾晶体,研细后加入10 mL蒸馏水溶解;
②将足量的NaOH溶液与上述溶液充分反应,生成蓝色沉淀,过滤后洗涤沉淀;
③将所得沉淀转移到坩埚中,均匀缓慢加热至完全变为黑色,研细备用;
④按下表中的质量混合好固体后,在相同条件下加热,并与MnO2的催化效果做比较,实验时间均以生成50 mL气体为准(见图甲),其他可能影响实验的因素均忽略.
| 编号 | KClO3质量(g) | 其他物质质量(g) | 待测数据 |
| 1 | 2.0 | / | |
| 2 | 2.0 | CuO 0.5 | |
| 3 | 2.0 | MnO2 0.5 |
(1)步骤①中的x应至少称取
(2)表格中的“待测数据”是指
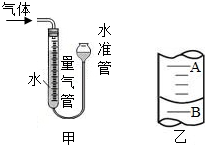
(3)为了较准确地测量气体体积,在读取反应前后量气管中液面的读数的过程中,应注意
a.视线与凹液面最低处相平b.读数前不能移动量气管和水准管
c.保持水准管静止,待水准管中液面不再上升时,立刻读数
d.读数前应上下移动水准管,待两管液面相平再读数
(4)若50mL量气管中液面的位置如图乙所示,A与B刻度间相差1 mL,刻度A为20,则此时气体的读数为
(5)如果要进一步探究CuO在反应中是否起到催化作用,请完成下列表格后续实验.(提示:可从催化剂的概念完成实验.)
| 实验步骤 | 设计这一步骤的目的 |
| 实验表明,加入CuO后产生O2的速率比未加入时快得多 | CuO能加快KClO3的分解 |
.files/image049.gif)