摘要:(4) NH3?H2O + H+ = NH4+ + H2O , (1)用实线补全元素周期表边界.标出主族符号.
网址:http://m.1010jiajiao.com/timu_id_114055[举报]
(2013?番禺区模拟)工业合成氨的反应为:N2(g)+3H2(g)?2NH3(g)△H<0某实验将3.0mol N2(g)和4.0mol H2(g)充入容积为10L的密闭容器中,在温度T1下反应.测得H2的物质的量随反应时间的变化如图所示.
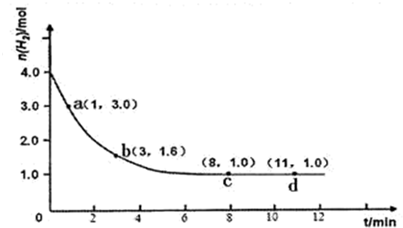
(1)反应开始3min内,H2的平均反应速率为
(2)计算该条件下合成氨反应的化学平衡常数(写出计算过程,结果保留2位有效数字)
(3)仅改变温度为T2( T2小于TI)再进行实验,请在答题卡框图中画出H2的物质的量随反应时间变化的预期结果示意图
 .
.
(4)在以煤为主要原料的合成氨工业中,原料气氢气常用下述方法获得:
①C+H2O(g)
CO+H2;②CO+H2O(g)
CO2+H2;
已知CO(g)+
O2(g)═CO2(g)△H=-283.0KJ/mol;
H2(g)+
O2(g)=H2O(g)△H=-285.8KJ/mol;
写出上述CO与H2O(g)反应的热化学方程式:
(5)合成氨工业中,原料气(N2,H2混有少量CO,NH3)在进入合成塔之前,用醋酸二氨合铜(I)溶液来吸收CO其反应为:
CH3COO[Cu(NH3)2]+CO+NH3?CH3COO[Cu(NH3)3]?CO△H<0写出提高CO吸收率的其中一项措施:
查看习题详情和答案>>

(1)反应开始3min内,H2的平均反应速率为
0.080mol/(L?min)
0.080mol/(L?min)
(2)计算该条件下合成氨反应的化学平衡常数(写出计算过程,结果保留2位有效数字)
2.0×102 (L/mol)2
2.0×102 (L/mol)2
.(3)仅改变温度为T2( T2小于TI)再进行实验,请在答题卡框图中画出H2的物质的量随反应时间变化的预期结果示意图


(4)在以煤为主要原料的合成氨工业中,原料气氢气常用下述方法获得:
①C+H2O(g)
| ||
| ||
已知CO(g)+
| 1 |
| 2 |
H2(g)+
| 1 |
| 2 |
写出上述CO与H2O(g)反应的热化学方程式:
CO(g)+H2O(g)=CO2(g)+H2(g)△H=+2.8kJ/mol
CO(g)+H2O(g)=CO2(g)+H2(g)△H=+2.8kJ/mol
(5)合成氨工业中,原料气(N2,H2混有少量CO,NH3)在进入合成塔之前,用醋酸二氨合铜(I)溶液来吸收CO其反应为:
CH3COO[Cu(NH3)2]+CO+NH3?CH3COO[Cu(NH3)3]?CO△H<0写出提高CO吸收率的其中一项措施:
增大压强、降低温度、通入氨气或分离出CH3COO[Cu(NH3)3]?CO(任写一点)
增大压强、降低温度、通入氨气或分离出CH3COO[Cu(NH3)3]?CO(任写一点)
.(1)0.5mol H2O的质量为
(2)质量都是50g的 HCl、NH3、CO2、O2四种气体中,含有分子数目最少的是
(3)在
(4)现用Zn与实验室中的盐酸反应制取4.48L H2(标准状况).如果选用所贴标签为2.0mol?L-1的盐酸,至少需该盐酸
查看习题详情和答案>>
9g
9g
,其中共含有1.5NA
1.5NA
个原子(用阿伏伽德罗常数表示).(2)质量都是50g的 HCl、NH3、CO2、O2四种气体中,含有分子数目最少的是
CO2
CO2
(填分子式,下同),在相同温度和相同压强条件下,体积最大的是NH3
NH3
.(3)在
125
125
mL 0.2mol/L NaOH溶液中含1g溶质;配制500mL 0.2mol/L CuSO4溶液,需要CuSO4?5H2O25
25
g.(4)现用Zn与实验室中的盐酸反应制取4.48L H2(标准状况).如果选用所贴标签为2.0mol?L-1的盐酸,至少需该盐酸
200
200
ml. 某实验小组拟用50mL NaOH溶液吸收CO2气体,制备Na2CO3溶液.为了防止通入的CO2气体过量生成NaHCO3,设计了如下实验步骤:
某实验小组拟用50mL NaOH溶液吸收CO2气体,制备Na2CO3溶液.为了防止通入的CO2气体过量生成NaHCO3,设计了如下实验步骤:①用25mL NaOH溶液吸收CO2气体,至CO2气体不再溶解;
②小火煮沸溶液1min~2min;
③在得到的溶液中加入另一半(25mL)NaOH溶液,使其充分混合.
此方案能制得较纯净的Na2CO3(第一步的实验装置如图所示).
(1)将块状大理石加入试管中的正确方法是
(2)写出①、③两步的化学反应程式
(3)装置B中盛放的试剂是
(4)有人认为将实验步骤②、③的顺序对调,即先混合再煮沸,更合理.你认为对吗?
(5)此实验中的装置A还可以作为下列
①NH3 ②H2 ③C2H4
(6)实验室中吸收尾气的方法很多.下列装置中可以用来吸收氨气的是(填序号,多填倒扣分)
 查看习题详情和答案>>
查看习题详情和答案>>
 的说法正确的是
的说法正确的是