摘要:
网址:http://m.1010jiajiao.com/timu_id_114051[举报]
某化学研究性学习小组在学习了《化学反应原理》后作出了如下的归纳总结,其中正确的是( )
| A、pH=1和pH=2的盐酸,c(H+)之比为1:2 | B、物质A三态间的转化如下:A(g)→A(l)→A(s),则该转化过程中△S<0 | C、pH=13的强碱溶液,加水稀释后,溶液中所有离子的浓度均变小 | D、pH=9的CH3COONa溶液和pH=9的NH3?H2O溶液,两溶液中水的电离程度相同 |
二甲醚和甲醇被称为21世纪的新型燃料,以CH4和H2O为原料制备二甲醚和甲醇的工业流程如图1:
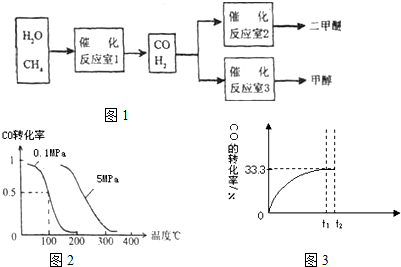
I:(1)在一定条件下,容积为 100L密闭容器中发生反应:CH4(g)+H2O(g)?CO(g)+3H2(g);△H>0
将1.0mol CH4和2.0mol H2O(g)通入该密闭容器 l0min时有0.1mol CO生成,则10min内该反应的平均速率v(H2)
(2)在压强为0.1MPa条件下,容积为V L某密闭容器中a mol CO与 2a mol H2在催化剂作用下反应生成甲醇:CO(g)+2H2(g)?CH3OH(g)平衡时CO的转化率与温度、压强的关系如图2.
①该反应的△H
②100℃时该反应的平衡常数K=
(用含a、V的代数式表示).
③在温度容积不变的情况下,向该密闭容器再增加a mol CO与 2a mol H2,达到新平衡时,CO的转化率
④在某温度下,向一个容积不变的密闭容器中通入2.5mol CO和7.5mol H2反应生成CH3OH(g),达到平衡时CO的转化率为90%,此时容器内的压强为开始时的
II:某温度下,向密闭容器中充入2.0mol CO和1.0mol H2O,发生反应:
CO(g)+H2O(g)?CO2(g)+H2(g).CO的转化率随时间变化关系如图2,回答下列问题:
(1)如果一个可逆反应的平衡常数K值很大,下列说法正确的是
A.该反应的反应物混合后很不稳定
B.该反应一旦发生将在很短的时间内完成
C.该反应达平衡时至少有一种反应物的百分含量很小
D.该反应一定是放热反应 E.该反应使用催化剂意义不大
(2)t2时刻向平衡体系中再通入1.0mol H2O(g),请在原坐标图3中将改变这一条件后CO的转化率的变化结果表示出来.
查看习题详情和答案>>

I:(1)在一定条件下,容积为 100L密闭容器中发生反应:CH4(g)+H2O(g)?CO(g)+3H2(g);△H>0
将1.0mol CH4和2.0mol H2O(g)通入该密闭容器 l0min时有0.1mol CO生成,则10min内该反应的平均速率v(H2)
0.0003mo1?L-1?min-1
0.0003mo1?L-1?min-1
.(2)在压强为0.1MPa条件下,容积为V L某密闭容器中a mol CO与 2a mol H2在催化剂作用下反应生成甲醇:CO(g)+2H2(g)?CH3OH(g)平衡时CO的转化率与温度、压强的关系如图2.
①该反应的△H
<
<
0 (填“<”、“>”或“=”).②100℃时该反应的平衡常数K=
| V2 |
| a2 |
| V2 |
| a2 |
③在温度容积不变的情况下,向该密闭容器再增加a mol CO与 2a mol H2,达到新平衡时,CO的转化率
增大
增大
(填“增大”、“减小”或“不变”).平衡常数不变
不变
(填“增大”、“减小”或“不变”)④在某温度下,向一个容积不变的密闭容器中通入2.5mol CO和7.5mol H2反应生成CH3OH(g),达到平衡时CO的转化率为90%,此时容器内的压强为开始时的
0.55
0.55
倍.II:某温度下,向密闭容器中充入2.0mol CO和1.0mol H2O,发生反应:
CO(g)+H2O(g)?CO2(g)+H2(g).CO的转化率随时间变化关系如图2,回答下列问题:
(1)如果一个可逆反应的平衡常数K值很大,下列说法正确的是
C
C
(填字母).A.该反应的反应物混合后很不稳定
B.该反应一旦发生将在很短的时间内完成
C.该反应达平衡时至少有一种反应物的百分含量很小
D.该反应一定是放热反应 E.该反应使用催化剂意义不大
(2)t2时刻向平衡体系中再通入1.0mol H2O(g),请在原坐标图3中将改变这一条件后CO的转化率的变化结果表示出来.
两种微粒含有相同的质子数和电子数,这两种微粒的关系可能是:(1)同一元素的不同原子,(2)不同元素的原子,(3)两种不同的分子(4)一种原子和一种分子,(5)一种原子和一种离子,(6)一种分子和一种离子,(7)两种不同的阳离子,(8)两种不同的阴离子,(9)一种阴离子和一种阳离子,其中正确的是( )
查看习题详情和答案>>
乙醛与银氨溶液的反应常因条件控制不当,会出现黑色浊液、长时间没有银折出、析出的银镜不均匀或发暗等现象,影响了银镜反应的效果.
某研究小组为控究乙醛发生银镜反应的最佳实验条件,进行了有关实验,相关数据如下表:
请回答下列问题:
(1)写出乙醛与银氨溶液发生银镜反应的化学方程式 .
(2)若只进行实验1和实验2,其探究目的是 .
(3)实验 (填序号)组合,可探究混合液pH对银镜反应的影响.
(4)实验4无银镜出现的原因是 .
(5)试管内壁的银镜用硝酸洗涤,可以回收硝酸银溶液.你认为选用 (填“浓硝酸”或“稀硝酸”)较好,理由是 .
查看习题详情和答案>>
某研究小组为控究乙醛发生银镜反应的最佳实验条件,进行了有关实验,相关数据如下表:
| 实验变量 实验序号 |
银氨溶液的量/mL | 乙醛的量/滴 | 水浴温度/℃ | 反应混合液的pH | 出现银镜时间/min |
| 1 | 1 | 3 | 50 | 11 | t1 |
| 2 | 1 | 3 | 65 | 11 | t2 |
| 3 | 1 | 5 | 65 | 11 | t3 |
| 4 | 1 | 5 | 65 | 4 | 无银镜 |
| 5 | 1 | 5 | 65 | 10 | t5 |
| 6 | 3 | 3 | 20 | 10 | t6 |
(1)写出乙醛与银氨溶液发生银镜反应的化学方程式
(2)若只进行实验1和实验2,其探究目的是
(3)实验
(4)实验4无银镜出现的原因是
(5)试管内壁的银镜用硝酸洗涤,可以回收硝酸银溶液.你认为选用