摘要:C.B.C.D的分子数之比为3┱2┱1 D.B的生成速率和D的消耗速率为3┱1学科网
网址:http://m.1010jiajiao.com/timu_id_113991[举报]
A、B、C、D、E五种元素分属三个短周期,且原子序数依次增大.A、C同主族.A与B、A与C、A与E、B与C可按原子个数比1:1分别形成化合物甲、乙、丙、丁,B、D同主族,可形成DB2、DB3两种分子.
回答下列问题:
(1)B在元素周期表中的位置为
(2)化合物乙的电子式为
 .
.
(3)B、E的单质及两元素之间形成的化合物中可作水消毒剂的有
(4)A2D的燃烧热△H=-a kJ/mol,写出A2D燃烧反应的热化学方程式:
(5)写出FeE2与物质丁按物质的量之比2:1的反应的离子方程式:
(6)熔融状态下,C的单质和FeE2能组成可充电电池(装置示意图如下),反应原理为:2Z+FeE2
Fe+2ZE
放电时,电池的正极反应式为
以二甲醚(CH3OCH3)、空气、氢氧化钾溶液为原料,石墨为电极可构成一种性能优良的高效燃料电池.给上述电池充电,则与a电极相连的二甲醚电池电极上的反应式为
查看习题详情和答案>>

回答下列问题:
(1)B在元素周期表中的位置为
第二周期ⅥA族
第二周期ⅥA族
.(2)化合物乙的电子式为


(3)B、E的单质及两元素之间形成的化合物中可作水消毒剂的有
O3、Cl2、ClO2等
O3、Cl2、ClO2等
(写出其中两种物质的化学式)).(4)A2D的燃烧热△H=-a kJ/mol,写出A2D燃烧反应的热化学方程式:
2H2S+3O2=2SO2(g)+2H2O(l)△H=-2akJ/mol
2H2S+3O2=2SO2(g)+2H2O(l)△H=-2akJ/mol
.(5)写出FeE2与物质丁按物质的量之比2:1的反应的离子方程式:
6Fe2++3Na2O2+6H2O=4Fe(OH)3↓+2Fe3++6Na+
6Fe2++3Na2O2+6H2O=4Fe(OH)3↓+2Fe3++6Na+
.(6)熔融状态下,C的单质和FeE2能组成可充电电池(装置示意图如下),反应原理为:2Z+FeE2
| 放电 | 充电 |
放电时,电池的正极反应式为
Fe2++2e-=Fe
Fe2++2e-=Fe
.以二甲醚(CH3OCH3)、空气、氢氧化钾溶液为原料,石墨为电极可构成一种性能优良的高效燃料电池.给上述电池充电,则与a电极相连的二甲醚电池电极上的反应式为
CH3OCH3+16OH--12e-=2CO32-+11H2O
CH3OCH3+16OH--12e-=2CO32-+11H2O
.A、B、C、D、E五种元素,它们满足以下条件.
①分别属于不同主族,且均为短周期元素;
②A、B的氢化物的沸点均比它们相邻周期、同族元素的氢化物的沸点高,且A元素的氢化物常温下为液态;
③原子半径大小顺序是A<B<C<D<E;
④C的最外层电子数等于B、D的最外层电子数之和.
(1)A元素是
(2)这五种元素的单质中,沸点最高的是
(3)A、B的氢化物分子结合H+能力较强的是
(4)C、D形成的化合物的水溶液呈
查看习题详情和答案>>
①分别属于不同主族,且均为短周期元素;
②A、B的氢化物的沸点均比它们相邻周期、同族元素的氢化物的沸点高,且A元素的氢化物常温下为液态;
③原子半径大小顺序是A<B<C<D<E;
④C的最外层电子数等于B、D的最外层电子数之和.
(1)A元素是
氧
氧
,C元素是氯
氯
,E元素是钠
钠
(填元素名称).(2)这五种元素的单质中,沸点最高的是
Mg
Mg
(填元素符号).(3)A、B的氢化物分子结合H+能力较强的是
NH3
NH3
(填化学式),用一个离子方程式加以证明:NH3+H3O+=NH4++H2O
NH3+H3O+=NH4++H2O
.(4)C、D形成的化合物的水溶液呈
酸
酸
(填“酸”、“碱”或“中”性),其原因是Mg2++2H2O?Mg(OH)2+2H+
Mg2++2H2O?Mg(OH)2+2H+
(用离子方程式表示).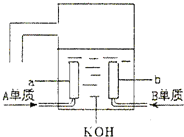 A、B、C、D是四种短周期元素,它们的原子序数依次增大,其中A与C,B与D分别是同主族元素;已知B、D二元素原子核中质子数之和是A、C二元素原子核中质子数之和的2倍;四种元素形成的单质中有两种是气体,两种是固体.请回答以下问题:
A、B、C、D是四种短周期元素,它们的原子序数依次增大,其中A与C,B与D分别是同主族元素;已知B、D二元素原子核中质子数之和是A、C二元素原子核中质子数之和的2倍;四种元素形成的单质中有两种是气体,两种是固体.请回答以下问题:(1)写出由A、B两元素形成的原子个数比为1:1的化合物的化学式
H2O2
H2O2
,此化合物能使酸性KMnO4溶液退色,体现该化合物具有还原性
还原性
性.(2)D元素在元素周期表中的位置
第三周期第ⅥA族
第三周期第ⅥA族
,B和C两元素形成的原子个数比为1:1的化合物中含有的化学键的类型为离子键、共价键
离子键、共价键
.(3)A、B、C、D四种原子半径由大到小为
Na>S>O>H
Na>S>O>H
(填元素符号);四种离子半径由大到小为S2->O2->Na+>H+
S2->O2->Na+>H+
(填离子符号).(4)写出由A、B两元素形成的原子个数比为2:1的化合物与B、C两元素形成的原子个数比为1:1的化合物反应的离子方程式
2Na2O2+2H2O=4Na++4OH-+O2↑
2Na2O2+2H2O=4Na++4OH-+O2↑
.(5)两种物质均由A、B、C、D四种元素组成,写出它们在水溶液中反应的离子方程式
HSO3-+H+=SO2↑+H2O
HSO3-+H+=SO2↑+H2O
.(6)用A元素的单质与B元素的单质可制成新型的化学电源,已在宇宙飞船中使用.其构造如图所示.两个电极均由多孔性碳制成,通入的气体由孔隙中逸出,并在电极表面放电.则a是
负
负
极,电极反应式为4H2-4e-=4H+
4H2-4e-=4H+
,b是正
正
极,电极反应式为O2+2H2O+4e-=4OH-
O2+2H2O+4e-=4OH-
.A、B、C、D是四种短周期元素,E是过渡元素.A、B、C同周期,C、D同主族,A的原子结构示意图为: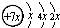 ,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题:
,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题:
(1)写出下列元素的符号:A
(2)用化学式表示上述五种元素中最高价氧化物对应水化物酸性最强的是
(3)用元素符号表示D所在周期(除稀有气体元素外)第一电离能最大的元素是
(4)D的氢化物比C的氢化物的沸点
(5)E元素原子的核电荷数是
(6)A、B、C最高价氧化物的晶体类型是分别是
(7)画出D的核外电子排布图
 ,这样排布遵循了
,这样排布遵循了
查看习题详情和答案>>
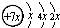 ,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题:
,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题:(1)写出下列元素的符号:A
Si
Si
BNa
Na
CP
P
DN
N
(2)用化学式表示上述五种元素中最高价氧化物对应水化物酸性最强的是
HNO3
HNO3
,碱性最强的是NaOH
NaOH
.(3)用元素符号表示D所在周期(除稀有气体元素外)第一电离能最大的元素是
F
F
,电负性最大的元素是F
F
.(4)D的氢化物比C的氢化物的沸点
高
高
(填“高“或“低“),原因氨气分子之间含有氢键
氨气分子之间含有氢键
(5)E元素原子的核电荷数是
26
26
,E元素在周期表的第四
四
周期,第Ⅷ
Ⅷ
族,已知元素周期表可按电子排布分为s区、p区等,则E元素在d
d
区.(6)A、B、C最高价氧化物的晶体类型是分别是
原子
原子
晶体、离子
离子
晶体、分子
分子
晶体(7)画出D的核外电子排布图


泡利
泡利
原理和洪特
洪特
规则.a、b、c、d、e是短周期元素,周期表中a与b、b与c相邻,c和e同主族;a与c的最外层电子数之比为2:3,b的最外层电子数比c的最外层电子数少1个;常见化合物d2c2与水反应生成c的单质,且溶液使酚酞试液变红.
(1)e的元素符号是
(2)a、b、c的氢化物稳定性顺序为(用分子式表示)
 .
.
(3)由a、c、d形成化合物的水溶液显碱性,其原因是(用离子方程式表示)
(4)一定量的d2c2与ac2反应后的固体物质,恰好与0.8mol稀盐酸溶液完全反应,并收集到0.25mol气体,则用物质的量表示该固体物质的组成为
查看习题详情和答案>>
(1)e的元素符号是
S
S
.(2)a、b、c的氢化物稳定性顺序为(用分子式表示)
H2O>NH3>SiH4
H2O>NH3>SiH4
;b的氢化物和b的最高价氧化物的水化物反应生成Z,则Z中的化学键类型为离子键、共价键
离子键、共价键
,Z的晶体类型为离子晶体
离子晶体
;d2c2的电子式为

(3)由a、c、d形成化合物的水溶液显碱性,其原因是(用离子方程式表示)
SiO32-+2H2O?H2SiO3+2OH-
SiO32-+2H2O?H2SiO3+2OH-
.(4)一定量的d2c2与ac2反应后的固体物质,恰好与0.8mol稀盐酸溶液完全反应,并收集到0.25mol气体,则用物质的量表示该固体物质的组成为
0.1molNa2CO3、0.3molNa2O2
0.1molNa2CO3、0.3molNa2O2
.