摘要:(3) 2NaCl+2H2O 2NaOH+H2↑+Cl2↑. 2Cl― -2e― = Cl2↑
网址:http://m.1010jiajiao.com/timu_id_109911[举报]
氯气是一种重要的化工原料,在生产和生活实际中应用十分广泛.
已知:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,所以在实验室可用高锰酸钾固体和浓盐酸制氯气.
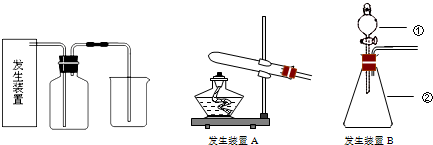
(1)请为该实验选择合适的发生装置 .(填“A”或“B”)
(2)在2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O反应中,氧化剂是 .
(3)当集气瓶中收集满氯气时,可以观察到气体呈 色.
(4)工业上常用电解饱和食盐水制取氯气,试完成该反应的化学方程式:
2NaCl+2H2O
2NaOH+ +Cl2↑
(5)写出仪器名称:① ,② .
查看习题详情和答案>>
已知:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,所以在实验室可用高锰酸钾固体和浓盐酸制氯气.

(1)请为该实验选择合适的发生装置
(2)在2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O反应中,氧化剂是
(3)当集气瓶中收集满氯气时,可以观察到气体呈
(4)工业上常用电解饱和食盐水制取氯气,试完成该反应的化学方程式:
2NaCl+2H2O
| ||
(5)写出仪器名称:①
(2010?广东)某科研小组用MnO2和浓盐酸制备Cl2时,利用刚吸收过少量SO2的NaOH溶液对其尾气进行吸收处理.
(1)请完成SO2与过量NaOH溶液反应的化学方程式:SO2+2NaOH=
(2)反应Cl2+Na2SO3+2NaOH═2NaCl+Na2SO4+H2O中的还原剂为
(3)吸收尾气一段时间后,吸收液(强碱性)中肯定存在Cl-、OH- 和SO42-.请设计实验,探究该吸收液中可能存在的其他阴离子(不考虑空气的CO2的影响).
①提出合理假设
假设1:只存在SO32-
假设2:既不存在SO32-也不存在ClO-
假设3:
②设计实验方案,进行实验.请在答题卡上写出实验步骤以及预期现象和结论.限选实验试剂:3moL/LH2SO4、1moL/LNaOH、0.01mol/LKMnO4、淀粉-KI溶液、紫色石蕊试液
查看习题详情和答案>>
(1)请完成SO2与过量NaOH溶液反应的化学方程式:SO2+2NaOH=
Na2SO3+H2O
Na2SO3+H2O
(2)反应Cl2+Na2SO3+2NaOH═2NaCl+Na2SO4+H2O中的还原剂为
Na2SO3
Na2SO3
(3)吸收尾气一段时间后,吸收液(强碱性)中肯定存在Cl-、OH- 和SO42-.请设计实验,探究该吸收液中可能存在的其他阴离子(不考虑空气的CO2的影响).
①提出合理假设
假设1:只存在SO32-
假设2:既不存在SO32-也不存在ClO-
假设3:
只存在ClO-
只存在ClO-
②设计实验方案,进行实验.请在答题卡上写出实验步骤以及预期现象和结论.限选实验试剂:3moL/LH2SO4、1moL/LNaOH、0.01mol/LKMnO4、淀粉-KI溶液、紫色石蕊试液
| 实验步骤 | 预期现象和结论 |
| 步骤1:取少量吸收液于试管中,滴加3moL/LH2SO4至溶液呈酸性,然后将所得溶液分置于A、B试管中 | / |
| 步骤2: 在A试管中滴加紫色石蕊试液 在A试管中滴加紫色石蕊试液 |
若先变红后退色,证明有ClO-,否则无 若先变红后退色,证明有ClO-,否则无 |
| 步骤3: 在B试管中滴加0.01mol?L-1KMnO4溶液 在B试管中滴加0.01mol?L-1KMnO4溶液 |
若紫红色退去,证明有SO32-,否则无 若紫红色退去,证明有SO32-,否则无 |
如图A为直流电源,B为浸透饱和氯化钠溶液和酚酞试液的滤纸,C为电镀槽,接通电路后,发现B上的c点显红色,请填空:
(1)电源A上的a为
(2)滤纸B上发生的总化学方程式为:
(3)欲在电镀槽中实现铁上镀锌,接通K点,使c、d两点短路,则电极e上发生的反应为:

查看习题详情和答案>>
(1)电源A上的a为
正极
正极
极;(2)滤纸B上发生的总化学方程式为:
2NaCl+2H2O
2NaOH+Cl2↑+H2↑
| ||
2NaCl+2H2O
2NaOH+Cl2↑+H2↑
;
| ||
(3)欲在电镀槽中实现铁上镀锌,接通K点,使c、d两点短路,则电极e上发生的反应为:
Zn-2e-=Zn2+
Zn-2e-=Zn2+
,电极f上发生的反应为:Zn2++2e-=Zn;
Zn2++2e-=Zn;
,槽中盛放的电镀液可以是ZnSO4
ZnSO4
或Zn(NO3)2
Zn(NO3)2
(只要求填两种电解质溶液).
 (2011?宁波模拟)“化学与技术”模块
(2011?宁波模拟)“化学与技术”模块海洋是一座巨大的宝藏,若把海水淡化和化工生产结合起来,既可解决淡水资源缺乏的问题,又可充分利用海洋资源.而以海水为主要原料的海洋化学工业,又被称为“蓝色化工”.
(1)常用的海水淡化方法有
蒸馏
蒸馏
法、膜
膜
法(电渗析、反渗透)、冷冻法、离子交换法等.(2)如图是电渗析法淡化海水的原理图.其中,电极A接直流电源的正极,电极B接直流电源的负极.
①隔膜A是
阴离子交换膜
阴离子交换膜
(填:阴离子交换膜或阳离子交换膜)②从宁波港采集的海水样品,经分析含有大量的Na+、Cl-,以及少量的K+、SO42-.
若用上述装置对采自宁波港的海水进行淡化,当淡化工作完成后,A、B、C三室中所得溶液(或液体)的pH分别为pHa、pHb、
pHc,则其大小顺序为
pHa<pHb<pHc
pHa<pHb<pHc
.③请写出用电渗析法对采自宁波港的海水进行淡化处理时所发生的化学反应方程式
2NaCl+2H2O
2NaOH+H2↑+Cl2↑
| ||
2NaCl+2H2O
2NaOH+H2↑+Cl2↑
.
| ||
(3)具有暂时硬度的硬水在长时间加热煮沸后,生成沉淀的主要成分是
CaCO3、Mg(OH)2
CaCO3、Mg(OH)2
.(4)为获得纯净水(去离子水),某同学在实验室将含Mg2+、Ca2+、Cl-的硬水先后通过阴离子交换树脂[如RN(CH3)3OH]和阳离子交换树脂[如RSO3H],写出Cl-与上述离子交换反应的方程式
RN(CH3)3OH+Cl-═RN(CH3)3Cl+OH∴-
RN(CH3)3OH+Cl-═RN(CH3)3Cl+OH∴-
;结果实验未获得成功,其可能原因是阴离子交换树脂交换出的OH-和Mg2+、Ca2+等反应生成沉淀堵塞了离子交换柱
阴离子交换树脂交换出的OH-和Mg2+、Ca2+等反应生成沉淀堵塞了离子交换柱
.