摘要:(3)第三份加足量BaCl2溶液后.得干燥沉淀6.27 g.经足量盐酸洗涤.干燥后.沉淀质量为2.33 g.根据上述实验.以下推测正确的是
网址:http://m.1010jiajiao.com/timu_id_109577[举报]
一.选择题(48分)
1
2
3
4
5
6
7
8
9
10
11
12
B
A
A
D
C
D
A
D
B
A
B
B
13
14
15
16
17
18
19
20
21
22
23
24
D
C
B
B
A
D
A
C
B
B
B
A
25.(7分)略
26.(14分,每个方程式2分)
(1)Ar K (2 )KOH (3)Cl― Al3+
(4)H2O 2K+H2O==2KOH+H2↑
(5)黄 Cl2+2NaBr==2NaCl+Br2
点燃
(6)2Mg+CO2====2MgO+C
(7)Al2O3+2OH―====2AlO2―+H2O
27.(4分)x-8 x+18 x-18 x+8
28.(5分)250mL的容量瓶、烧杯内壁、容量瓶、胶头滴管、相切(各1分)
29.(10分,其中(3)4分,(4)2分,其余每空1分)
(1)乙 亚铁盐在空气中易被氧气氧化 (2) 还原
(3) 2Fe2++H2O2+2H+=2Fe3++2H2O Fe3++3SCN-=Fe(SCN)3 。
(4)再加过量KSCN,如果变血红色,则第二种合理;如果不变色,则第一种合理
(5) 未能测其成分。
三.计算题(12分)
30.(4分)(1)12 (2)27
31.(8分)(1)2min 末B的浓度为0.7mol?L-1 ,C的浓度为0.6mol?L-1 。
(2) 
 每个计算结果2分,本题共8分。
每个计算结果2分,本题共8分。
(1)第一份加入AgNO3溶液有沉淀产生
(2)第二份加足量NaOH溶液加热后,收集到气体0.04mol
(3)第三份加足量BaCl2溶液后,得干燥沉淀6.27g,经足量盐酸洗涤、干燥后,沉淀质量为2.33g。根据上述实验,以下推测正确的是: ( )
①K+一定存在;②100mL溶液中含0.01mol CO32-;③ Cl-可能存在;
④Ba2+一定不存在;⑤Mg2+可能存在
A.①② B. ③④⑤ C.①③④ D①⑤
有一未知的无色溶液,只可能含有以下离子中的若干种(忽略由水电离产生的H+、OH-):H+、NH4+、K+、Mg2+、Cu2+、
Al3+,NO3-、CO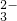 、SO
、SO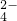 ,现取三份100mL溶液进行如下实验:
,现取三份100mL溶液进行如下实验:
①第一份加足量AgNO3溶液后,有白色沉淀产生.
②第二份加足里BaCl2 溶液后,有白色沉淀产生,经洗涤、干燥后,沉淀质量为6.99g.
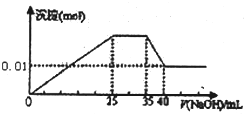
③第三份逐滴滴加NaOH 溶液,测得沉淀与NaOH溶液的体积关系如图.根据上述实验.回答以下问题

(1)原溶液确定含有Mg2+、Al3+、NH +,其物质的量之比n(Mg2+):n(Al3+):n(NH
+,其物质的量之比n(Mg2+):n(Al3+):n(NH +)=______.
+)=______.
(2)实验所加的NaOH 物质的量浓度.c(Na0H )=______mol?L-1
(3)原溶液中NO -的物质的量为n (NO3-),则n(NO3-)的取值范围为:______.
-的物质的量为n (NO3-),则n(NO3-)的取值范围为:______.
查看习题详情和答案>>
某无色水溶液可能含有以下离子中的若干种:NH4+、Cl-、Fe2+、Ba2+、K+、CO32-、SO42-,现取三份100mL 的该溶液进行如下实验:①第一份加入AgNO3溶液有沉淀产生;②第二份加足量NaOH溶液加热后,收集到气体0.04mol; ③第三份加足量BaCl2溶液后,得干燥沉淀6.27g,用足量盐酸洗涤、干燥后,剩余沉淀质量为2.33g.根据上述实验结果推测以下说法不正确的是( )
| A、Cl-可能存在 | B、Ba2+一定不存在 | C、K+一定存在 | D、溶液中CO32-浓度为0.1 mol/L |
今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、NH4+、Cl-、Mg2+、Ba2+、CO32-、SO42-,现取三份100mL溶液进行如下实验:
①第一份加入AgNO3溶液有沉淀产生
②第二份加足量NaOH溶液加热后,收集到气体0.04mol
③第三份加足量BaCl2溶液后,得干燥沉淀6.27g,经足量盐酸洗涤、干燥后,沉淀质量为2.33g.
试回答下列问题
(1)由实验②可知溶液中含有的离子为
(2)由实验③可以判断中溶液中含有的离子为
(3)由上述实验信息判断下列说法中正确的是
A.K+一定存在 B.100mL溶液中含0.01mol CO32-
C.Cl-可能存在 D.Ba2+一定不存在,Mg2+可能存在.
查看习题详情和答案>>
①第一份加入AgNO3溶液有沉淀产生
②第二份加足量NaOH溶液加热后,收集到气体0.04mol
③第三份加足量BaCl2溶液后,得干燥沉淀6.27g,经足量盐酸洗涤、干燥后,沉淀质量为2.33g.
试回答下列问题
(1)由实验②可知溶液中含有的离子为
NH4+
NH4+
,在100mL溶液中该离子的物质的量浓度为0.4mol/L
0.4mol/L
(2)由实验③可以判断中溶液中含有的离子为
CO32-,SO42-
CO32-,SO42-
(3)由上述实验信息判断下列说法中正确的是
AC
AC
A.K+一定存在 B.100mL溶液中含0.01mol CO32-
C.Cl-可能存在 D.Ba2+一定不存在,Mg2+可能存在.
 有一未知的无色溶液,只可能含有以下离子中的若干种:H+、NH+4、K+、Mg2+、Cu2+、Al3+、NO-3、CO2-3、SO2-4,现取三份100mL溶液进行如下实验
有一未知的无色溶液,只可能含有以下离子中的若干种:H+、NH+4、K+、Mg2+、Cu2+、Al3+、NO-3、CO2-3、SO2-4,现取三份100mL溶液进行如下实验①第一份加足量AgNO3溶液后,有白色沉淀产生.
②第二份加足量BaCl2溶液后,有白色沉淀产生,经洗涤、干燥后,沉淀质量为6.99g.
③第三份逐滴滴加NaOH溶液,测得沉淀与NaOH溶液的体积关系如图.
根据上述实验,以下推测不正确的是( )
| A、原溶液一定不存在H+、Cu2+、CO2-3 | B、不能确定原溶液是否含有K+、NO-3 | C、原溶液确定含Mg2+、Al3+、NH+4,且n(Mg2+):n(Al3+):n(NH+4)=1:1:2 | D、实验所加的NaOH的浓度为2 mol?L-1 |