网址:http://m.1010jiajiao.com/timu_id_109190[举报]
一 二、选择题
题号
1
2
3
4
5
6
7
8
答案
B
A
D
B
B
A
D
D
题号
9
10
11
12
13
14
答案
D
BD
CD
C
AD
AC
15.(1)防止暴沸 冷凝回流
(2)3.2
(3)温度过高发生副反应。
(4)除去产物中的丁醇。(每空2分)
16.(1)SO2
(1分) 
 (1分) (2)第四周期第Ⅷ族(2分)
(1分) (2)第四周期第Ⅷ族(2分)
(3)2Al+Fe2O3 Al2O3+2Fe (2分) 0.1 mol (1分)
Al2O3+2Fe (2分) 0.1 mol (1分)
(4) ③(1分)
(5) 3Fe2++NO3- +4H+ = 3Fe3++NO↑+2H2O(2分)
(6) Fe2O3+3KNO3+4KOH  2K2FeO4+3KNO2+2H2O(2分)
2K2FeO4+3KNO2+2H2O(2分)
17.(共8分)
(1)0.075mol/L?min(1分)
(2)放热, CO(g)+2H2(g) → CH3OH(g) +91KJ, 不能(各1分,共3分)
(3)K = ,减小;(各1分,共2分) (4)c(2分)
18.
(1)反应速率突然减小(或铁片表面生成的气泡突然减少)(2分)
(2)过滤(1分)
(3)b、d(2分),Fe和Cu(1分)
(4)抑制Fe2+、NH4+水解(2分)
(5)避免加热过程中晶体受热分解(或被氧化)(2分)
19.(每空2分)
(1) 氧化还原反应 (2)
氧化还原反应 (2)
(3)C10H12O4
(4)
20.(每空2分,共10分)
(1)2.8×105 ;18
(2)86.96%
(3) ;138
;138
21.A(1)●:AlF6- ○:Na+ AlF6- 电解炼铝的助熔剂(各1分)
(2).H2O2分子间存在氢键(1分),与水分子可形成氢键(1分)。
(3)3d104s1(1分) Cr(1分) 共价键、配位键(2分)
降低Cu(NH3)4SO4?H2O的溶解度(2分)
B.(1) Fe + 2H+ → Fe2+ + H2↑;CuO + 2H+ → Cu2+ + H2O (各2分)
(2) ① (1分)
(3) ③ (1分)
(4) ①③ (2分)
(5) ②④① (2分)
(6)二; (1+3分)
(1+3分)
(14分)在实验室里可用右图所示装置制取氯酸钾、次氯酸钠和探究氯水的性质。
图中:①为氯气发生装置;②的试管里盛有15 mL 30% KOH溶液,并置于热 水浴中;③的试管里盛有15 mL 8% NaOH溶液,并置于冰水浴中;④的试管里加有紫色石蕊试液;⑤为尾气吸收装置。
水浴中;③的试管里盛有15 mL 8% NaOH溶液,并置于冰水浴中;④的试管里加有紫色石蕊试液;⑤为尾气吸收装置。
请填写下列空白:
⑴ 制取氯气时,在烧瓶里加入一定量的二氧化锰,通过________(填写仪器名称)向烧瓶中加入适量的浓盐酸。实验室制Cl2的化学方程式 ;实验时为了除去氯气中的HCl气体,可在①与②之间安装盛有_______(填写下列编号字母)的净化装置。
| A.碱石灰 | B.氢氧化钠溶液 | C.饱和食盐水 | D.浓硫酸 |
 06 mol。
06 mol。 其主要原因有:①_______________________________________________,
其主要原因有:①_______________________________________________,②__________________________________________________________________________。
⑶比较制取氯酸钾和次氯酸钠的条件,二者的差异是
① ;
② 。
反应完毕经冷却后,②的试管中有大量晶体析出。右图中符合该晶体溶解度曲线的是_______(填写编号字母);

从②的试管中分离出该晶体的方法是__________(填
 写实验操作名称)。
写实验操作名称)。⑷实验中可观察到④的试管里溶液的颜色发生了如下变化,请填写下表中的空白。
实验 现象 现象 | 原因 |
| 溶液最初从紫色逐渐变为_______色 | 氯气与水反应 生成的H+使石蕊变色 生成的H+使石蕊变色 |
| 随后溶液逐渐变为无色 | ____________________________ __________ __________ |
| 然后溶液从无色逐渐变为_______色 | ______________________ ________________ ________________ |
在实验室里可用右图所示装置制取氯酸钾、次氯酸钠和探究氯水的性质。 
图中:①为氯气发生装置;②的试管里盛有15 mL 30% KOH溶液,并置于热水浴中;③的试管里盛有15 mL 8% NaOH溶液,并置于冰水浴中;④的试管里加有紫色石蕊试液;⑤为尾气吸收装置。
请填写下列空白:
⑴制取氯气时,在烧瓶里加入一定量的二氧化锰,通过________(填写仪器名称)向烧瓶中加入适量的浓盐酸。实验室制Cl2的化学方程式 ;实验时为了除去氯气中的HCl气体,可在①与②之间安装盛有_______(填写下列编号字母)的净化装置。
| A.碱石灰 | B.氢氧化钠溶液 | C.饱和食盐水 | D.浓硫酸 |
①______________________________________ _________,
②__________________________________________________________________________。
⑶ 比较制取氯酸钾和次氯酸钠的条件,二者的差异是
① ;
② 。
(4)反应完毕经冷却后,②的试管中有大量晶体析出。
①下图中符合该晶体溶解度曲线的是_______(填写编号字母);
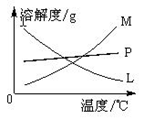
②从②的试管中分离出该晶体的方法是__________(填写实验操作名称)。
⑷ 实验中可观察到④的试管里溶液的颜色发生了如下变化,请填写下表中的空白。
| 实验现象 | 原因 |
| 溶液最初从紫色逐渐变为_______色 | 氯气与水反应生成的H+使石蕊变色 |
| 随后溶液逐渐变为无色 | ______________________________________ |
| 然后溶液从无色逐渐变为_______色 | ______________________________________ |
在实验室里可用右图所示装置制取氯酸钾、次氯酸钠和探究氯水的性质。

图中:①为氯气发生装置;②的试管里盛有15 mL 30% KOH溶液,并置于热水浴中;③的试管里盛有15 mL 8% NaOH溶液,并置于冰水浴中;④的试管里加有紫色石蕊试液;⑤为尾气吸收装置。
请填写下列空白:
⑴制取氯气时,在烧瓶里加入一定量的二氧化锰,通过________(填写仪器名称)向烧瓶中加入适量的浓盐酸。实验室制Cl2的化学方程式 ;实验时为了除去氯气中的HCl气体,可在①与②之间安装盛有_______(填写下列编号字母)的净化装置。
A.碱石灰 B.氢氧化钠溶液 C.饱和食盐水 D.浓硫酸
⑵ 如果将过量二氧化锰与20 mL 12 mol·L-1的浓盐酸混合加热,充分反应后生成的氯气明显少于0. 06 mol。其主要原因有:
①______________________________________ _________,
②__________________________________________________________________________。
⑶ 比较制取氯酸钾和次氯酸钠的条件,二者的差异是
① ;
② 。
(4)反应完毕经冷却后,②的试管中有大量晶体析出。
①下图中符合该晶体溶解度曲线的是_______(填写编号字母);

②从②的试管中分离出该晶体的方法是__________(填写实验操作名称)。
⑷ 实验中可观察到④的试管里溶液的颜色发生了如下变化,请填写下表中的空白。
|
实验现象 |
原因 |
|
溶液最初从紫色逐渐变为_______色 |
氯气与水反应生成的H+使石蕊变色 |
|
随后溶液逐渐变为无色 |
______________________________________ |
|
然后溶液从无色逐渐变为_______色 |
______________________________________ |
查看习题详情和答案>>
(12分)在实验室里可用右图所示装置制取氯酸钾、次氯酸钠和探究氯水的性质。
图中:①为氯气发生装置;②的试管里盛有15 mL 30% KOH溶液,并置于水浴中;③的试管里盛有15 mL 8% NaOH溶液,并置于冰水浴中;④的试管里加有紫色石蕊试液;⑤为尾气吸收装置。请填写下列空白: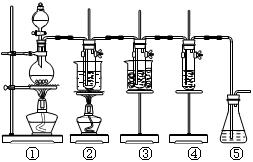
(1)装置①是氯气发生装置,蒸馏烧瓶中盛放MnO2固体,其反应的化学方程式为 ▲ 。
(2)如果实验室中MnO2用完了,则下列物质可能可以用来代替MnO2制Cl2的是: ▲ 。
| A.NaBiO3 | B.FeCl3 | C.PbO2 | D.Na2O2 |
 (3)比较制取氯酸钾和次氯酸钠的条件,二者的差异是
(3)比较制取氯酸钾和次氯酸钠的条件,二者的差异是① ▲ ; ② ▲ 。
(4)反应完毕经冷却后,②的试管中有大量晶体析出。右图中符合该晶体溶解度曲线的是 ▲ (填写编号字母);从②的试管中分离出该晶体的方法是 ▲ (填写实验操作名称)。
(5)根据④的试管里紫色石蕊试液的颜色变化可否证明氯气的强氧化性 ▲ 。
为什么? ▲ 。
(6)若②的试管溶液中不但有KClO3生成还有KClO生成,且二者的物质的量之比为1∶2,则该反应中氧化剂和还原剂的物质的量之比为: ▲ 。 查看习题详情和答案>>
A.可以由下列反应合成三聚氰胺:
CaO+3C
| ||
| ||
(1)写出与Ca在同一周期且最外层电子数相同、内层排满电子的基态原子的电子排布式:
(2)尿素分子中C原子采取


A.2个σ键 B.2个π键 C.1个σ键、1个π键
(3)三聚氰胺(
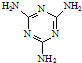 )俗称“蛋白精”.动物摄入三聚氰胺和三聚氰酸(
)俗称“蛋白精”.动物摄入三聚氰胺和三聚氰酸( 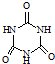 )后,三聚氰酸与三聚氰胺分子相互之间通过
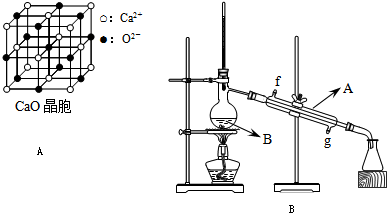
)后,三聚氰酸与三聚氰胺分子相互之间通过(4)CaO晶胞如图A所示,CaO晶体中Ca2+的配位数为
B.实验室用乙酸和正丁醇制备乙酸正丁酯.有关物质的物理性质如下表.请回答有关问题.
| 化合物 | 密度/g?cm-3 | 沸点/℃ | 溶解度/100g水 |
| 正丁醇 | 0.810 | 118.0 | 9 |
| 冰醋酸 | 1.049 | 118.1 | ∞ |
| 乙酸正丁酯 | 0.882 | 126.1 | 0.7 |
在干燥的50mL圆底烧瓶中,装入沸石,加入11.5mL正丁醇和9.4mL冰醋酸,再加3~4滴浓硫酸.然后安装分水器(作用:实验过程中不断分离除去反应生成的水)、温度计及回流冷凝管,加热冷凝回流反应.
(1)本实验过程中可能产生多种有机副产物,写出其中两种的结构简式:
(2)实验中为了提高乙酸正丁酯的产率,采取的措施是:
Ⅱ.乙酸正丁酯粗产品的制备
(1)将乙酸正丁酯粗产品用如下的操作进行精制:①水洗 ②蒸馏 ③用无水MgSO4干燥 ④用10%碳酸钠洗涤,正确的操作步骤是
A.①②③④B.③①④②C.①④①③②D.④①③②③
(2)将酯层采用如图B所示装置蒸馏.
1.出图中仪器A的名称
2.②蒸馏收集乙酸正丁酯产品时,应将温度控制在
Ⅲ.计算产率
测量分水器内由乙酸与正丁醇反应生成的水体积为1.8mL,假设在制取乙酸正丁酯过程中反应物和生成物没有损失,且忽略副反应,计算乙酸正丁酯的产率