0 36886 36894 36900 36904 36910 36912 36916 36922 36924 36930 36936 36940 36942 36946 36952 36954 36960 36964 36966 36970 36972 36976 36978 36980 36981 36982 36984 36985 36986 36988 36990 36994 36996 37000 37002 37006 37012 37014 37020 37024 37026 37030 37036 37042 37044 37050 37054 37056 37062 37066 37072 37080 447348
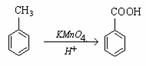
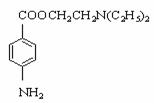 (11分)普鲁卡因为白色、细微的针状晶体,易溶于水;其针剂常用于临床局部麻醉剂。普鲁卡因的结构简式为:
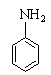
(11分)普鲁卡因为白色、细微的针状晶体,易溶于水;其针剂常用于临床局部麻醉剂。普鲁卡因的结构简式为: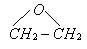 )通到二乙胺
)通到二乙胺 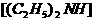 的醇溶液中可制备二乙胺基乙醇
的醇溶液中可制备二乙胺基乙醇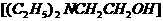
 )
)
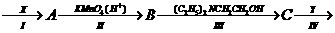 普鲁卡因
普鲁卡因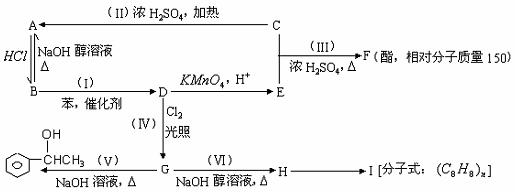
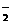 、O
、O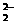 甚至O
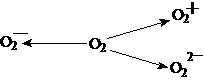
甚至O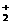 的化合物是可能存在的,通常它们是在氧分子进行下列各种反应时生成的:
的化合物是可能存在的,通常它们是在氧分子进行下列各种反应时生成的:
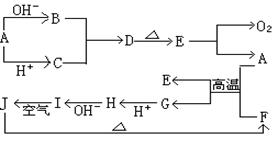
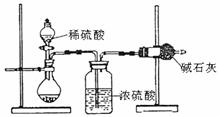 Ⅰ.甲同学的方案如右图所示:
Ⅰ.甲同学的方案如右图所示: