摘要:现有含H2SO4的质量分数为98%.密度为1.84g/mL的浓硫酸.要配制490mL密度为1.2g/mL溶质质量分数为20%的硫酸溶液.需用浓硫酸和水各多少毫升?
网址:http://m.1010jiajiao.com/timu3_id_99474[举报]
木炭粉还原氧化铜实验后的混合粉末中含有铜、氧化铜、少量木炭粉,实验室从该混合粉末中回收铜的方案(图1)如下:

(1)反应①所用的硫酸的质量分数为24.5%.现要配制40g 24.5%的硫酸,需
(2)在进行“反应①”、“反应②”、“反应③”的操作时,可将反应物加入
(3)试剂A可选用
(4)为了从混合粉末中回收更多的铜,可对实验方案进行修改和完善,你的建议是(提出一条即可)
查看习题详情和答案>>

(1)反应①所用的硫酸的质量分数为24.5%.现要配制40g 24.5%的硫酸,需
10
10
g98%的硫酸和30
30
g水.实际操作时,用lOmL量筒取98%的硫酸(密度为1.84g/cm3),请在答题卡图2中画出所取硫酸的液面.(2)在进行“反应①”、“反应②”、“反应③”的操作时,可将反应物加入
烧杯
烧杯
中(填仪器名称),然后用玻璃棒不断搅拌
用玻璃棒不断搅拌
(填操作名称),使反应充分进行.(3)试剂A可选用
H2SO4(合理均可)
H2SO4(合理均可)
溶液(填一种物质的化学式).(4)为了从混合粉末中回收更多的铜,可对实验方案进行修改和完善,你的建议是(提出一条即可)
回收滤渣I中的Cu(或将滤渣I在空气中充分灼烧,再投入反应①中)
回收滤渣I中的Cu(或将滤渣I在空气中充分灼烧,再投入反应①中)
.(2012?广州)木炭粉还原氧化铜实验后的混合粉末中含有铜、氧化铜、少量木炭粉,实验室从该混合粉末中回收铜的方案如下图1:
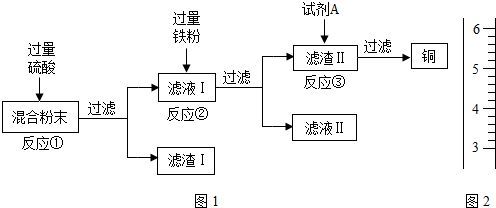
(1)写出下列反应的化学方程式:
反应①:
反应②:
(2)反应①所用的硫酸的质量分数为24.5%.现要配制40g 24.5%的硫酸,需
(3)在进行“反应①”、“反应②”、“反应③”的操作时,可将反应物加入
(4)试剂A可选用
(5)为了从混合粉末中回收更多的铜,可对实验方案进行修改和完善,你的建议是(提出一条即可)
查看习题详情和答案>>

(1)写出下列反应的化学方程式:
反应①:
H2SO4+CuO═CuSO4+H2O
H2SO4+CuO═CuSO4+H2O
;反应②:
Fe+CuSO4═FeSO4+Cu
Fe+CuSO4═FeSO4+Cu
.(2)反应①所用的硫酸的质量分数为24.5%.现要配制40g 24.5%的硫酸,需
10
10
g 98%的硫酸和30
30
g水.实际操作时,用lOmL量筒取98%的硫酸(密度为1.84g/cm3),请在图2中画出所取硫酸的液面.(3)在进行“反应①”、“反应②”、“反应③”的操作时,可将反应物加入
烧杯
烧杯
中(填仪器名称),然后搅拌
搅拌
(填操作名称),使反应充分进行.(4)试剂A可选用
H2SO4
H2SO4
溶液(填一种物质的化学式).(5)为了从混合粉末中回收更多的铜,可对实验方案进行修改和完善,你的建议是(提出一条即可)
回收滤渣I中的Cu
回收滤渣I中的Cu
. 现有一瓶未开启的浓硫酸,试剂瓶标签上的部分内容如图所示.请根据有关信息回答并计算:
现有一瓶未开启的浓硫酸,试剂瓶标签上的部分内容如图所示.请根据有关信息回答并计算:| 硫酸(500mL) 品 名 硫酸 化学式 H2SO4 相对分子质量98 密 度 1.84g/cm3 质量分数98% (1)硫酸由 氢 氢 元素、硫 硫 元素、氧 氧 元素组成,它含氧元素,它不是 不是 (是、不是)氧化物;磷酸相对分子质量为98 98 ;你认为硫酸与磷酸含氧元素质量相等的条件是硫酸和磷酸的质量相等 硫酸和磷酸的质量相等 ;(2)该试剂瓶中硫酸溶液的质量是 920 920 g.(3)工会主席王赐用20g该浓硫酸配制20%的稀硫酸,以清洗钢铁表面的铁锈.他在配制该溶液时所用98%的浓硫酸与水的质量比应该为 10:39 10:39 .(4)某固体物质由氯化钠和氯化钡组成,取32.8g该固体混合物完全溶于水,并逐滴加入上述20%的稀硫酸,产生沉淀的质量与加入稀硫酸的质量有如图所示关系,计算32.8g固体混合物中氯化钠和氯化钡的质量. (5)若加入的稀硫酸刚好使沉淀达最大量时,将所得混合物过滤、洗涤,得滤液并将其稀释至200g(过程中损耗忽略不计),计算该滤液中溶质的质量分数为 氯化钠的质量分数为6%,氯化氢的质量分数为3.65% 氯化钠的质量分数为6%,氯化氢的质量分数为3.65% .(若溶液中含有多种溶质,则每种溶质的质量分数为该溶质的质量与溶液总质量之比)[注:(3)、(4)两问需写出计算过程].(6)喜欢探究又善于思考的周泽坤出这样题目考大家:把30g含Fe、Al、Mg、Zn的金属粉末投入适量的稀硫酸中全部溶解完,再将溶液蒸干得无水干燥固体126g,则同时产生的氢气质量为 2 2 g;探究中泽坤发现:用相同浓度的硫酸,与一瓶未变质、部分变质、全变质(杂质都是氢氧化钙)的生石灰样品反应,需要的硫酸质量都相等,其原因是氧化钙和碳酸钙都是每40g钙元素生成136g硫酸钙,消耗98g硫酸 氧化钙和碳酸钙都是每40g钙元素生成136g硫酸钙,消耗98g硫酸 .
查看习题详情和答案>>
酸、碱、盐是有广泛用途的重要化合物.某化学活动小组的同学围绕这几类化合物进行了一系列的探究活动.
(1)同学们打开盛浓盐酸和浓硫酸试剂瓶的瓶盖,立即就能把它们区分开来,这是为什么? (2)右图是某试剂瓶标签上的内容.要把10g这种浓硫酸稀释为20%的硫酸,需要水的质量为______g.稀释浓硫酸时,不可将水倒进浓硫酸里,请解释其原因.______
①取少量该固体样品置于试管中,向其中加入一种无色溶液,发现有气泡产生,说明该样品中含有碳酸钠,由此可确定该固体已发生变质.则无色溶液可能是______. ②为探究该固体中是否还有未变质的氢氧化钠,同学们又进行了如下表所示的实验.已知碳酸钠的水溶液呈碱性,它的存在会对氢氧化钠的检验造成干扰.
查看习题详情和答案>>
(2009?河南)酸、碱、盐是有广泛用途的重要化合物.某化学活动小组的同学围绕这几类化合物进行了一系列的探究活动.
(1)同学们打开盛浓盐酸和浓硫酸试剂瓶的瓶盖,立即就能把它们区分开来,这是为什么? (2)右图是某试剂瓶标签上的内容.要把10g这种浓硫酸稀释为20%的硫酸,需要水的质量为______g.稀释浓硫酸时,不可将水倒进浓硫酸里,请解释其原因.______
①取少量该固体样品置于试管中,向其中加入一种无色溶液,发现有气泡产生,说明该样品中含有碳酸钠,由此可确定该固体已发生变质.则无色溶液可能是______. ②为探究该固体中是否还有未变质的氢氧化钠,同学们又进行了如下表所示的实验.已知碳酸钠的水溶液呈碱性,它的存在会对氢氧化钠的检验造成干扰.
查看习题详情和答案>> |