摘要: 现有含杂质的氧化铜样品.为了测定该样品中氧化铜的质量分数.某同学称取12.5g样品.并用如图所示的装置进行实验.得到如下两组数据: (1)实验中可以观察到的现象是 . (2)有关的化学方程式为 . (3)假设样品完全反应.应选择 组数据计算.样品中氧化铜的质量分数是 . (4)该同学所用实验装置的不足之处是 .
网址:http://m.1010jiajiao.com/timu3_id_93289[举报]
现有含杂质的氧化铜样品,为测定该样品中氧化铜的质量分数,某同学称取一定质量的这样品,用下图装置进行实验,得到如下数据(假设样品中的杂质不参加反应).请回答:
| 反应前 | 氧化铜被完全还原后 | 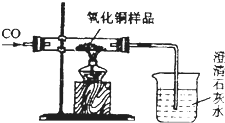 | |
| A组 | 玻璃管和氧化铜样品质量为m1g | 玻璃管和固体物质的质量为m2g | |
| B组 | 烧杯和澄清石灰水的质量为m3g | 烧杯和烧杯中物质的质量为m1g |
(2)澄清石灰水出现白色浑浊,此现象说明________.
(3)写出CO与CuO发生化学反应的化学方程式________.
(4)计算样品中氧化铜的质量分数应选择组数据________.
(5)从安全环保的角度看,这位同学所用实验装置的不足之处是________. 查看习题详情和答案>>
现有含杂质的氧化铜样品(杂质不参加反应),为了测定该样品中氧化铜的质量分数,某同学称取12.5g样品,并用如图所示的装置进行实验,得到如下两组数据:
(1)实验中可以观察到的现象是______.
(2)有关的化学方程式为______ Cu+CO2,CO2+Ca(OH)2=CaCO3↓+H2O
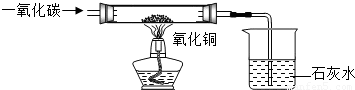 查看习题详情和答案>>
查看习题详情和答案>>
| 反应前 | 氧化铜完全反应后 | |
| 第一组 | 烧杯和澄清石灰水的总质量180.0g | 烧杯和烧杯内物质的总质量184.3g |
| 第二组 | 玻璃管和氧化铜样品的总质量是44.5g | 玻璃管和管内物质的总质量是42.9g |
(2)有关的化学方程式为______ Cu+CO2,CO2+Ca(OH)2=CaCO3↓+H2O
 查看习题详情和答案>>
查看习题详情和答案>>
现有含杂质的氧化铜样品(杂质不参加反应),为了测定该样品中氧化铜的质量分数,某同学称取12.5g样品,并用如图所示的装置进行实验,得到如下两组数据:
(1)实验中可以观察到的现象是______.
(2)有关的化学方程式为______ Cu+CO2,CO2+Ca(OH)2=CaCO3↓+H2O
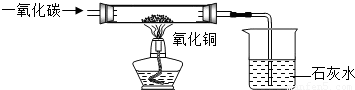 查看习题详情和答案>>
查看习题详情和答案>>
| 反应前 | 氧化铜完全反应后 | |
| 第一组 | 烧杯和澄清石灰水的总质量180.0g | 烧杯和烧杯内物质的总质量184.3g |
| 第二组 | 玻璃管和氧化铜样品的总质量是44.5g | 玻璃管和管内物质的总质量是42.9g |
(2)有关的化学方程式为______ Cu+CO2,CO2+Ca(OH)2=CaCO3↓+H2O
 查看习题详情和答案>>
查看习题详情和答案>>
现有含杂质的氧化铜样品,为测定该样品中氧化铜的质量分数,某同学称取一定质量的这样品,用下图装置进行实验,得到如下数据(假设样品中的杂质不参加反应).请回答:
(1)写出装置中任意一种仪器的名称______,
(2)澄清石灰水出现白色浑浊,此现象说明______.
(3)写出CO与CuO发生化学反应的化学方程式______ Cu+CO2 查看习题详情和答案>>
| 反应前 | 氧化铜被完全还原后 | 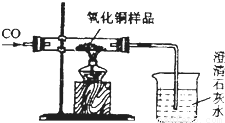 | |
| A组 | 玻璃管和氧化铜样品质量为m1g | 玻璃管和固体物质的质量为m2g | |
| B组 | 烧杯和澄清石灰水的质量为m3g | 烧杯和烧杯中物质的质量为m1g |
(2)澄清石灰水出现白色浑浊,此现象说明______.
(3)写出CO与CuO发生化学反应的化学方程式______ Cu+CO2 查看习题详情和答案>>
 (2005?西城区一模)现有含杂质的氧化铜样品(杂质不参加反应),为了测定该样品中氧化铜的质量分数,某同学称取12.5g样品,并用如图所示的装置进行实验,得到如下两组数据:
(2005?西城区一模)现有含杂质的氧化铜样品(杂质不参加反应),为了测定该样品中氧化铜的质量分数,某同学称取12.5g样品,并用如图所示的装置进行实验,得到如下两组数据:| 反应前 | 氧化铜完全反应后 | |
| 第一组 | 烧杯和澄清石灰水的总质量180.0g | 烧杯和烧杯内物质的总质量184.3g |
| 第二组 | 玻璃管和氧化铜样品的总质量是44.5g | 玻璃管和管内物质的总质量是42.9g |
黑色粉末变为红色,澄清石灰水变浑浊
黑色粉末变为红色,澄清石灰水变浑浊
.(2)有关的化学方程式为
CO+CuO
Cu+CO2,CO2+Ca(OH)2=CaCO3↓+H2O
| ||
CO+CuO
Cu+CO2,CO2+Ca(OH)2=CaCO3↓+H2O
.
| ||
(3)假设样品完全反应,应选择
二
二
组数据计算,样品中氧化铜的质量分数是64%
64%
.(4)该同学所用实验装置的不足之处是
没有处理含有CO的尾气
没有处理含有CO的尾气
.