网址:http://m.1010jiajiao.com/timu3_id_89016[举报]
(1)写出五种元素的元素符号:A:
(2)用电子式表示离子化合物A2B的形成过程:


(3)写出下列物质的电子式:
①D元素形成的单质:


②E与B形成的化合物:
 或
或
 或
或
③A、B、E形成的化合物:


④D与E形成的化合物:
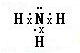
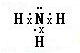
⑤C、D、E形成的离子化合物:
 或
或
 或
或
(1)写出下列元素的元素名称:A
(2)用电子式表示离子化合物A2B的形成过程:


(3)写出D元素形成的单质的结构式
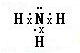
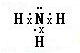
(4)实验室制取D的氢化物的化学方程式
| ||
| ||
(5)A、B两元素组成的化合物A2B2属于
(1)写出五种元素名称:
A________,B________,C________,D________,E________。
(2)用电子式表示离子化合物A2B的形成过程________________________。
(3)写出D元素形成的单质的结构式:________________________。
(4)写出下列物质的电子式:
E与B形成的化合物________; A、B、E形成的化合物________;
D、E形成的化合物________;
(5)A、B两元素组成的化合物A2B2属于________(填“离子”或“共价”)化合物,存在的化学键是________、________,写出A2B2与水反应的化学方程式:________________。
查看习题详情和答案>>试回答下列问题:
(1)写出五种元素的名称:A____________,B____________,C____________,D____________,E____________。
(2)用电子式表示离子化合物A2B的形成过程:_____________________________________。
(3)写出下列物质的电子式:
D元素形成的单质_____________________________________________;
E与B形成的化合物____________________________________________;
A、B、E形成的化合物_________________________________________;
D与E形成的共价化合物________________________________________。
查看习题详情和答案>>