摘要:10.25 ℃时.向20 mL 0.1 mol·L-1NaOH溶液中逐滴加入0.2 mol·L-1醋酸溶液.其pH变化曲线如下图所示.有关粒子浓度关系的比较中.正确的是 ( ) A.在A点:c(Na+)>c(OH-)>c(CH3COO-)>c(H+) B.在A点:c(Na+)+c(H+)=c(OH-)+c(CH3COO-) C.在B点:c(CH3COO-)>c(Na+)>c(H+)=c(OH-) D.在C点:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) [解析] A点CH3COOH与NaOH正好反应.得到CH3COONa溶液.CH3COO-少量水解.故c(CH3COO-)>c(OH-).A项错.在B点.由电荷守恒知.c(CH3COO-)=c(Na+).在C点的溶液应为CH3COOH与CH3COONa等浓度的混合液.呈酸性. [答案] BD
网址:http://m.1010jiajiao.com/timu3_id_88213[举报]
下列图示与对应的叙述相符的是( )

① ② ③ ④
A.图①表示25℃时,用0.1 mol·L-1盐酸滴定20 mL 0.1 mol·L-1NaOH溶液,溶液的pH随加入酸体积的变化
B.图②中曲线表示反应2A(g) + B(g)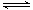 2C(g) ΔH > 0,正、逆反应的平衡常数K随温度的变化
2C(g) ΔH > 0,正、逆反应的平衡常数K随温度的变化
C.图③表示压强对可逆反应2A(g)+2B(g) 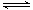 3C(g)+D(s)的影响,乙的压强比甲的压强大
3C(g)+D(s)的影响,乙的压强比甲的压强大
D.据图④若除去CuSO4溶液中的Fe3+可向溶液中加入适量CuO至pH在4左右。
查看习题详情和答案>>
下列图示与对应的叙述相符的是( )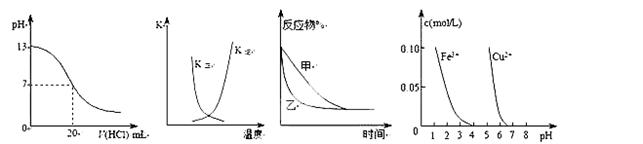
① ② ③ ④
| A.图①表示25℃时,用0.1 mol·L-1盐酸滴定20 mL 0.1 mol·L-1NaOH溶液,溶液的pH随加入酸体积的变化 |
B.图②中曲线表示反应2A(g) + B(g) 2C(g) ΔH > 0,正、逆反应的平衡常数K随温度的变化 2C(g) ΔH > 0,正、逆反应的平衡常数K随温度的变化 |
C.图③表示压强对可逆反应2A(g)+2B(g)  3C(g)+D(s)的影响,乙的压强比甲的压强大 3C(g)+D(s)的影响,乙的压强比甲的压强大 |
| D.据图④若除去CuSO4溶液中的Fe3+可向溶液中加入适量CuO至pH在4左右。 |

 2C(g) ΔH > 0,正、逆反应的平衡常数K随温度的变化
2C(g) ΔH > 0,正、逆反应的平衡常数K随温度的变化