摘要:7.对可逆反应4NH3(g)+5O2(g)4NO(g)+6H2O(g).下列叙述正确的是( ) A.达到化学平衡时.4v正(O2)=5v逆(NO) B.若单位时间内生成x mol NO的同时.消耗x mol NH3.则反应达到平衡状态 C.达到化学平衡时.若增加容器体积.则正反应速率减小.逆反应速率增大 D.化学反应速率关系是:2v正(NH3)=3v正(H2O) [解析] 本题综合考查化学平衡的建立及外界条件对化学反应速率的影响.根据不同物质表示同一反应时的速率关系可知.v逆(O2)∶v逆(NO)=5∶4.v逆(NO)=v逆(O2).代入A中表达式知v正(O2)=v逆(O2).A正确,NO的生成与NH3的消耗同时表示正反应在任意时刻都成比例.故B不正确,达到平衡时.增加容器体积.反应物.生成物浓度同时减小.正逆反应速率同时减小.C不正确.在反应的任意状态总有v正(NH3)∶v正(H2O)=4∶6即3v正(NH3)=2v正 (H2O).D不正确. [答案] A
网址:http://m.1010jiajiao.com/timu3_id_88143[举报]
对可逆反应4NH3(g)+5O2(g)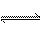 4NO(g)+6H2O(g),下列叙述正确的是( )
4NO(g)+6H2O(g),下列叙述正确的是( )
A.达到化学平衡时,4v正(O2)=5v逆(NO)
B.若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达到平衡状态
C.达到化学平衡时,若增加容器体积,则正反应速率减小,逆反应速率增大
D.化学反应速率关系是:2v正(NH3)=3v逆(H2O)
查看习题详情和答案>>
对可逆反应4NH3(g)+5O2(g)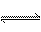 4NO(g)+6H2O(g),下列叙述正确的是( )
4NO(g)+6H2O(g),下列叙述正确的是( )
A.达到化学平衡时4v正(O2)=5v逆(CO)
B.若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达到平衡状态
C.达到化学平衡时,若增加容器体积,则正反应速率减小,逆反应速率增大
D.化学反应速率关系是:2v正(NH3)=3v正(H2O)
查看习题详情和答案>>
对可逆反应4NH3(g)+5O2(g)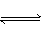 4NO(g)+6H2O(g),下列叙述正确的是( )
4NO(g)+6H2O(g),下列叙述正确的是( )
A.达到化学平衡时4v正(O2)=5v逆(CO)
B.若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达到平衡状态
C.达到化学平衡时,若增加容器体积,则正反应速率减小,逆反应速率增大
D.化学反应速率关系是:2v正(NH3)=3v正(H2O)
查看习题详情和答案>>