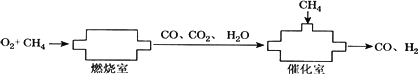摘要:CO和H2是有机合成的重要原料.某化学小组拟用下列装置抽取合成气CO.H2O.将x mol O2和一定量CH4在燃烧室中不完全燃烧.产生的物质完全进入催化室与CH4恰好完全反应.生成CO和H2.则从催化室中出来的H2为( ) A.x mol B.3x mol C.4x mol D.5x mol
网址:http://m.1010jiajiao.com/timu3_id_86150[举报]
CO和H2是有机合成的重要原料.某化学小组拟用下列装置制取合成气CO、H2.将xmol O2和一定量CH4在燃烧室中不完全燃烧,产生的物质完全进入催化室与CH4恰好完全反应,生成CO和H2.则从催化室中出来的H2为( )

查看习题详情和答案>>
|
CO和H2是有机合成的重要原料.某化学小组拟用下列装置制取合成气CO、H2.将x mol O2和一定量CH4在燃烧室中不完全燃烧,产生的物质进入催化室与CH4恰好完全反应,生成CO和H2.则从催化室中出来的H2为
| |
| [ ] | |
A. |
x mol |
B. |
3 x mol |
C. |
4 x mol |
D. |
5 x mol |
|
CO和H2是有机合成的重要原料.某化学小组拟用下列装置抽取合成气CO、H2O.将x mol O2和一定量CH4在燃烧室中不完全燃烧,产生的物质完全进入催化室与CH4恰好完全反应,生成CO和H2.则从催化室中出来的H2为
| |
| [ ] | |
A. |
x mol |
B. |
3x mol |
C. |
4x mol |
D. |
5x mol |
CO和H2是有机合成的重要原料.某化学小组拟用下列装置制取合成气CO、H2.将xmol O2和一定量CH4在燃烧室中不完全燃烧,产生的物质完全进入催化室与CH4恰好完全反应,生成CO和H2.则从催化室中出来的H2为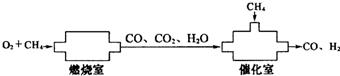
- A.xmol
- B.3xmol
- C.4xmol
- D.5xmol
甲醇又称“木精”,是重要的溶剂和基本有机原料.工业上常以CO和H2为原料合成甲醇.
(1)已知每1g液态甲醇不完全燃烧生成一氧化碳和液态水时放出13.8kJ热量,写出甲醇不完全燃烧的热化学方程式: .
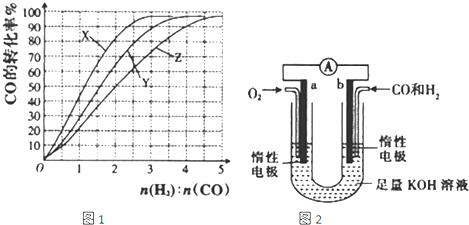
(2)工业上常利用反应:CO(g)+2H2(g)=CH3OH(g)△H<0合成甲醇,其在230~270℃下反应最为有利.为研究合成气最合适的起始组成比,在230℃、250℃和270℃进行实验,结果如图所示,则230℃时的实验结果所对应的曲线是 (填字母,下同);该温度下工业生产适宜采用的合成气组成n(H2):n(CO)的比值范围是 .
A.1~1.5B.2.5~3C.3.5~4.5
(3)制甲醇所需要的氢气,可用下列反应制取:HO2(g)+CO(g)?H2(g)+CO2(g)△H<0
150℃时,在容积为2L的恒温恒容密闭容器中充入1mol CO和2molH2O(g),反应达到平衡后测得H2的体积分数为25%.
①平衡时CO的转化率为 .
②150℃下,若起始时充入2molCO和4molH2O(g),反应达到平衡时CO2的体积分数为 .
(4)某研究小组设计了如图所示的原电池装置,向导管中通入物质的量之比为1:1的CO和H2混合气体(CO和H2同时放电).
①电池工作一段时间后,电解质溶液的pH (填“增大”、“减小”或“不变”).
②电池工作一段时间后,测得电解质溶液增重6.2g(不考虑未反应气体的溶解),则负极参加反应的气体质量为 .
查看习题详情和答案>>
(1)已知每1g液态甲醇不完全燃烧生成一氧化碳和液态水时放出13.8kJ热量,写出甲醇不完全燃烧的热化学方程式:
(2)工业上常利用反应:CO(g)+2H2(g)=CH3OH(g)△H<0合成甲醇,其在230~270℃下反应最为有利.为研究合成气最合适的起始组成比,在230℃、250℃和270℃进行实验,结果如图所示,则230℃时的实验结果所对应的曲线是
A.1~1.5B.2.5~3C.3.5~4.5

(3)制甲醇所需要的氢气,可用下列反应制取:HO2(g)+CO(g)?H2(g)+CO2(g)△H<0
150℃时,在容积为2L的恒温恒容密闭容器中充入1mol CO和2molH2O(g),反应达到平衡后测得H2的体积分数为25%.
①平衡时CO的转化率为
②150℃下,若起始时充入2molCO和4molH2O(g),反应达到平衡时CO2的体积分数为
(4)某研究小组设计了如图所示的原电池装置,向导管中通入物质的量之比为1:1的CO和H2混合气体(CO和H2同时放电).
①电池工作一段时间后,电解质溶液的pH
②电池工作一段时间后,测得电解质溶液增重6.2g(不考虑未反应气体的溶解),则负极参加反应的气体质量为