摘要:3.已知金属离子的氧化性:Cu2+>Ni2+>Fe2+>Zn2+.金属镍有广泛用途.粗镍中含有少量的Fe.Zn.Cu.Pt等杂质.可用电解法制备高纯度的镍.下列叙述正确的是( ) A.阳极发生还原反应.其电极反应式为Ni2++2e-===Ni B.电解过程中.阳极减少的质量等于阴极增加的质量 C.电解后.溶液中存在的金属阳离子只有Fe2+和Zn2+ D.电解后.电解槽底部的阳极泥中只有铜和铂两种金属单质 解析:电解池中阳极发生氧化反应.电极反应为Ni-2e-===Ni2+.Zn-2e-===Zn2+.Fe-2e-===Fe2+.A项错误,阳极镍.铁.锌都溶解.而阴极只析出镍.故阳极减少的质量不等于阴极增加的质量.B项错误,镍精炼实验中的电解质溶液是镍盐.溶液中存在Ni2+.Fe2+.Zn2+.C项错误,铜.铂没有溶解.D项正确. 答案:D
网址:http://m.1010jiajiao.com/timu3_id_85228[举报]
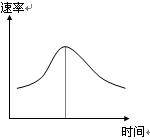
(6分)氯酸钾和亚硫酸氢钠发生氧化还原反应生成Cl(-1价)和S(+6价)的速率如图曲线所示,已知ClO3-的氧化性随c(H+)的增大而增强,有关方程式为:
ClO3-+3 HSO3- Cl-+3 H+ +3 SO42-
Cl-+3 H+ +3 SO42-

(1)反应开始时反应速率加快的原因是 ;
(2)反应后期反应速率下降的原因是 。
查看习题详情和答案>>
 氯酸钾和亚硫酸氢钠发生氧化还原反应生成Cl(-1价)
氯酸钾和亚硫酸氢钠发生氧化还原反应生成Cl(-1价)
和S(+6价)的速率如图曲线所示,已知ClO3-的氧化性随
c(H+)的增大而增强,有关方程式为:
ClO3-+3 HSO3-![]() Cl-+3 H+ +3 SO42-
Cl-+3 H+ +3 SO42-
(1)反应开始时反应速率加快的原因是 ![]()
(2)反应后期反应速率下降的原因是
查看习题详情和答案>>
(6分)氯酸钾和亚硫酸氢钠发生氧化还原反应生成Cl(-1价)和S(+6价)的速率如图曲线所示,已知ClO3-的氧化性随c(H+)的增大而增强,有关方程式为:
ClO3-+3 HSO3-Cl-+3 H+ +3 SO42-
(1)反应开始时反应速率加快的原因是 ;
(2)反应后期反应速率下降的原因是 。
查看习题详情和答案>>
 Cl-+3 H+ +3 SO42-
Cl-+3 H+ +3 SO42-