摘要:11.如何利用实验室常见的药品试剂探究11-17号元素的金属性逐渐减 弱.非金属性逐渐增强?已知实验室有你想用到的仪器和药品.试纸等一切用品. 猜想与假设:(1)用 三种金属分别与水反应.通过观察生成气泡的速率便会 得出从 到 金属性减弱. (2)因实验室不可能有硅单质.但可以测0.1 mol/L的 溶液和 溶液及 Na2SO4溶液的pH.推断三种盐溶液的水解情况.得出 . .硫酸三 种最高价含氧酸的酸性强弱顺序是 .从而得出从 到 非金属性增强. (3)制取饱和的氯水和饱和的氢硫酸溶液.用将 方法. 通过 现象便直接得出非金属性S比Cl弱. 设计和实施方案:(1)用列表的方式(从实验方案.实验现象.有关化学方程式)完成你 的实验报告中的实验内容. (2)实验结论是 . (3)请你用物质结构理论知识解释结论. 解析:[问题]变换一个角度就是实验目的.也应是要得出的结论.根据[猜想与假设] 可以设计实验方案.关键细节要注意到.如镁条.铝条都要用砂纸擦后去氧化膜放入 沸水中.设计的方案尽量具有可操作性和简单性. 答案:猜想与假设:(1)钠.镁.铝 钠 铝 (2)Na2SiO3 Na3PO4 硅酸 磷酸 H2SiO3<H3PO4<H2SO4 Si S (3)饱和氯水滴加到饱和氢硫酸溶液中的 溶液中有浅黄色沉淀生成的(或溶液变浑 浊) 设计和实施方案 (1) 实验方案 实验现象 有关化学方程式 用砂纸擦后的镁条.铝条分别投入到盛有沸水的小烧杯中.再分别滴加酚酞 投入镁条的试管有大量气泡产生.滴加酚酞后溶液变成浅红色,投入铝条的试管中无明显现象. Mg+2H2O Mg(OH)2+H2↑ 将一绿豆粒大小的钠投入到盛有冷水且预先滴有酚酞的小烧杯中 钠浮于水面上.迅速熔成闪亮小球四处游动.有响声.随之消失.溶液很快变红色 2Na+2H2O===2NaOH+H2↑ 用玻璃棒分别蘸取0.1 mol/L的Na2SiO3(aq).Na3PO4(aq).Na2SO4(aq)测其pH Na2SiO3(aq)的pH比Na3PO4(aq)的pH大,Na2SO4 SiO-+2H2OSiO3-+ OH- PO-+H2OHPO-+OH- 用胶头滴管向盛有5 mL饱和氢硫酸溶液的试管中滴加饱和的氯水 试管中有淡黄色沉淀生成 Cl2+H2S===2HCl+S↓ (2)金属性:Na>Mg>Al 非金属性:Si<P<S<Cl (3)Na.Mg.Al.Si.P.S.Cl原子核外都有三个电子层.但最外层电子数依次为1.
网址:http://m.1010jiajiao.com/timu3_id_82806[举报]
如何利用实验室常见的药品试剂探究11号~17号元素的金属性逐渐减弱,非金属性逐渐增强?已知实验室有你想用到的仪器和药品、试纸等一切用品.
猜想与假设:(1)用
(2)因实验室不可能有硅单质,但可以测0.1mol/L的
(3)制取饱和的氯水和饱和的氢硫酸溶液,用将
设计和实施方案:(1)用列表的方式(从实验方案、实验现象、有关化学方程式)完成你的实验报告中的实验内容.
(2)实验结论是
(3)请你用物质结构理论知识解释结论.
查看习题详情和答案>>
猜想与假设:(1)用
钠、镁、铝
钠、镁、铝
三种金属分别与水反应,通过观察生成气泡的速率便会得出从钠
钠
到铝
铝
金属性逐渐减弱.(2)因实验室不可能有硅单质,但可以测0.1mol/L的
Na2SiO3
Na2SiO3
溶液和Na3PO4
Na3PO4
溶液及Na2SO4溶液的pH,推断三种盐溶液的水解情况,得出H2SiO3
H2SiO3
、H3PO4
H3PO4
、硫酸三种最高价含氧酸的酸性强弱顺序是H2SiO3<H3PO4<H2SO4
H2SiO3<H3PO4<H2SO4
,从而得出从Si
Si
到S
S
非金属性逐渐增强.(3)制取饱和的氯水和饱和的氢硫酸溶液,用将
饱和氯水滴加到饱和氢硫酸溶液中的
饱和氯水滴加到饱和氢硫酸溶液中的
方法,通过溶液中有浅黄色沉淀生成
溶液中有浅黄色沉淀生成
现象便直接得出非金属性S比Cl弱.设计和实施方案:(1)用列表的方式(从实验方案、实验现象、有关化学方程式)完成你的实验报告中的实验内容.
(2)实验结论是
金属性:Na>Mg>Al,非金属性:Si<P<S<Cl
金属性:Na>Mg>Al,非金属性:Si<P<S<Cl
.(3)请你用物质结构理论知识解释结论.
如何利用实验室常见的药品试剂探究11号~17号元素的金属性逐渐减弱,非金属性逐渐增强?已知实验室有你想用到的仪器和药品、试纸等一切用品.
猜想与假设:(1)用______三种金属分别与水反应,通过观察生成气泡的速率便会得出从______到______金属性逐渐减弱.
(2)因实验室不可能有硅单质,但可以测0.1mol/L的______溶液和______溶液及Na2SO4溶液的pH,推断三种盐溶液的水解情况,得出______、______、硫酸三种最高价含氧酸的酸性强弱顺序是______,从而得出从______到______非金属性逐渐增强.
(3)制取饱和的氯水和饱和的氢硫酸溶液,用将______方法,通过______现象便直接得出非金属性S比Cl弱.
设计和实施方案:(1)用列表的方式(从实验方案、实验现象、有关化学方程式)完成你的实验报告中的实验内容.
(2)实验结论是______.
(3)请你用物质结构理论知识解释结论.
查看习题详情和答案>>
猜想与假设:(1)用______三种金属分别与水反应,通过观察生成气泡的速率便会得出从______到______金属性逐渐减弱.
(2)因实验室不可能有硅单质,但可以测0.1mol/L的______溶液和______溶液及Na2SO4溶液的pH,推断三种盐溶液的水解情况,得出______、______、硫酸三种最高价含氧酸的酸性强弱顺序是______,从而得出从______到______非金属性逐渐增强.
(3)制取饱和的氯水和饱和的氢硫酸溶液,用将______方法,通过______现象便直接得出非金属性S比Cl弱.
设计和实施方案:(1)用列表的方式(从实验方案、实验现象、有关化学方程式)完成你的实验报告中的实验内容.
(2)实验结论是______.
(3)请你用物质结构理论知识解释结论.
如何利用实验室常见的药品试剂探究11号~17号元素的金属性逐渐减弱,非金属性逐渐增强?已知实验室有你想用到的仪器和药品、试纸等一切用品.
猜想与假设:(1)用______三种金属分别与水反应,通过观察生成气泡的速率便会得出从______到______金属性逐渐减弱.
(2)因实验室不可能有硅单质,但可以测0.1mol/L的______溶液和______溶液及Na2SO4溶液的pH,推断三种盐溶液的水解情况,得出______、______、硫酸三种最高价含氧酸的酸性强弱顺序是______,从而得出从______到______非金属性逐渐增强.
(3)制取饱和的氯水和饱和的氢硫酸溶液,用将______方法,通过______现象便直接得出非金属性S比Cl弱.
设计和实施方案:(1)用列表的方式(从实验方案、实验现象、有关化学方程式)完成你的实验报告中的实验内容.
(2)实验结论是______.
(3)请你用物质结构理论知识解释结论.
查看习题详情和答案>>
猜想与假设:(1)用______三种金属分别与水反应,通过观察生成气泡的速率便会得出从______到______金属性逐渐减弱.
(2)因实验室不可能有硅单质,但可以测0.1mol/L的______溶液和______溶液及Na2SO4溶液的pH,推断三种盐溶液的水解情况,得出______、______、硫酸三种最高价含氧酸的酸性强弱顺序是______,从而得出从______到______非金属性逐渐增强.
(3)制取饱和的氯水和饱和的氢硫酸溶液,用将______方法,通过______现象便直接得出非金属性S比Cl弱.
设计和实施方案:(1)用列表的方式(从实验方案、实验现象、有关化学方程式)完成你的实验报告中的实验内容.
(2)实验结论是______.
(3)请你用物质结构理论知识解释结论.
查看习题详情和答案>>
利用化学反应可以制备新物质,下列是实验室中常见的药品和装置:
药品:过氧化氢溶液、二氧化锰、浓盐酸、氢氧化钠溶液、浓硫酸、饱和氯化钠溶液、水.
装置:

(1)利用上述药品在实验室中能制备氯气和氧气,二氧化锰的作用分别为
(2)制取氯气选用的发生装置为
(3)实验室制取氧气的反应原理是
查看习题详情和答案>>
药品:过氧化氢溶液、二氧化锰、浓盐酸、氢氧化钠溶液、浓硫酸、饱和氯化钠溶液、水.
装置:

(1)利用上述药品在实验室中能制备氯气和氧气,二氧化锰的作用分别为
氧化剂(反应物)
氧化剂(反应物)
、催化剂
催化剂
.(2)制取氯气选用的发生装置为
A
A
,用装置C除去氯气中混有的HCl气体,C中应盛装的试剂为饱和食盐水
饱和食盐水
,气体从c
c
管进;装置D的作用是尾气处理
尾气处理
.(3)实验室制取氧气的反应原理是
2H2O
2H2O+O2↑
| ||
2H2O
2H2O+O2↑
.制备并收集一瓶干燥的氧气,装置中导管连接顺序为
| ||
b
b
→c→d→g
g
→f
f
;其中C中应盛装的试剂为浓H2SO4
浓H2SO4
.某校化学研究性学习小组利用下面所提供的仪器装置和药品制取NaHCO![]() 溶液,设计如下实验。实验室提供的药品、仪器装置如下:
溶液,设计如下实验。实验室提供的药品、仪器装置如下:
药品:①2% NaOH溶液②稀HCl③稀H![]() SO
SO![]() ④饱和KHCO
④饱和KHCO![]() 溶液⑤浓H
溶液⑤浓H![]() SO
SO![]() ⑥CaCO
⑥CaCO![]() 固体⑦K
固体⑦K![]() CO
CO![]() 粉末
粉末
仪器装置(如图所示):
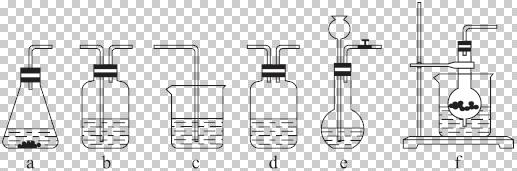
请根据题目要求完成下列问题:
请按下表要求,填写选择的装置和药品。
| 分项 内容 | CO (随开随用,随关随停) (X) | 除杂洗 气装置 (Y) | 制备产 品装置 (Z) |
| 选择的装置 (填序号) | C | ||
| 选择的药品 (填序号) | ① |
(2)如何检验所选择的CO![]() 发生装置(X)的气密性,请写出主要操作过程:__________。
发生装置(X)的气密性,请写出主要操作过程:__________。
(3)将装置按X、Y、Z顺序连接并检查气密性后,当加入药品实验时,X装置中发生化学反应的离子方程式为_____________,Y装置中除去的杂质为_________________。
(4)常温下,向Z装置的NaOH溶液中通入过量CO2气体,其目的是______________。
(5)若要保证Z装置中不析出晶体(不考虑过饱和溶液问题),NaOH溶液最大浓度不能超过________________%(质量分数)。
附:有关物质在常温(25 ℃)时的溶解度
| 化学式 | Na | NaHCO | NaOH | NaCl | Na |
| 溶解度 (g/100 g H | 21.3 | 9.60 | 107 | 35.8 | 19.4 |