摘要:12.(2010年云南大理四校联考)25℃时.氢氧化钠的溶解度为40 g.向100 g 水中投入一定量金属钠.反应完全后.恢复至25℃.此时溶液恰好处于饱和状态且无晶体析出.则投入的钠的质量约为( ) A.23.5 g B.11.5 g C.19.5 g D. 23.0 g
网址:http://m.1010jiajiao.com/timu3_id_82127[举报]
25℃时,氢氧化钠的溶解度为40 g.向100 g 水中投入一定量金属钠,反应完全后,恢复至25℃,此时溶液恰好处于饱和状态且无任何晶体析出,则投入的钠的质量约为
A.23.5 g B.11.5 g C.23.0 g D.19.5 g
查看习题详情和答案>>25℃时,氢氧化钠的溶解度为40 g,向100 g 水中投入一定量金属钠,反应完全后,恢复至25℃,此时溶液恰好处于饱和状态且无晶体析出,则投入的钠的质量约为( )
A.23.5 g ![]() 11.5 g C.19.5 g D. 23.0 g
11.5 g C.19.5 g D. 23.0 g
重铬酸钠(Na2Cr2O7)广泛用于合成颜料、媒染剂等.以铬铁矿(主要成分为Cr2O3,还含有FeO,Al2O3,SiO2等杂质)为原料制取重铬酸钠的流程图如图所示: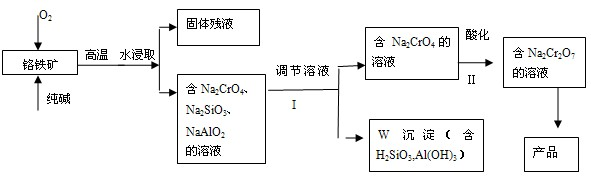
请回答下列问题:
(1)若步骤I中只用一种试剂调节溶液的pH,应选用
A.稀硫酸 B.氢氧化钠固体 C.氢氧化钾溶液
(2)步骤I中,调节溶液pH后,如果溶液的pH过小,可能导致W沉淀部分溶解,原因是:
(3)步骤Ⅱ中,Na2CrO4转化为Na2Cr2O7的离子反应如下:2CrO42-(黄色)+2H+=Cr2O72-(橙红色)+H2O
①该反应
.
②若向Na2Cr2O7溶液(橙红色)中加入足量的NaOH固体,溶液
A.变黄色 B.颜色不变 C.橙红色溶液
③已知:25℃时,Ag2CrO4的Ksp=1.12×10-12,Ag2Cr2O7的Ksp=2×10-7.25℃时,向Na2Cr2O7溶液中加入AgNO3溶液,最终只生成一种砖红色沉淀,该沉淀的化学式是
查看习题详情和答案>>

请回答下列问题:
(1)若步骤I中只用一种试剂调节溶液的pH,应选用
A
A
(填标号).A.稀硫酸 B.氢氧化钠固体 C.氢氧化钾溶液
(2)步骤I中,调节溶液pH后,如果溶液的pH过小,可能导致W沉淀部分溶解,原因是:
Al(OH)3+3H+=Al3++3H2O
Al(OH)3+3H+=Al3++3H2O
(用离子方程式表示).(3)步骤Ⅱ中,Na2CrO4转化为Na2Cr2O7的离子反应如下:2CrO42-(黄色)+2H+=Cr2O72-(橙红色)+H2O
①该反应
不是
不是
氧化还原反应(填“是”或“不是”),反应的平衡常数表达式:K=| c(Cr2O72-) |
| c2(CrO42-)?c2(H+) |
| c(Cr2O72-) |
| c2(CrO42-)?c2(H+) |
②若向Na2Cr2O7溶液(橙红色)中加入足量的NaOH固体,溶液
A
A
(填标号)A.变黄色 B.颜色不变 C.橙红色溶液
③已知:25℃时,Ag2CrO4的Ksp=1.12×10-12,Ag2Cr2O7的Ksp=2×10-7.25℃时,向Na2Cr2O7溶液中加入AgNO3溶液,最终只生成一种砖红色沉淀,该沉淀的化学式是
Ag2CrO4
Ag2CrO4
.