摘要:15.(2010·潍坊一中期中考题)2008年奥运会在北京举行.右图象征奥运会会旗的五圆环.表示A.B.C.D.E.五种化合物.圆环交叉部分代表两种化合物含有一种相同元素.五种化合物由5种短周期元素组成.且每种化合物仅由两种元素组成.A是可燃冰的主要成分.B.E分子中所含电子总数与硅烷(SiH4)分子的电子数相等.B不稳定.具有较强氧化性.能发生自身氧化还原反应.E的相对分子质量为32.具有还原性.且常用作航天器的燃料.C能发生反应:化合物化合物.D是新型无机非金属材料.它所含两种元素的原子个数之比为3∶4.电子数之比为3∶2. (1)B的水溶液呈酸性.用离子方程式表示其原因是 ,D的化学式为 . (2)A.B.E中均含有一种元素.其名称为 . (3)B和E反应生成单质G和常见的液态化合物H.写出化学方程式: . (4)写出C符合“化合物化合物 的化学方程式: . 解析:可燃冰是甲烷结晶水合物.硅烷分子是18电子结构.H2O2含18个电子.且具有较强氧化性.能发生自身氧化还原反应,相对分子质量为32的有:O2.S.N2H4等.根据五圆环可推知.A为CH4.B为H2O2.C为SiO2.D为Si3N4.E为N2H4.两种化合物在高温下生成另两种化合物的反应.在中学化学中符合条件的有制普通玻璃的化学反应. 答案:(1)H2O2HO2-+H+ Si3N4 2H2O2+N2H4===N2+4H2O (4)Na2CO3+SiO2Na2SiO3+CO2↑或CaCO3+SiO2CaSiO3+CO2↑
网址:http://m.1010jiajiao.com/timu3_id_81027[举报]
2008年奥运会在北京举行,下图类似奥运五元环,表示A、B、C、D、E五种化合物,元环交叉部分代表两种化合物含有一种相同元素,五种化合物由五种短周期元素组成,且每种化合物仅由两种元素组成.A是可燃冰的主要成分;B、E分子中所含电子总数均与硅烷(SiH4)分子的电子数相等,B不稳定,具有较强氧化性,能发生自身氧化还原反应,E的相对分子质量为32,具有还原性,且常用作航天器的燃料;C能发生反应:化合物(Ⅰ)+化合物(Ⅱ) 化合物(Ⅲ)+化合物(Ⅳ);D是新型无机非金属材料,它所含两种元素的原子个数之比为3∶4,电子数之比为3∶2
化合物(Ⅲ)+化合物(Ⅳ);D是新型无机非金属材料,它所含两种元素的原子个数之比为3∶4,电子数之比为3∶2
 化合物(Ⅲ)+化合物(Ⅳ);D是新型无机非金属材料,它所含两种元素的原子个数之比为3∶4,电子数之比为3∶2
化合物(Ⅲ)+化合物(Ⅳ);D是新型无机非金属材料,它所含两种元素的原子个数之比为3∶4,电子数之比为3∶2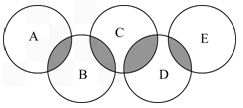
(1)B的水溶液呈酸性,用离子方程式表示其原因是________;D的化学式为________.
(2)A、B、E中含有一种相同的元素,其名称为________.
(3)B和E反应可生成单质G和常见的液态化合物H,写出化学方程式________.
(4)写出C符合“化合物(Ⅰ)+化合物(Ⅱ) 化合物(Ⅲ)+化合物(Ⅳ)”的化学方程式______________________________________.
化合物(Ⅲ)+化合物(Ⅳ)”的化学方程式______________________________________.
查看习题详情和答案>>
(2)A、B、E中含有一种相同的元素,其名称为________.
(3)B和E反应可生成单质G和常见的液态化合物H,写出化学方程式________.
(4)写出C符合“化合物(Ⅰ)+化合物(Ⅱ)
 化合物(Ⅲ)+化合物(Ⅳ)”的化学方程式______________________________________.
化合物(Ⅲ)+化合物(Ⅳ)”的化学方程式______________________________________. 2008年奥运会在北京举行,下图类似奥运五元环,表示A、B、C、D、E五种化合物,元环交叉部分代表两种化合物含有一种相同元素,五种化合物由五种短周期元素组成,且每种化合物仅由两种元素组成。A是可燃冰的主要成分;B、E分子中所含有电子总数均与硅烷(SiH4)分子的电子数相等,B不稳定,具有较强氧化性,能发生自身氧化还原反应;E的相对分子质量为32,具有还原性,且常用作航天器的燃料。C能发生反应:化合物(Ⅰ)+化合物(Ⅱ)![]() 化合物(Ⅲ)+化合物(Ⅳ)。D是新型无机非金属材料,它所含有两种元素的原子个数之比为3:4,电子数之比为3:2。
化合物(Ⅲ)+化合物(Ⅳ)。D是新型无机非金属材料,它所含有两种元素的原子个数之比为3:4,电子数之比为3:2。

(1)A的电子式为 ;D的化学式为 。
(2)A、B、E中含有一种相同的元素,其名称为 。
(3)B和E反应可生成单质G和常见的液态化合物H,写出化学反应方程式 。
(4)说出C物质的一种用途: 。
查看习题详情和答案>>