摘要:4.硫酸盐:BaSO4.PbSO4难溶.Ag2SO4.Hg2SO4.CaSO4微溶.其它都易溶.
网址:http://m.1010jiajiao.com/timu3_id_80284[举报]
硫酸盐在生产生活中有广泛应用.
Ⅰ.工业上以重晶石(主要成分BaSO4)为原料制备BaCl2,其工艺流程示意图如图1所示:

某研究小组查阅资料得:
BaSO4(s)+4C(s)
4CO(g)+BaS(s)△H1=+571.2kJ?mol-1 ①
BaSO4(s)+2C(s)
2CO2(g)+BaS(s)△H2=+226.2kJ?mol-1 ②
(1)用过量NaOH溶液吸收气体,得到硫化钠.该反应的离子方程式是
H2S+OH-
(2)反应C(s)+CO2(g)═2CO(g)的△H=
(3)实际生产中必须加入过量的炭,同时还要通入空气,其目的有两个
①从原料角度看,
②从能量角度看,①②为吸热反应,炭和氧气反应放热维持反应所需高温.
(4)该小组同学想对BaSO4在水中的沉淀溶解平衡做进一步研究,查资料发现在某温度时BaSO4在水中的沉淀溶解平衡曲线如图2所示.
该小组同学提出以下四种观点:
①当向含有SO42-的溶液中加入Ba2+使SO42-沉淀
完全,则此时SO42-在溶液中的浓度为0
②加入Na2SO4可以使溶液由a点变到b点
③通过蒸发可以使溶液由d点变到c点
④d点无BaSO4沉淀生成
其中正确的是
Ⅱ.某燃料电池以CaHSO4固体为电解质传递H+,其基本结构如图3所示,电池总反应可表示为2H2+O2═2H2O.
请回答:
(5)H+由
(6)b极上发生的电极反应是
查看习题详情和答案>>
Ⅰ.工业上以重晶石(主要成分BaSO4)为原料制备BaCl2,其工艺流程示意图如图1所示:

某研究小组查阅资料得:
BaSO4(s)+4C(s)
| ||
BaSO4(s)+2C(s)
| ||
(1)用过量NaOH溶液吸收气体,得到硫化钠.该反应的离子方程式是
H2S+2OH-═2S2-+H2O
H2S+2OH-═2S2-+H2O
.S2-+H2O?HS-+OH-;HS-+H2O| 高温 |
(2)反应C(s)+CO2(g)═2CO(g)的△H=
+172.5 kJ?mol-1
+172.5 kJ?mol-1
.(3)实际生产中必须加入过量的炭,同时还要通入空气,其目的有两个
①从原料角度看,
使BaSO4得到充分的还原,提高BaS的产量
使BaSO4得到充分的还原,提高BaS的产量
;②从能量角度看,①②为吸热反应,炭和氧气反应放热维持反应所需高温.
(4)该小组同学想对BaSO4在水中的沉淀溶解平衡做进一步研究,查资料发现在某温度时BaSO4在水中的沉淀溶解平衡曲线如图2所示.
该小组同学提出以下四种观点:
①当向含有SO42-的溶液中加入Ba2+使SO42-沉淀
完全,则此时SO42-在溶液中的浓度为0
②加入Na2SO4可以使溶液由a点变到b点
③通过蒸发可以使溶液由d点变到c点
④d点无BaSO4沉淀生成
其中正确的是
④
④
(填序号).Ⅱ.某燃料电池以CaHSO4固体为电解质传递H+,其基本结构如图3所示,电池总反应可表示为2H2+O2═2H2O.
请回答:
(5)H+由
a
a
极通过固体酸电解质传递到另一极(填a或者b).(6)b极上发生的电极反应是
O2+4e-+4H+═2H2O
O2+4e-+4H+═2H2O
.(2011?嘉兴模拟)工业上用矿物M(含有X、Y、Z三种元素)在空气中高温煅烧,X、Y、Z分别转化成A、B、C三种产物,A、B、C的物质的量之比为1:1:2,其中A为单质,9.6g A溶于稀硝酸后产生标准状况下2.24L气体G,G遇空气呈红棕色,所得溶液中滴加浓氨水至过量,先产生沉淀,后沉淀溶解;B中Y元素与氧元素的质量比为7:2,B溶于适量的稀硝酸得到溶液W和无色气体G,W溶液中滴入硫氰化钾溶液呈血红色; C为酸性氧化物,且常温下呈气态,将C通入氯化钡溶液中,无明显变化现象,再滴加双氧水产生白色沉淀.
(1)指出Z元素在周期表中的位置
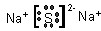 ;
;
(2)写出C与双氧水、氯化钡溶液产生沉淀的离子反应方程式
(3)在游泳池中通常用X的硫酸盐来消毒杀菌,试说明该盐能起消毒杀菌作用的本质原因是
(4)将X的单质溶于N2O4的乙酸乙酯溶液中可制得Y的无水硝酸盐,同时生成G,请写出以上反应的化学方程式
查看习题详情和答案>>
(1)指出Z元素在周期表中的位置
第3周期,ⅥA族
第3周期,ⅥA族
,Z与处于同一周期且原子半径最大的元素(除稀有气体)所形成的稳定化合物电子式为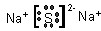
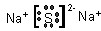
(2)写出C与双氧水、氯化钡溶液产生沉淀的离子反应方程式
H2O2+SO2+Ba2+=BaSO4↓+2H+
H2O2+SO2+Ba2+=BaSO4↓+2H+
;(3)在游泳池中通常用X的硫酸盐来消毒杀菌,试说明该盐能起消毒杀菌作用的本质原因是
Cu2+使蛋白质变性
Cu2+使蛋白质变性
;试推断M的化学式为CuFeS2
CuFeS2
.(4)将X的单质溶于N2O4的乙酸乙酯溶液中可制得Y的无水硝酸盐,同时生成G,请写出以上反应的化学方程式
Cu+2N2O4=Cu(NO3)2+2NO↑
Cu+2N2O4=Cu(NO3)2+2NO↑
.钡(Ba)和锶(Sr)及其化合物在工业上有着广泛的应用,它们在地壳中常以硫酸盐的形式存在,BaSO4和SrSO4都是难溶性盐.工业上提取钡和锶时首先将BaSO4和SrSO4转化成难溶弱酸盐.
已知:SrSO4(s)?Sr2+(aq)+SO2-4(aq) KSP=2.5×10-7
SrSO3(s)?Sr2+(aq)+CO2-4(aq) KSP=2.5×10-9
(1)将SrSO4转化成SrCO3的离子方程式为 ,该反应的平衡常数表达式为 ;该反应能发生的原因是 .(用沉淀溶解再平衡的有关理论解释)
(2)对于上述反应,实验证明增大CO2-3的浓度或降低温度都有利于提高SrSO4的转化率.判断在下列两种情况下,平衡常数K的变化情况(填“增大”、“减小”或“不变”):
①升高温度,平衡常数K将 ;
②增大CO2-3的浓度,平衡常数K将 .
(3)已知,SrSO4和SrCO3在酸中的溶解性与BaSO4和BaCO3类似,设计实验证明上述过程中SrSO4是否完全转化成SrCO3.实验所用试剂为 ;实验现象及其相应结论 .
(4)BaCl2溶液和Ba(NO3)2溶液是实验中检验SO2-4的常用试剂.某化学研究性学习小组检验某溶液中存在SO2-4时,首先加入Ba(NO3)2溶液,产生白色沉淀,然后加入过量稀硝酸,白色沉淀不溶解,由此得出结论:溶液中一定含有SO2-4.你认为该推理是否严密?试说明理由.
查看习题详情和答案>>
已知:SrSO4(s)?Sr2+(aq)+SO2-4(aq) KSP=2.5×10-7
SrSO3(s)?Sr2+(aq)+CO2-4(aq) KSP=2.5×10-9
(1)将SrSO4转化成SrCO3的离子方程式为
(2)对于上述反应,实验证明增大CO2-3的浓度或降低温度都有利于提高SrSO4的转化率.判断在下列两种情况下,平衡常数K的变化情况(填“增大”、“减小”或“不变”):
①升高温度,平衡常数K将
②增大CO2-3的浓度,平衡常数K将
(3)已知,SrSO4和SrCO3在酸中的溶解性与BaSO4和BaCO3类似,设计实验证明上述过程中SrSO4是否完全转化成SrCO3.实验所用试剂为
(4)BaCl2溶液和Ba(NO3)2溶液是实验中检验SO2-4的常用试剂.某化学研究性学习小组检验某溶液中存在SO2-4时,首先加入Ba(NO3)2溶液,产生白色沉淀,然后加入过量稀硝酸,白色沉淀不溶解,由此得出结论:溶液中一定含有SO2-4.你认为该推理是否严密?试说明理由.
酸、碱、盐是化学工作者研究的重要领域,请回答下列各小题:
(1)某二元酸H2X的电离方程式是:H2X═H++HX-,HX-?X2-+H+.回答下列问题:
①KHX溶液显 (填“酸性”、“碱性”或“中性”).
②若0.1mol?L-1KHX溶液的pH=2,则0.1mol?L-1H2X溶液中氢离子的物质的量浓度 (填“<”、“>”或“=”)0.11mol?L-1,理由是 .
③0.01mol?L-1的HCl与0.02mol?L-1的KHX溶液等体积混合液中各离子浓度由大到小的顺序是 .
(2)在25℃下,向浓度均为0.1mol?L-1的FeCl3和AlCl3混合溶液中逐滴加入氨水,先生成 (填化学式)沉淀.已知25℃时
Ksp[Fe(OH)3]=2.6×10-39 mol4?L-4,KsP[Al(OH)3]=1.3×10-33 mol4?L-4.
(3)在25℃下,有pH=3的醋酸溶液和pH=11的氢氧化钠溶液,其中氢氧化钠溶液的物质的量浓度是 ,醋酸溶液的物质的量浓度 (填“>”、“<”、“=”)氢氧化钠溶液物质的量浓度.将上述两溶液等体积混合,反应后溶液显 (填“酸”、“碱”、“中”)性.
(4)某强酸性反应体系中,发生反应: X+ PbO2+ H2SO4= Pb(MnO4)2+ PbSO4+ H2O,已知X是一种硫酸盐,且0.2mol X在该反应中失去1mol 电子,则X的化学式是 .请将上述化学方程式配平,把系数填在各物质前的横线上.
查看习题详情和答案>>
(1)某二元酸H2X的电离方程式是:H2X═H++HX-,HX-?X2-+H+.回答下列问题:
①KHX溶液显
②若0.1mol?L-1KHX溶液的pH=2,则0.1mol?L-1H2X溶液中氢离子的物质的量浓度
③0.01mol?L-1的HCl与0.02mol?L-1的KHX溶液等体积混合液中各离子浓度由大到小的顺序是
(2)在25℃下,向浓度均为0.1mol?L-1的FeCl3和AlCl3混合溶液中逐滴加入氨水,先生成
Ksp[Fe(OH)3]=2.6×10-39 mol4?L-4,KsP[Al(OH)3]=1.3×10-33 mol4?L-4.
(3)在25℃下,有pH=3的醋酸溶液和pH=11的氢氧化钠溶液,其中氢氧化钠溶液的物质的量浓度是
(4)某强酸性反应体系中,发生反应: