网址:http://m.1010jiajiao.com/timu3_id_78602[举报]
向甲、乙两个容积均为1 L的恒容容器中,分别充入2 mol A、2 mol B和1 mol A、1 mol B。相同条件下(温度为T),发生下列反应:A(g)+B(g) xC(g) ΔH<0。测得两容器中c(A)随时间t的变化如图所示:
回答下列问题:
(1)乙容器中,平衡后物质B的转化率为 。
(2)x= 。
(3)下列说法正确的是( )
A.向平衡后的乙容器中充入氦气可使c(A)增大
B.将乙容器单独升温可使乙容器内各物质的体积分数与甲容器内的相同
C.若向甲容器中再充入2 mol A、2 mol B,则平衡时甲容器中0.78 mol·L-1<c(A)<1.56 mol·L-1
D.若甲容器为等压可变容器,向甲中充入惰性气体,则c(A)减小,平衡正向移动,v(正)、v(逆)减小
查看习题详情和答案>>
向甲、乙两个容积均为1 L的恒容容器中,分别充入2 mol A、2 mol B和1 mol A、1 mol B。相同条件下(温度为T),发生下列反应:A(g)+B(g)  xC(g) ΔH<0。测得两容器中c(A)随时间t的变化如图所示:
xC(g) ΔH<0。测得两容器中c(A)随时间t的变化如图所示:


回答下列问题:
(1)乙容器中,平衡后物质B的转化率为 。
(2)x= 。
(3)下列说法正确的是( )
A.向平衡后的乙容器中充入氦气可使c(A)增大
B.将乙容器单独升温可使乙容器内各物质的体积分数与甲容器内的相同
C.若向甲容器中再充入2 mol A、2 mol B,则平衡时甲容器中0.78 mol·L-1<c(A)<1.56 mol·L-1
D.若甲容器为等压可变容器,向甲中充入惰性气体,则c(A)减小,平衡正向移动,v(正)、v(逆)减小
查看习题详情和答案>>
向甲、乙两个容积均为1 L的恒容容器中,分别充入2 mol A,4 mol B和1 mol A,2 mol B。相同条件下,发生下列反应:A(g)+2B(g) xC(g) ΔH<0。测得两容器中c(A)随时间t的变化如图所示,下列说法正确的是 ( )
xC(g) ΔH<0。测得两容器中c(A)随时间t的变化如图所示,下列说法正确的是 ( )
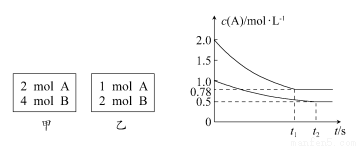
A.x可能等于3
B.向平衡后的乙容器中充入氦气可使A的转化率降低
C.将乙容器单独升温,c(A)可达到0.78 mol/L
D.若向甲容器中再充入2 mol A,4 mol B,平衡时甲容器中c(A)大于1.56 mol/L
查看习题详情和答案>>
 xC(g) ΔH<0。测得两容器中c(A)随时间t的变化如图所示,下列说法正确的是 ( )
xC(g) ΔH<0。测得两容器中c(A)随时间t的变化如图所示,下列说法正确的是 ( )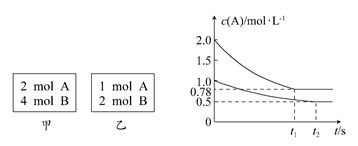
A.x可能等于3
B.向平衡后的乙容器中充入氦气可使A的转化率降低
C.将乙容器单独升温,c(A)可达到0.78 mol/L
D.若向甲容器中再充入2 mol A,4 mol B,平衡时甲容器中c(A)大于1.56 mol/L
|
向甲、乙两个容积均为1 L的恒容容器中,分别充入2 mol A、2 mol B和1 mol A、1 mol B.相同温度下,发生反应:A(g)+B(g)
| |
A. |
x不可能等于2 |
B. |
甲、乙两容器中反应达平衡时,平衡常数K(甲)<K(乙) |
C. |
将乙容器升温可使甲、乙容器内各物质的体积分数相同 |
D. |
若向甲容器中再充入2 mol A、2 mol B,则平衡时甲容器中0.78 mol/L<c(A)<1.56 mol/L |
