摘要:将2.3 g 钠在纯氧中完全燃烧得淡黄色固体Na2O2.该固体与足量的CO2气体充分反应.所生成的气体的质量为 A.0.16 g B.0.8 g C.0.48 g D.0.32 g
网址:http://m.1010jiajiao.com/timu3_id_73992[举报]
工业合成氨与制备硝酸一般可连续生产,流程如图:
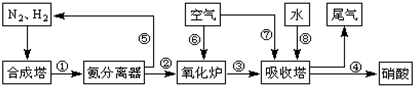
(1)工业生产时,制取氢气的一个反应为:CO(g)+H2O(g)?CO2(g)+H2(g).t℃时,往10L密闭容器中充入2mol CO和3mol水蒸气.反应建立平衡后,体系中c(H2)=0.12mol?L-1.则该温度下此反应的平衡常数K= (填计算结果).
(2)合成塔中发生反应N2(g)+3H2(g)?2NH3(g)△H<0.下表为不同温度下该反应的平衡常数.由此可推知,表中T1 300℃(填“>”、“<”或“=”).
(3)氨气在纯氧中燃烧生成一种单质和水,科学家利用此原理,设计成“氨气-氧气”燃料电池,则通入氨气的电极是 (填“正极”或“负极”);碱性条件下,该电极发生反应的电极反应式为 .
(4)用氨气氧化可以生产硝酸,但尾气中的NOx会污染空气.目前科学家探索利用燃料气体中的甲烷等将氮的氧化物还原为氮气和水,反应机理为:
CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(g)△H=-574kJ?mol-1
CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O(g)△H=-1160kJ?mol-1
则甲烷直接将NO2还原为N2的热化学方程式为 .
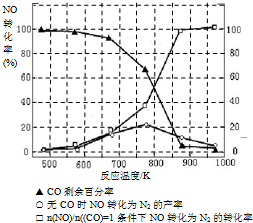
(5)某研究小组在实验室以“Ag-ZSM-5”为催化剂,测得将NO转化为N2的转化率随温度变化情况如下图.据图分析,若不使用CO,温度超过775℃,发现NO的转化率降低,其可能的原因为 ;在
=1的条件下,应控制的最佳温度在 左右.
 查看习题详情和答案>>
查看习题详情和答案>>

(1)工业生产时,制取氢气的一个反应为:CO(g)+H2O(g)?CO2(g)+H2(g).t℃时,往10L密闭容器中充入2mol CO和3mol水蒸气.反应建立平衡后,体系中c(H2)=0.12mol?L-1.则该温度下此反应的平衡常数K=
(2)合成塔中发生反应N2(g)+3H2(g)?2NH3(g)△H<0.下表为不同温度下该反应的平衡常数.由此可推知,表中T1
| T/℃ | T1 | 300 | T2 |
| K | 1.00×107 | 2.45×105 | 1.88×103 |
(4)用氨气氧化可以生产硝酸,但尾气中的NOx会污染空气.目前科学家探索利用燃料气体中的甲烷等将氮的氧化物还原为氮气和水,反应机理为:
CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(g)△H=-574kJ?mol-1
CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O(g)△H=-1160kJ?mol-1
则甲烷直接将NO2还原为N2的热化学方程式为
(5)某研究小组在实验室以“Ag-ZSM-5”为催化剂,测得将NO转化为N2的转化率随温度变化情况如下图.据图分析,若不使用CO,温度超过775℃,发现NO的转化率降低,其可能的原因为
| n(NO) |
| n(CO) |
 查看习题详情和答案>>
查看习题详情和答案>>
氨气是一种重要的化工产品,是生产铵盐、尿素等的原料.工业合成氨的反应如下:
N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ?mol-1.
(1)实验室中常用来制备氨气的化学方程式为 .
(2)已知H2(g)的燃烧热为285.8kJ?mol-1,写出NH3(g)在纯氧中燃烧生成无毒、无害物质的热化学方程式 .
(3)25℃时,将a mol (NH4)2SO4溶于水,向该溶液中滴加V L稀氨水后溶液呈中性,则滴加氨水的过程中水的电离平衡将 (填“正向”、“不”或“逆向”)移动,所滴加稀氨水的物质的量浓度为 mol?L-1.(25℃时,NH3?H2O的电离平衡常数Kb≈2×10-5).
(4)工业上常用CO2和NH3通过如下反应合成尿素[CO(NH2)2].
CO2(g)+2NH3(g)
CO(NH2)2(l)+H2O(g)△H<0,t℃时,向容积恒定为2L的密闭容器中加入0.10mol CO2和0.40mol NH3,70min开始达到平衡.反应中CO2(g)的物质的量随时间变化如下表所示:
①20min时v正(CO2) 80min时v逆(H2O)(填“>”、“=”或“<”).
②在100min时,保持其它条件不变,再向容器中充入0.050mol CO2和0.20mol NH3,重新建立平衡后CO2的转化率与原平衡相比将 (填“增大”、“不变”或“减小”).
③根据表中数据在图甲中绘制出在t℃下NH3的转化率随时间变化的图象;保持其它条件不变,则(t+10)℃下正确的图象可能是 (填图甲中的“A”或“B”).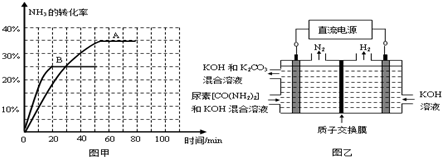
④图乙所示装置(阴、阳极均为惰性电极)可用于电解尿素[CO(NH2)2]的碱性溶液制取氢气.该装置中阳极的电极反应式为 ,若两极共收集到气体22.4L(标况),则消耗的尿素为 g(忽略气体的溶解).
查看习题详情和答案>>
N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ?mol-1.
(1)实验室中常用来制备氨气的化学方程式为
(2)已知H2(g)的燃烧热为285.8kJ?mol-1,写出NH3(g)在纯氧中燃烧生成无毒、无害物质的热化学方程式
(3)25℃时,将a mol (NH4)2SO4溶于水,向该溶液中滴加V L稀氨水后溶液呈中性,则滴加氨水的过程中水的电离平衡将
(4)工业上常用CO2和NH3通过如下反应合成尿素[CO(NH2)2].
CO2(g)+2NH3(g)
| 一定条件 |
| 时间/min | 0 | 30 | 70 | 80 | 100 |
| n(CO2)/mol | 0.10 | 0.060 | 0.040 | 0.040 | 0.040 |
②在100min时,保持其它条件不变,再向容器中充入0.050mol CO2和0.20mol NH3,重新建立平衡后CO2的转化率与原平衡相比将
③根据表中数据在图甲中绘制出在t℃下NH3的转化率随时间变化的图象;保持其它条件不变,则(t+10)℃下正确的图象可能是

④图乙所示装置(阴、阳极均为惰性电极)可用于电解尿素[CO(NH2)2]的碱性溶液制取氢气.该装置中阳极的电极反应式为
.(8分)某仅由碳、氢、氧三种元素组成的有机化合物,经测定其相对分子质量为90。取有机物样品1.8 g,在纯氧中完全燃烧,将产物先后通过浓硫酸和碱石灰,两者分别增重1.08 g和2.64 g。试求该有机物的分子式。
查看习题详情和答案>>