摘要:常温下将c1 mol/L V1 mL的氨水滴加到c2 mol/L V2 mL的盐酸中.下列结论正确的是( ) A.若混合溶液的pH=7.则c1V1>c2V2 B.若V1=V2.c1=c2.则混合液中c(NH4+)=c(Cl-) C.若混合溶液的pH=7.则混合液中c(NH4+)>c(Cl-) D.若V1=V2.且混合溶液的pH<7.则一定有c1<c2 [解析]选A.A项.若混合溶液的pH=7.则氨水稍过量.c1V1>c2V2,B项.若V1=V2.c1=c2则氨 水与盐酸恰好完全反应.混合液中溶质为NH4Cl. c(Cl-)>c(NH4+),C项.若混合溶液的pH=7.由 电荷守恒知.c(NH4+)=c(Cl-),D项.混合溶液的pH<7.溶质可能是NH4Cl或NH4Cl和HCl.可能 c1=c2或 c1<c2.
网址:http://m.1010jiajiao.com/timu3_id_71615[举报]
常温下将c1 mol·L-1 V1 mL的氨水滴加到c2 mol·L-1 V2 mL的盐酸中,下列结论正确的是
A.若混合溶液的pH=7,则c1·V1> c2·V2
B.若V1=V2,c1=c2,则混合溶液中c(![]() )=c(Cl-)
)=c(Cl-)
C.若混合溶液的pH=7,则混合溶液中c(![]() )>c(Cl-)
)>c(Cl-)
D.若V1=V2,且混合液的pH<7,则一定有c1<c2
查看习题详情和答案>>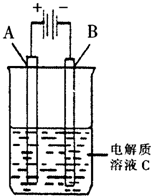 (2011?丹东模拟)肼(N2H4)又称联氨,是一种可燃性液体,其燃烧热较大且燃烧产物对环境无污染,故可以用作火箭燃料.
(2011?丹东模拟)肼(N2H4)又称联氨,是一种可燃性液体,其燃烧热较大且燃烧产物对环境无污染,故可以用作火箭燃料.(1)已知:N2(g)+2O2(g)=2NO2(g)△H=+67.7kJ/mol,2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g)△H=一1135.7kJ/mol.则肼完全燃烧的热化学方程式为
N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=-534kJ/mol
N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=-534kJ/mol
.(2)肼--空气燃料电池是一种碱性燃料电池,电解质溶液是20%-30%的KOH溶液.该电池放电时,正极的电极反应式是
O2+2H2O+4e-=4OH-
O2+2H2O+4e-=4OH-
,电池工作一段时间后,电解质溶液的pH将减小
减小
(填“增大”、“减小”、“不变”).(3)如图是一个电化学装置示意图.用肼--空气燃料电池做此装置的电源.
①如果A为含有锌、银、金三种杂质的粗铜,B为纯铜,C为CuSO4.该装置的实际意义是
精炼粗铜
精炼粗铜
.②如果A是铂电极,B是石墨电极,C是AgNO3溶液,若B极增重10.8g,该燃料电池理论上消耗
0.025
0.025
molN2H4.(4)肼易溶于水,它是与氨类似的弱碱,用电离方程式表示肼的水溶液显碱性的原因
N2H4+H2O N2H+5+OH-;N2H+5+H2O
N2H+5+OH-;N2H+5+H2O N2H+6+OH-
N2H+6+OH-
 N2H+5+OH-;N2H+5+H2O
N2H+5+OH-;N2H+5+H2O N2H+6+OH-
N2H+6+OH-N2H4+H2O N2H+5+OH-;N2H+5+H2O
N2H+5+OH-;N2H+5+H2O N2H+6+OH-
N2H+6+OH-
. N2H+5+OH-;N2H+5+H2O
N2H+5+OH-;N2H+5+H2O N2H+6+OH-
N2H+6+OH-(5)常温下将0.2mol/L HCl溶液与0.2mol/L N2H4?H2O溶液等体积混合(忽略混合后溶液体积的变化),若测得混合溶液的pH=6,则混合溶液中由水电离出的c(H+)
大于
大于
0.1mol/LHCl溶液中由水电离出的c(H+)(填“大于”、“小于”、或“等于”).(6)已知:在相同条件下N2H4?H2O的电离程度大于N2H5C1的水解程度.常温下,若将0.2mol/L N2H4?H2O溶液与0.1mol/L HCl溶液等体积混合,则溶液中N2H-5、Cl-、OH-、H+离子浓度南大到小的顺序为
c(N2H+5)>c(Cl-)>c(OH-)>c(H+)
c(N2H+5)>c(Cl-)>c(OH-)>c(H+)
. 肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料.
肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料.(1)已知在25℃,101kPa时,16.0g N2H4在氧气中完全燃烧生成氮气,放出热量312kJ,N2H4完全燃烧反应的热化学方程式是
N2H4(l)+O2(g)=N2(g)+2H2O(l)△H=-624KJ/mol
N2H4(l)+O2(g)=N2(g)+2H2O(l)△H=-624KJ/mol
.肼-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液.肼-空气燃料电池放电时,负极的电极反应式是:N2H4+4OH--4e-=4H2O+N2
N2H4+4OH--4e-=4H2O+N2
.电池工作一段时间后,电解质溶液的pH将减小
减小
(填“增大”、“减小”、“不变”).(2)如图是一个电化学装置示意图.用肼--空气燃料电池做此装置的电源.如果A是铂电极,B是石墨电极,C是500mL足量的饱和氯化钠溶液,当两极共产生1.12L气体时,溶液的pH为
13
13
,则肼-空气燃料电池理论上消耗的空气1.4
1.4
L(气体体积在标准状况下测定,假设空气中氧气体积分数为20%)(3)肼易溶于水,它是与氨类似的弱碱,用电离方程式表示肼的水溶液显碱性的原因
N2H4+H2O=N2H5++OH-;N2H5++H2O=N2H62++OH-
N2H4+H2O=N2H5++OH-;N2H5++H2O=N2H62++OH-
.(4)常温下将0.2mol/L HCl溶液与0.2mol/L N2H4?H2O溶液等体积混合(忽略混合后溶液体积的变化),若测得混合溶液的pH=6,则混合溶液中由水电离出的c(H+)
大于
大于
0.1mol/L HCl溶液中由水电离出的c(H+)(填“大于”、“小于”、或“等于”).(5)已知:在相同条件下N2H4?H2O的电离程度大于N2H5C1的水解程度.常温下,若将0.2mol/L N2H4?H2O溶液与0.1mol/L HCl溶液等体积混合,则溶液中N2H+5、Cl-、OH-、H+离子浓度由大到小的顺序为
c(N2H5+)>c(Cl-)>c(OH-)>c(H+)
c(N2H5+)>c(Cl-)>c(OH-)>c(H+)
.