网址:http://m.1010jiajiao.com/timu3_id_70709[举报]
| |||||||||||||||||||||||||||||
 373 K时,某1 L密闭容器中发生如下可逆反应:A (g)
373 K时,某1 L密闭容器中发生如下可逆反应:A (g)2B (g)。其中物质B的物质的量变化如右图所示。
(1)已知373 K时60 s达到平衡,则前60s内A的平均反应速率为 。
(2)该反应的平衡常数表达式为 。
(3)若在此平衡体系中再加入amol的A,反应速率
(填“增大”或“减小”,下同),平衡时A的转化率 。A的平衡浓度 。
(4)若373 K时B的平衡浓度为A的2倍,473 K时(其他条件不变),B的平衡浓度为A的3倍,该反应的正反应为 (填“放热反应”或 “吸热反应”),为使该反应的平衡常数变小,可以采取的措施是 。
a.升高温度 b.扩大容器的体积
c.降低温度 d.将B从体系中抽走
(4)若反应在373K进行,在甲、乙两容器都为1 L密闭容器,分别加入1 mol B;1 mol B、0.2 mol He,达到平衡时B的转化率应 。
a.甲>乙 b.乙>甲 c.甲=乙 d.无法确定
查看习题详情和答案>>
373K时,某1 L密闭容器中加入1 mol NH3发生如下可逆反应:
2NH3(g)![]() N2(g)+3H2(g).其中物质H2的物质的量变化如下图所示.
N2(g)+3H2(g).其中物质H2的物质的量变化如下图所示.

(1)前20 s内NH3(g)的平均反应速率为________
(2)373K时该反应的平衡常数的值为________
(3)若在此平衡体系中再加入1 mol的NH3,与原平衡比较,新平衡时NH3的转化率________(填“增大”或“减小”,下同).NH3的平衡浓度________.
(4)将原平衡升温至473K,重新达平衡时(其他条件不变),H2的平衡浓度为NH3的2倍,该反应的正反应为(填“放热反应”或“吸热反应”)________,为增大平衡体系中H2的物质的量,下列措施正确的是(其它条件相同)________
a.升高温度
b.扩大容器的体积
c.加入合适的催化剂
d.再充入N2
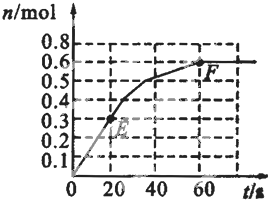 373K时,某1L密闭容器中发生如下可逆反应:A (g)?2B (g).其中物质B的物质的量变化如图所示
373K时,某1L密闭容器中发生如下可逆反应:A (g)?2B (g).其中物质B的物质的量变化如图所示(1)已知373K时60s达到平衡,则前60s内A的平均反应速率为
(2)若373K时B的平衡浓度为A的3倍,473K时(其他条件不变),B的平衡浓度为A的2倍,请在上图中画出473K时A的物质的量随时间的变化曲线.
(3)若反应在373K进行,在1L密闭容器中加入1mol B、0.2mol He,达到平衡时B的转化率应
A.等于60% B.等于40% C.小于40% D.介于40%~60%之间
(4)已知曲线上任意两点之间边线的斜率表示该时段内B的平均反应速率(例如直线EF的斜率表示20s~60s内B的平均反应速率),试猜想曲线上任意一点的切线斜率的意义
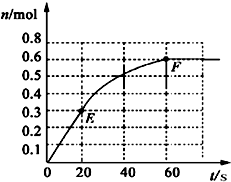 373K时,某1L密闭容器中加入1molPCl5发生如下可逆反应:
373K时,某1L密闭容器中加入1molPCl5发生如下可逆反应:PCl5 (g)
 PCl3(g)+Cl2 (g).其中物质PCl3的物质的量变化如右图所示.
PCl3(g)+Cl2 (g).其中物质PCl3的物质的量变化如右图所示.(1)前20s内PCl5(g)的平均反应速率为
(2)373K时该反应的平衡常数的值为
(3)若在此平衡体系中再加入1mol的PCl5,与原平衡比较,新平衡时PCl5的转化率
(4)将原平衡升温至473K,重新达平衡时(其他条件不变),PCl3的平衡浓度为PCl5的3倍,该反应的正反应为
a.升高温度 b.扩大容器的体积
c.加入合适的催化剂 d.再充入PCl3.
