网址:http://m.1010jiajiao.com/timu3_id_69559[举报]
阅读分析材料,据此完成下列要求。
工业纯碱中常含有少量的NaCl和NaOH。某校课外活动小组的同学为测定纯碱样品中
Na2CO3的质量分数,选择下列适当装置进行连接,并对设计方案不断完善,成功完成了
测定实验。
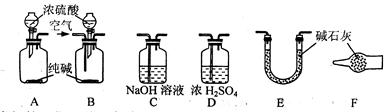 |
⑴活动小组的五位同学对实验装置的设计进行了讨论发言,内容如下:
甲:将装置A和E连接即可。因为Na2CO3与稀硫酸反应生成的CO2被E中的碱石灰吸收,分别测量反应前和反应后E的总质量,就可求出Na2CO3的质量分数。
乙:还应在A和E之间连接装置 (填序号),其目的是 。
丙:应该用B装置取代A装置。从B装置的导管口处缓慢鼓入空气,其目的是 。
丁:若直接向B装置中鼓入空气会导致实验测定结果 (填“偏高”、“偏低”或
“无影响”),因此,应将鼓入的空气先通过装置 (填序号)。
戊:E装置后还应连接装置F,其作用是 。
⑵学生课外活动小组测定的数据如下,计算该工业纯碱中Na2CO3的质量分数为 。
| 工业纯碱样品质量 | 反应前E的总质量 | 反应后E的总质量 |
| 6.4g | 51.9g | 54.1g |
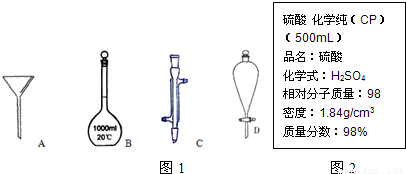
(1)写出图1序号所代表的仪器的名称:B______;C______;D______.
(2)图2是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.
现用该浓硫酸配制100mL 1mol/L的稀硫酸.可供选用的仪器有:①胶头滴管;②烧瓶;③烧杯;④药匙;⑤量筒;⑥托盘天平.
请回答下列问题:
Ⅰ配制稀硫酸时,上述仪器中不需要使用的有______(选填序号),还缺少的仪器有______(写仪器名称);
Ⅱ经计算,该浓硫酸的物质的量浓度为______mol/L.配制100mL1mol/L的稀硫酸需要用量筒量取上述浓硫酸的体积为______mL(保留一位小数),量取浓硫酸时应选用______(选填①10mL、②50mL、③100mL)规格的量筒;
Ⅲ用胶头滴管往容量瓶中加水时,不小心液面超过了刻度,处理的方法是______(填序号);
A.吸出多余液体,使凹液面与刻度线相切
B.小心加热容量瓶,经蒸发后,使凹液面与刻度线相切
C.经计算加入一定量的浓盐酸
D.重新配制
Ⅳ用该浓硫酸配制100mL1mol/L稀硫酸的正确顺序是______;
A.冷却 B.量取 C.洗涤 D.定容 E.溶解 F.摇匀 G.移液
Ⅴ将所配制的稀硫酸进行测定,发现浓度大于1mol/L.请你分析配制过程中可能引起该误差的原因是(填序号)______;
①容量瓶不干燥,含有少量蒸馏水 ②定容时俯视刻度线 ③定容时仰视刻度线
④未冷却至室温就转移到容量瓶中 ⑤没有洗涤烧杯和玻璃棒
Ⅵ请写出“定容”的具体操作:______.
查看习题详情和答案>>
某研究性小组借助A~D的仪器装置完成有关实验.

[实验一]收集NO气体
(1)用装置A收集NO气体,正确的操作是________(填序号)
a.从①口进气,用排水法集气
b.从①口进气,用排气法集气
c.从②口进气,用排水法集气
d.从②口进气,用排气法集气
[实验二]为了探究镀锌薄铁板上的锌的质量分数ω(Zn)和镀层厚度,查询得知锌易溶于强碱:Zn+2NaOH![]() Na2ZnO2+H2↑,据此,截取面积为S的双面镀锌薄铁板试样,剪碎、称得质量为m1g.用固体烧碱和水作试剂,拟出下列实验方案并进行相关实验.
Na2ZnO2+H2↑,据此,截取面积为S的双面镀锌薄铁板试样,剪碎、称得质量为m1g.用固体烧碱和水作试剂,拟出下列实验方案并进行相关实验.
方案甲:通过测量试样与碱反应生成的氢气体积来实现探究目标.
(2)选用B和________(填仪器标号)两个装置进行实验.
(3)测得充分反应后生成氢气的体积为V L(标准状况),则ω(Zn)=________.
(4)计算镀层厚度,还需要检索的一个物理量是________.
(5)若将装置B的恒压分液漏斗改为普通分泌漏斗,测量结果将________(填“偏大”“偏小”或“无影响”).
方案乙:通过称量试样与碱反应前后的质量实现探究目标.选用仪器C做实验,试样经充分反应,滤出不溶物、洗涤、烘干,称得其质量为m2g.
(6)ω(Zn)=________.
方案丙:通过称量试样与碱反应前后仪器、试样和试剂的总质量(其差值即为H2的质量)实现探究目标.实验同样使用仪器C.
(7)从实验误差角度分析,方案丙________(填“优于”“劣于”或“等同于”)方案乙.
“套管实验”是将一支较小的玻璃仪器装入另一玻璃仪器中,经组装来完成原来需要两只或更多普通玻璃仪器进行的实验.因其具有许多优点,近年被广泛开发并应用于化学实验中.下述两个实验均为“套管实验”,请观察实验装置,分析实验原理,并回答下列问题:
实验一:如图甲,小试管内塞有沾有无水硫酸铜粉末的棉花球.

(1)从点燃酒精灯开始,试管及烧杯A、B中能观察到的现象有________.
(2)整个实验结束时,在操作上需要特别注意的问题是________.
(3)通过该实验可以得出的结论是________.
实验二:在氨气的喷泉实验中,将圆底烧瓶集满氨气的操作很麻烦.请设计一个简单的操作方法,用图乙仪器,并选用下列药品:A.氯化铵固体、B.氢氧化钠固体、C.浓氨水、D.浓硫酸、E.湿润的红色石蕊试纸,采用“套管法”在圆底烧瓶中集满喷泉实验用的氨气.
(4)所用的试剂为(填写编号):________.
(5)请简述所设计的操作及判断烧瓶集已满氨气的方法:________.
(6)将上述两个实验与普通实验相比较,“套管实验”明显具备的优点是:________.
查看习题详情和答案>>“套管实验”是将一支较小的玻璃仪器装入另一玻璃仪器中,经组装来完成原来需要两只或更多普通玻璃仪器进行的实验.因其具有许多优点,近年被广泛开发并应用在化学实验中.下列两个实验均为“套管实验”请观察实验装置,分析实验原理,回答下列问题:

实验一:如图甲,小试管内塞有沾有无水硫酸铜粉末的棉花球.
(1)从点燃酒精灯开始,试管及烧杯A、B中能观察到的现象有________
(2)整个实验结束时,在操作上需要特别注意的问题是________
(3)通过该实验可以得到的结论是________.
实验二:在氨的喷泉实验中,将圆底瓶集满氨气的操作很麻烦.请设计一个简单的操作方法,只有一支试管(如图乙),选用下列药品:
A.氯化铵固体 B.氢氧化钠固体 C.浓氨水
D.浓硫酸 E.湿润的红色石蕊试纸
采用“套管法”在圆底烧瓶中集满喷泉实验用的氨气.
(4)所用的试剂为________
(5)请简述所设计的操作及判定集满氨气的现象________
(6)产生氨气的化学方程式为________.
(7)将上述两个实验与普通实验相比较.“套管实验”明显具备的优点是________.
查看习题详情和答案>>