摘要:9.若取100 g混合物.则m(Mg2+)=62.4 g.设N元素为x g.则O元素为100-62.4-x g, 根据化合价守恒有:2×62.4/24=3x/14+2×/16.解得x=5.6 g.则N%=5.6%.
网址:http://m.1010jiajiao.com/timu3_id_68451[举报]
用NaOH(s)、水、大理石和盐酸制取33 g纯NaHCO3。请参照物质的溶解度表回答下列问题:
(1)写出制取过程中反应的化学方程式。
(2)若提供100 g水,则需NaOH的物质的量为多少?
(3)简述实验的操作过程。
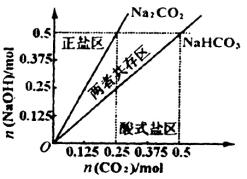
(4)在右图中反映上述实验过程的图象中,标出A点(即当![]() =
=![]() 且n(
且n(![]() )=)0.125 mol时)的位置,并判断此时所得盐的组成及其物质的量。
)=)0.125 mol时)的位置,并判断此时所得盐的组成及其物质的量。
查看习题详情和答案>>
用NaOH(s)、水、大理石和盐酸制取33 g纯NaHCO3。
请参照物质的溶解度表回答下列问题:
(1)写出制取过程中反应的化学方程式。
(2)若提供100 g水,则需NaOH的物质的量为多少?
(3)简述实验的操作过程。
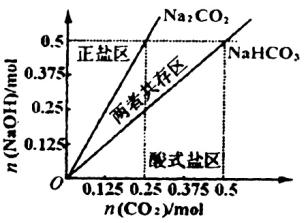
(4)在右图中反映上述实验过程的图象中,标出A点(即当![]() =
=![]() ,且n(
,且n(![]() )=0.125 mol时)的位置,并判断此时所得盐的组成及其物质的量。
)=0.125 mol时)的位置,并判断此时所得盐的组成及其物质的量。
查看习题详情和答案>>
用NaOH(s)、水、大理石和盐酸制取33 g纯NaHCO3。
请参照物质的溶解度表回答下列问题:
(1)写出制取过程中反应的化学方程式。
(2)若提供100 g水,则需NaOH的物质的量为多少?
(3)简述实验的操作过程。
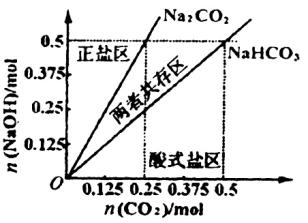
(4)在右图中反映上述实验过程的图象中,标出A点(即当![]() =
=![]() ,且n(
,且n(![]() )=0.125 mol时)的位置,并判断此时所得盐的组成及其物质的量。
)=0.125 mol时)的位置,并判断此时所得盐的组成及其物质的量。
查看习题详情和答案>>
 工业生产的纯碱中常含有少量的NaCl杂质.某校研究性学习活动小组为了测定混合物中纯碱的质量分数,拟使用如图实验装置(说明:连接甲和乙的橡皮管有铁夹控制),先测定一定量的样品和酸反应放出二氧化碳的质量,再计算混合物中纯碱的质量分数.
工业生产的纯碱中常含有少量的NaCl杂质.某校研究性学习活动小组为了测定混合物中纯碱的质量分数,拟使用如图实验装置(说明:连接甲和乙的橡皮管有铁夹控制),先测定一定量的样品和酸反应放出二氧化碳的质量,再计算混合物中纯碱的质量分数.(1)甲装置的作用是
吸收空气中的二氧化碳
吸收空气中的二氧化碳
;丙装置的作用是吸收二氧化碳中的水蒸气
吸收二氧化碳中的水蒸气
.(2)乙装置反应完成后,打开甲和乙之间的铁夹,通数分钟空气的作用是
排出装置中的二氧化碳气体,使之都被丁处碱石灰完全吸收
排出装置中的二氧化碳气体,使之都被丁处碱石灰完全吸收
.写出甲装置中发生反应的离子方程式(NaOH溶液足量):CO2+2OH-=CO32-+H2O
CO2+2OH-=CO32-+H2O
.(3)若去掉戊装置,测得的CO2质量会
偏大
偏大
(填“偏大”或“偏小”).(4)若取n g样品装入广口瓶,且反应前填满碱石灰的干燥管丁总质量为m g,实验结束后称得干燥管丁的总质量为w,则Na2CO3质量分数的计算式为
| 53(w-m) |
| 22n |
| 53(w-m) |
| 22n |
