摘要:实验1:把2cm×5cm的铝箔的一端固定在粗铁丝上.另一端裹一根火柴.点燃火柴.待火柴快燃尽时.立即把铝箔伸入盛有氧气的集气瓶中.观察现象. 现象与解释:铝箔在氧气中剧烈燃烧.放出大量的热和耀眼的白光.反应生成Al2O3. 实验2:在两支试管里分别加入10mL浓NaOH溶液.在各放入一小段铝片和镁条.观察实验现象.过一段时间后.用点燃的木条分别放在两支试管口.有什么现象发生. 现象与解释:镁不能与NaOH溶液反应.铝能反应.并放出一种可燃性气体--氢气.同时生成NaAlO2. 实验3:把点燃的镁条放入盛有二氧化碳的集气瓶里.观察现象. 现象与解释:镁条在二氧化碳里剧烈燃烧.生成白色粉末.在瓶的内壁有黑色的碳附着. 实验4:用两张圆形滤纸分别叠成漏斗状.套在一起.使四周都有四层.把内层滤纸取出.再底部剪一个孔.用水润湿.再跟另一纸漏斗套在一起.架在铁圈上.下面放置盛沙的蒸发皿.把5g炒干的氧化铁粉末和2g铝粉混合均匀.放在纸漏斗上.上面加少量氯酸钾并在混合物中间插一根镁条.用小木条点燃镁条.观察发生的现象. 现象与解释:镁条剧烈燃烧.放出一定的热量.使氧化铁粉末和铝粉在较高温度下发生剧烈反应.反应放出大量的热.并放出耀眼的光芒.纸漏斗的下部被烧穿.有熔融物落入沙中.该反应生成了Al2O3和Fe.被称为铝热反应. 实验5:在试管里加入少量稀的Al2(SO4)3溶液.滴加氨水.生成白色胶状沉淀.继续滴加氨水.直到不再产生沉淀为止.过滤.用蒸馏水冲洗沉淀.可得较纯净的Al(OH)3.取少量Al(OH)3沉淀放在蒸发皿中.加热. 现象与解释:生成的白色胶状沉淀是Al(OH)3.Al(OH)3分解生成Al2O3和H2O. 实验6:把上述“实验5 中制得的Al(OH)3沉淀分装在2支试管里.往一个试管里滴加2mol/L 盐酸.往另一个试管里滴加2mol/L NaOH溶液.边加边振荡. 现象与解释:在酸或强碱里都能溶解.Al(OH)3是典型的两性氢氧化物.能与酸反应生成铝盐.与强碱反应生成偏铝酸盐.
网址:http://m.1010jiajiao.com/timu3_id_67284[举报]
下面是某课外活动小组在进行探究乙醇性质实验时遇到的问题,请你帮助解决.
(1)在做乙醇与钠反应的实验时,把一小块钠缓慢放入装有乙醇的试管内,与钠和水反应相比有所不同:钠没有熔化成小球;钠先沉在试管底;反应后逐渐浮起.小组同学进行讨论,前两点现象解释达成共识.请说出你的看法.
钠没有熔化成小球,因为
第三点现象解释存在争议,活动小组的同学形成两种意见:a生成的氢气产生浮力所致;b生成的乙醇钠增大了溶液的密度所致.请你设计一个实验验证a和b说法的合理性.
(2)在做乙醇的催化氧化实验中,某同学有个意外发现:在酒精灯外焰灼烧铜丝观察到铜丝表面变黑;当铜丝接近灯芯,变黑的铜丝又恢复原来的红色.请用化学方程式解释上述变化过程.
查看习题详情和答案>>
(1)在做乙醇与钠反应的实验时,把一小块钠缓慢放入装有乙醇的试管内,与钠和水反应相比有所不同:钠没有熔化成小球;钠先沉在试管底;反应后逐渐浮起.小组同学进行讨论,前两点现象解释达成共识.请说出你的看法.
钠没有熔化成小球,因为
钠与乙醇反应不如与水反应剧烈,放出热量少,温度没有达到钠的熔点
钠与乙醇反应不如与水反应剧烈,放出热量少,温度没有达到钠的熔点
;钠先沉在试管底,因为钠的密度比水小比乙醇大,因而沉到试管底
钠的密度比水小比乙醇大,因而沉到试管底
第三点现象解释存在争议,活动小组的同学形成两种意见:a生成的氢气产生浮力所致;b生成的乙醇钠增大了溶液的密度所致.请你设计一个实验验证a和b说法的合理性.
向完成实验的试管中再缓慢加入一小块钠,观察钠是浮在液面还是沉下去.
向完成实验的试管中再缓慢加入一小块钠,观察钠是浮在液面还是沉下去.
(2)在做乙醇的催化氧化实验中,某同学有个意外发现:在酒精灯外焰灼烧铜丝观察到铜丝表面变黑;当铜丝接近灯芯,变黑的铜丝又恢复原来的红色.请用化学方程式解释上述变化过程.
2Cu+O2
2CuO; CuO+CH3CH2OH
CH3CHO+H2O+Cu.
| ||
| △ |
2Cu+O2
2CuO; CuO+CH3CH2OH
CH3CHO+H2O+Cu.
.
| ||
| △ |
硫酸亚铁是一种可用于治疗缺铁性贫血的药剂.硫酸亚铁药片外表包有一层特制的糖衣,以保护硫酸亚铁不被空气中的氧气氧化成硫酸铁(硫酸铁无治疗贫血的药效).
(1)请完成硫酸亚铁在硫酸酸化的条件下与空气中的氧气反应的离子方程式:
Fe2+ O2+ H+-- Fe3++ H2O 反应中的氧化剂是 (填化学式).
(2)试设计一个实验方案,探究某硫酸亚铁药片是否被氧化.请在答题卡的表格中(可以不填满,表格不够时也可自行添加)写出实验步骤以及预期现象和结论.
限选实验试剂:0.1moL?L-1 KSCN、氯水.
(3)步骤2的离子方程式为 .
查看习题详情和答案>>
(1)请完成硫酸亚铁在硫酸酸化的条件下与空气中的氧气反应的离子方程式:
(2)试设计一个实验方案,探究某硫酸亚铁药片是否被氧化.请在答题卡的表格中(可以不填满,表格不够时也可自行添加)写出实验步骤以及预期现象和结论.
限选实验试剂:0.1moL?L-1 KSCN、氯水.
| 实验步骤 | 预期现象和结论 |
| 步骤1:把药品刮去糖衣,用研钵研碎;取少量研碎的粉末在试管中,用少量的蒸馏水溶解; | 硫酸亚铁在蒸馏水中溶解. |
| 步骤2: |
|
| 步骤3: |
乙醛能与银氨溶液反应析出银.如果条件控制适当,析出的银会均匀地分布在试管壁上,形成光亮的银镜,这个反应又叫银镜反应.银镜的光亮程度与反应条件有关.某课外活动小组同学在课外活动中对乙醛的银镜反应进行了探究.
Ⅰ.探究银镜反应的最佳实验条件部分实验数据如下表:
请回答下列问题:
(1)读表若只进行实验1和实验3,其探究目的是 .
(2)推理当银氨溶液的量为1mL,乙醛的量为3滴,水浴温度为40℃,反应混合液pH为11时,出现银镜的时间是 ;要探索不同水浴温度下乙醛进行银镜反应的最佳条件,除了测量银镜出现的时间外,还需要比较不同条件下形成的银镜的 .
(3)进一步实验 若还要探索银氨溶液的用量对出现银镜快慢的影响,如何进行实验?
.
Ⅱ.探究对废液的回收处理:
银氨溶液放久后会变成氮化银而引起爆炸,直接排放会污染环境,且造成银资源的浪费.通过查找资料,已知从银氨溶液中提取银的一种实验流程为:
操作④的方法是:把Ag2S和铁粉放到烧杯中加浓盐酸搅拌煮沸,使Ag2S变成银粉.反应的化学方程式为:Ag2S+Fe+2HCl
2Ag+FeCl2+H2S↑
(4)若获得的银粉中含有少量没有反应完的铁粉,除去铁的反应的离子方程式为: ,需要用到的玻璃仪器有 (填编号).
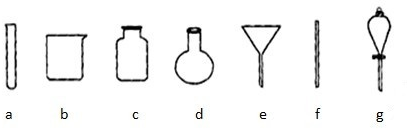
(5)操作④应在(填实验室设备名称) 中进行.
(6)要洗去试管壁上的银镜,采用的试剂是 (填名称).
查看习题详情和答案>>
Ⅰ.探究银镜反应的最佳实验条件部分实验数据如下表:
| 实验变量 实验序号 |
银氨溶液 /mL |
乙醛的量 /滴 |
水液温度/℃ | 反应混合液的PH | 出现银镜时间/min |
| 1 | 1 | 3 | 65 | 11 | 5 |
| 2 | 1 | 3 | 45 | 11 | 6.5 |
| 3 | 1 | 5 | 65 | 11 | 4 |
| 4 | 1 | 3 | 30 | 11 | 9 |
| 5 | 1 | 3 | 50 | 11 | 6 |
| 6 | 1 | 5 | 80 | 11 | 3 |
(1)读表若只进行实验1和实验3,其探究目的是
(2)推理当银氨溶液的量为1mL,乙醛的量为3滴,水浴温度为40℃,反应混合液pH为11时,出现银镜的时间是
(3)进一步实验 若还要探索银氨溶液的用量对出现银镜快慢的影响,如何进行实验?
Ⅱ.探究对废液的回收处理:
银氨溶液放久后会变成氮化银而引起爆炸,直接排放会污染环境,且造成银资源的浪费.通过查找资料,已知从银氨溶液中提取银的一种实验流程为:
| 银氨溶液 | 加(NH4)2S ① |
过滤、洗涤 ② |
烘干 ③ |
Ag2S沉淀 | 铁粉还原 ④ |
银 粉 |
| ||
(4)若获得的银粉中含有少量没有反应完的铁粉,除去铁的反应的离子方程式为:

(5)操作④应在(填实验室设备名称)
(6)要洗去试管壁上的银镜,采用的试剂是
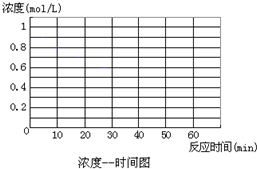 某化学反应2A(g)B (g)+D(g)在不同条件下进行,B、D的起始浓度为0,把反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表所示.
某化学反应2A(g)B (g)+D(g)在不同条件下进行,B、D的起始浓度为0,把反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表所示.实验序号 |
时间 浓度 温度/℃ |
0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 1 | 800 | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800 | 1.0 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 820 | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
| 4 | 760 | 1.0 |
(1)与实验1相比,实验2的反应速率更快,其原因可能是
(2)根据实验1和实验3的数据分析升温对该反应的影响,写出两条结论:①
②
(3)实验4只改变温度,其它条件不变.请在答题卡的相应位置画出实验1和实验4的“反应物A浓度-时间”关系曲线.
 (2013?红桥区二模)为减小CO2对环境的影响,在限制其排放量的同时,应加强对CO2创新利用的研究.
(2013?红桥区二模)为减小CO2对环境的影响,在限制其排放量的同时,应加强对CO2创新利用的研究.(1)①把含有较高浓度CO2的空气通入饱和K2CO3溶液.
②在①的吸收液中通高温水蒸气得到高浓度的CO2气体.
写出②中反应的化学方程式
2KHCO3
K2CO3+H2O+CO2↑
| ||
2KHCO3
K2CO3+H2O+CO2↑
.
| ||
(2)如将CO2与H2 以1:3的体积比混合.
①适当条件下合成某烃和水,该烃是
B
B
(填序号).A.烷烃 B.烯烃 C.炔烃 D.苯的同系物
②适当条件下合成燃料甲醇和水.在体积为2L的密闭容器中,充入 2mol CO2和6mol H2,一定条件下发生反应:
CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ/mol.
测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示.
从反应开始到平衡,v(H2)=
0.225mol/(L?min)
0.225mol/(L?min)
;氢气的转化率=75%
75%
;能使平衡体系中n(CH3OH)增大的措施有降低温度(或加压或增大H2的量等)
降低温度(或加压或增大H2的量等)
.(3)如将CO2与H2 以1:4的体积比混合,在适当的条件下可制得CH4.已知:
CH4 (g)+2O2(g)═CO2(g)+2H2O(l)△H1=-890.3kJ/mol
H2(g)+1/2O2(g)═H2O(l)△H2=-285.8kJ/mol
则CO2(g)与H2(g)反应生成CH4(g)与液态水的热化学方程式是
CO2(g)+4H2(g)═CH4(g)+2H2O(l)△H=-252.9kJ/mol
CO2(g)+4H2(g)═CH4(g)+2H2O(l)△H=-252.9kJ/mol
.(4)某同学用沉淀法测定含有较高浓度CO2的空气中CO2的含量,经查得一些物质在20℃的数据如下表.
| 溶解度(S)/g | 溶度积(Ksp) | ||
| Ca(OH)2 | Ba(OH)2 | CaCO3 | BaCO3 |
| 0.16 | 3.89 | 2.9×10-9 | 2.6×10-9 |
吸收CO2最合适的试剂是
Ba(OH)2
Ba(OH)2
(填“Ca(OH)2”或“Ba(OH)2”)溶液,实验时除需要测定工业废气的体积(折算成标准状况)外,还需要测定BaCO3的质量
BaCO3的质量
.