摘要: 答案. (2)2NaCl + 2H2O 2NaOH + H2↑ + Cl2↑ (3)Fe元素的化合价显+6价.易得电子 (6)KNO3 KCl. KNO3可用于化肥.炸药等
网址:http://m.1010jiajiao.com/timu3_id_60258[举报]
高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂.其生产流程如下: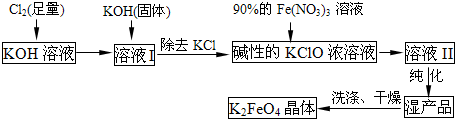
(1)KOH 与Cl2反应放热,随着反应的进行,温度会逐渐升高,就会有KClO3生成.所以,反应①应保持在
(2)在溶液I中加入KOH固体的目的是
a.KOH固体溶解时会放出较多的热量,有利于提高反应速率
b.与溶液I中过量的Cl2继续反应,生成更多的KClO
c.为下一步反应提供碱性的环境
d.使KClO3转化为 KClO
(3)从溶液II中分离出K2FeO4后,还得到副产品KNO3、KCl,写出③中反应的离子方程式为
(4)如何判断K2FeO4晶体已经洗涤干净
(5)高铁酸钾(K2FeO4)与水反应时,生成红褐色胶体的同时释放出一种具有氧化性的气体单质,该气态单质的化学式
查看习题详情和答案>>

(1)KOH 与Cl2反应放热,随着反应的进行,温度会逐渐升高,就会有KClO3生成.所以,反应①应保持在
较低温度
较低温度
下进行.若测得溶液I中KClO和KClO3的物质的量浓度之比为1:3,写出①反应的离子方程式20OH-+10Cl2
3ClO3-+ClO-+16Cl-+10H2O
| ||
20OH-+10Cl2
3ClO3-+ClO-+16Cl-+10H2O
.
| ||
(2)在溶液I中加入KOH固体的目的是
bc
bc
(填编号).a.KOH固体溶解时会放出较多的热量,有利于提高反应速率
b.与溶液I中过量的Cl2继续反应,生成更多的KClO
c.为下一步反应提供碱性的环境
d.使KClO3转化为 KClO
(3)从溶液II中分离出K2FeO4后,还得到副产品KNO3、KCl,写出③中反应的离子方程式为
2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O
2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O
.(4)如何判断K2FeO4晶体已经洗涤干净
用试管取少量最后一次的洗涤液,加入硝酸银溶液,无白色沉淀则已被洗净
用试管取少量最后一次的洗涤液,加入硝酸银溶液,无白色沉淀则已被洗净
.(5)高铁酸钾(K2FeO4)与水反应时,生成红褐色胶体的同时释放出一种具有氧化性的气体单质,该气态单质的化学式
O2
O2
,请写出反应的离子方程式:4FeO42-+10H2O═4Fe(OH)3(胶体)+3O2↑+8OH-
4FeO42-+10H2O═4Fe(OH)3(胶体)+3O2↑+8OH-
.(2012?保定一模)【化学一化学与技术】
高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂.其生产工艺如图:
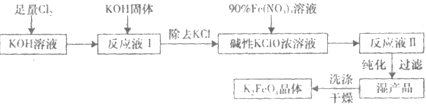
已知:
①温度较低时,Cl2通入KOH溶液生成次级酸盐;温度较高时,Cl2通入KOH溶液生成氯酸盐;
②Fe(NO3)3溶液与KClO溶液在强碱性环境中生成K2FeO4.请回答下列问题:
(1)该生产工艺应在
(2)为了提高生活用水的卫生标准,自来水厂常使用高铁酸钾(K2FeO4)进行消毒、净化以改善水质,其原因是
(3)经过高铁酸钾(K2FeO4)处理后的水不是纯净水,若要得到纯净水.可采用的净化方法是
(4)高铁酸钾溶于水形成浅紫红色溶液,溶液静置时会逐渐生成氧气并沉淀出三氧化二铁,此过程也会使溶液的pH增大.写出其化学方程式:
(5)在“反应液I”中加KOH固体的目的是为了①吸收“反应液I”中过量的Cl2,生成更多的KClO;②
(6)从“反应液Ⅱ”中分离出K2FeO4后,副产品是
查看习题详情和答案>>
高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂.其生产工艺如图:

已知:
①温度较低时,Cl2通入KOH溶液生成次级酸盐;温度较高时,Cl2通入KOH溶液生成氯酸盐;
②Fe(NO3)3溶液与KClO溶液在强碱性环境中生成K2FeO4.请回答下列问题:
(1)该生产工艺应在
温度较低
温度较低
(填“温度较高”或“温度较低”)的情况下进行.(2)为了提高生活用水的卫生标准,自来水厂常使用高铁酸钾(K2FeO4)进行消毒、净化以改善水质,其原因是
+6价的Fe元素易得电子表现出强氧化性,可杀菌消毒,还原产物Fe元素为+3价,在水中形成Fe(OH)3胶体,可吸附水中悬浮物并可使泥沙聚沉
+6价的Fe元素易得电子表现出强氧化性,可杀菌消毒,还原产物Fe元素为+3价,在水中形成Fe(OH)3胶体,可吸附水中悬浮物并可使泥沙聚沉
(3)经过高铁酸钾(K2FeO4)处理后的水不是纯净水,若要得到纯净水.可采用的净化方法是
蒸馏
蒸馏
(4)高铁酸钾溶于水形成浅紫红色溶液,溶液静置时会逐渐生成氧气并沉淀出三氧化二铁,此过程也会使溶液的pH增大.写出其化学方程式:
4K2FeO4+4H2O=2Fe2O3+8KOH+3O2↑
4K2FeO4+4H2O=2Fe2O3+8KOH+3O2↑
(5)在“反应液I”中加KOH固体的目的是为了①吸收“反应液I”中过量的Cl2,生成更多的KClO;②
为下一步反应提供反应物
为下一步反应提供反应物
.(6)从“反应液Ⅱ”中分离出K2FeO4后,副产品是
KNO3
KNO3
和KCl
KCl
(写化学式).(1)在其他条件不变的情况下,研究改变起始氢气物质的量[用n(H2)表示]对N2(g)+3H2(g)?2NH3(g)反应的影响,实验结果可表示成如图1所示的规律(图中T表示温度,n表示物质的量):
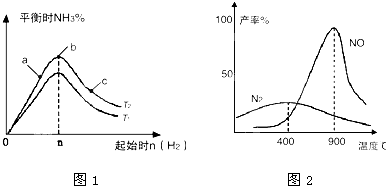
①比较在a、b、c三点所处的平衡状态中,反应物N2的转化率最高的是
②若容器容积为1L,n=3mol,反应达到平衡时N2、H2的转化率均为60%,则在起始时体系中加入N2的物质的量为
③图象中T2和T1的关系是
(2)氨气和氧气从145℃就开始反应,在不同温度和催化剂条件下生成不同产物(如图2):
4NH3+5O2?4NO+6H2O,4NH3+3O2?2N2+6H2O
温度较低时以生成
查看习题详情和答案>>

①比较在a、b、c三点所处的平衡状态中,反应物N2的转化率最高的是
c
c
.②若容器容积为1L,n=3mol,反应达到平衡时N2、H2的转化率均为60%,则在起始时体系中加入N2的物质的量为
1
1
mol,此条件下(T2),反应的平衡常数K=2.08(mol/L)-2
2.08(mol/L)-2
,当温度升高时该平衡常数将减小
减小
.③图象中T2和T1的关系是
低于
低于
.(填“高于”、“低于”、“等于”、“无法确定”).(2)氨气和氧气从145℃就开始反应,在不同温度和催化剂条件下生成不同产物(如图2):
4NH3+5O2?4NO+6H2O,4NH3+3O2?2N2+6H2O
温度较低时以生成
N2
N2
为主,温度高于900℃时,NO产率下降的原因是氨气氧化生成NO的反应是放热反应,升高温度转化率下降
氨气氧化生成NO的反应是放热反应,升高温度转化率下降
.(2009?沈阳三模)高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂.其生产工艺如下:

已知:①2KOH+Cl2→KCl+KClO+H2O(条件:温度较低)
②6KOH+3Cl2→5KCl+KClO3+3H2O(条件:温度较高)
③2Fe(NO3)3+2KClO+10KOH→2K2FeO4+6KNO3+3KCl+5H2O
回答下列问题:
(1)该生产工艺应在
(2)写出工业上制取Cl2的化学方程式
(3)K2FeO4具有强氧化性的原因
(4)配制KOH溶液时,是在每100mL水中溶解61.6g KOH固体(该溶液的密度为1.47g/mL),它的物质的量浓度为
(5)在“反应液I”中加KOH固体的目的是
A.与“反应液I”中过量的Cl2继续反应,生成更多的KClO
B.KOH固体溶解时会放出较多的热量,有利于提高反应速率
C.为下一步反应提供反应物
D.使副产物KClO3转化为 KClO
(6)从“反应液II”中分离出K2FeO4后,会有副产品
查看习题详情和答案>>

已知:①2KOH+Cl2→KCl+KClO+H2O(条件:温度较低)
②6KOH+3Cl2→5KCl+KClO3+3H2O(条件:温度较高)
③2Fe(NO3)3+2KClO+10KOH→2K2FeO4+6KNO3+3KCl+5H2O
回答下列问题:
(1)该生产工艺应在
温度较低
温度较低
(填“温度较高”或“温度较低”)情况下进行;(2)写出工业上制取Cl2的化学方程式
2NaCl+2H2O
2NaOH+H2↑+Cl2↑
| ||
2NaCl+2H2O
2NaOH+H2↑+Cl2↑
;
| ||
(3)K2FeO4具有强氧化性的原因
K2FeO4中铁元素化合价为+6价,易得电子
K2FeO4中铁元素化合价为+6价,易得电子
;(4)配制KOH溶液时,是在每100mL水中溶解61.6g KOH固体(该溶液的密度为1.47g/mL),它的物质的量浓度为
10mol/L
10mol/L
;(5)在“反应液I”中加KOH固体的目的是
AC
AC
:A.与“反应液I”中过量的Cl2继续反应,生成更多的KClO
B.KOH固体溶解时会放出较多的热量,有利于提高反应速率
C.为下一步反应提供反应物
D.使副产物KClO3转化为 KClO
(6)从“反应液II”中分离出K2FeO4后,会有副产品
KNO3、KCl
KNO3、KCl
(写化学式),它们都是重要的化工产品,具体说出其中一种物质的用途KNO3可用于化肥,炸药等
KNO3可用于化肥,炸药等
.
高铁酸钾(K2FeO4)是集氧化、吸附、絮凝于一体的新型多功能水处理剂,其生产工艺如下:
已知:①2KOH+Cl2=KCl+KClO+H2O(条件:温度较低)
②6KOH+3C12=5KCl+KClO3+3H2O(条件:温度较高)
③2Fe(NO3)3+2KC1O+10KOH=2K2FeO4+6KNO3+2KCl+5H2O
回答下列问题:(1)该工艺应在 (填“温度较高”或“温度较低”)的情况下进行,
(2)K2FeO4可作为新型多功能水处理剂的原因 ,
(3)在“反应液I”中加KOH固体的目的是① ,②为下一步反应提供反应物,
(4)从“反应液II”中分离出K2FeO4后,副产品是 (写化学式),
(5)高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压高铁电池的总反应3Zn+2K2FeO4+8H2O
3Zn(OH)2+2Fe(OH)3+4KOH
①写出该电池充电时阳极的电极反应式 ,
②下列叙述正确的是 (填字母)
A.Zn电极在放电时作负极,发生氧化反应
B.该电池放电时,K+向负极移动
C.放电时正极有1mol K2FeO4被还原,则转移3mol电子
③用该电池电解200mL 1mol?L-1 的AgNO3溶液(用惰性电极),当阴极质量增加2.16g时,被电解溶液的pH为 (溶液体积变化忽略不计).
查看习题详情和答案>>

已知:①2KOH+Cl2=KCl+KClO+H2O(条件:温度较低)
②6KOH+3C12=5KCl+KClO3+3H2O(条件:温度较高)
③2Fe(NO3)3+2KC1O+10KOH=2K2FeO4+6KNO3+2KCl+5H2O
回答下列问题:(1)该工艺应在
(2)K2FeO4可作为新型多功能水处理剂的原因
(3)在“反应液I”中加KOH固体的目的是①
(4)从“反应液II”中分离出K2FeO4后,副产品是
(5)高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压高铁电池的总反应3Zn+2K2FeO4+8H2O
| 放电 | 充电 |
①写出该电池充电时阳极的电极反应式
②下列叙述正确的是
A.Zn电极在放电时作负极,发生氧化反应
B.该电池放电时,K+向负极移动
C.放电时正极有1mol K2FeO4被还原,则转移3mol电子
③用该电池电解200mL 1mol?L-1 的AgNO3溶液(用惰性电极),当阴极质量增加2.16g时,被电解溶液的pH为