摘要: 表中①-⑥为短周期元素及相应部分原子半径的数据: 元 素 性 质 元 素 编 号 ① ② ③ ④ ⑤ ⑥ 原子半径(nm) a 0.075 b 0.110 c d 最 高 化 合 价 +6 +5 +5 +7 最 低 化 合 价 -2 -3 -2 -3 -1 -1 下列说法正确的是( ) A. 元素①的最外层电子排布为2S22P4 B. 元素②氢化物与元素⑥氢化物之间反应形成化合物中只有极性键 C. 原子半径:a>d>b>c D. 非金属性:元素⑤>元素④>元素① [答案]C [解析]先从化合价角度分析.最高正价为最外层电子数.最低价的绝对值为8减最外层电子数.元素①和元素③同在ⅥA族.由于O无最高正价.可确定元素①为S和元素③为O元素,元素②和元素④同在ⅤA族.半径大小②< ④.马上确定元素②为N元素④为P元素,元素①的最外层电子排布为3S23P4,NH3与HCl生成NH4Cl中含有离子键和极性键,原子半径大小应为S>Cl>O>F.即a>d>b>c,非金属性:元素⑤>元素①>元素④.即F>S>P.选C
网址:http://m.1010jiajiao.com/timu3_id_57448[举报]
表中①~⑥为短周期元素及相应部分原子半径的数据。下列说法正确的是

[ ]
A.元素①的最外层电子排布为2s22p4
B.元素②氢化物与元素⑥氢化物反应形成化合物中只有共价键
C.原子半径:a>d>b>c
D.非金属性:元素⑤>元素④>元素①
查看习题详情和答案>>
B.元素②氢化物与元素⑥氢化物反应形成化合物中只有共价键
C.原子半径:a>d>b>c
D.非金属性:元素⑤>元素④>元素①
有四种短周期元素的部分性质如下,请根据有关信息填空:
注:气体密度已换算为标准状况
(1)元素W在周期表中的位置
(2)短周期主族元素中,元素X以及与其相邻元素的气态氢化物的稳定性由强到弱顺序是:
(3)同族元素单质及其化合物在许多性质上都存在着递变规律.下列有关说法正确的是
a.元素W所在族,随着原子序数递增,单质的熔点逐渐降低
b.元素X所在族,随着原子序数递增,对应简单离子的还原性逐渐增强
c.元素Y所在族,随着原子序数递增,对应氢化物的沸点逐渐升高
d.元素Z所在族,随着原子序数递增,最高氧化物对应水化物的酸性逐渐增强
(4)Z单质与足量Y单质反应,生成物的电子式为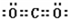
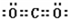 ,已知生成1mol该产物将伴随393.51kJ的热量变化,写出该反应的热化学方程式
,已知生成1mol该产物将伴随393.51kJ的热量变化,写出该反应的热化学方程式
查看习题详情和答案>>
| 元素 | W | X | Y | Z |
| 原子半径 | 186pm | 99pm | 66pm | 77pm |
| 核外电子 | 有4种能级不同的电子 | 最外层有7种运动状态不同的电子 | 核外电子占有5个轨道 | 有2个未成对电子 |
| 单质 部分 性质 |
密度:0.97g?cm-3 熔点:97.8℃ 能导电 |
沸点:-34.0℃ 不能导电 |
密度:1.43g?L-1 沸点:-183.0℃ 不能导电 |
熔点:3550℃ 能导电 |
(1)元素W在周期表中的位置
第三周期第ⅠA族
第三周期第ⅠA族
,根据性质描述,元素Z的单质是石墨
石墨
(写名称),上述元素的简单离子中半径最小的是Na+
Na+
(写离子符号).(2)短周期主族元素中,元素X以及与其相邻元素的气态氢化物的稳定性由强到弱顺序是:
HF>HCl>H2S
HF>HCl>H2S
(用化学式表示).(3)同族元素单质及其化合物在许多性质上都存在着递变规律.下列有关说法正确的是
b
b
(选填序号).a.元素W所在族,随着原子序数递增,单质的熔点逐渐降低
b.元素X所在族,随着原子序数递增,对应简单离子的还原性逐渐增强
c.元素Y所在族,随着原子序数递增,对应氢化物的沸点逐渐升高
d.元素Z所在族,随着原子序数递增,最高氧化物对应水化物的酸性逐渐增强
(4)Z单质与足量Y单质反应,生成物的电子式为
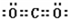
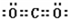
C(s)+O2(g)=CO2△H=-393.51kJ/mol
C(s)+O2(g)=CO2△H=-393.51kJ/mol
.
有四种短周期元素的部分性质如下,请根据有关信息填空:
注:气体密度已换算为标准状况
(1)元素W在周期表中的位置______,根据性质描述,元素Z的单质是______(写名称),上述元素的简单离子中半径最小的是______(写离子符号).
(2)短周期主族元素中,元素X以及与其相邻元素的气态氢化物的稳定性由强到弱顺序是:______(用化学式表示).
(3)同族元素单质及其化合物在许多性质上都存在着递变规律.下列有关说法正确的是______(选填序号).
a.元素W所在族,随着原子序数递增,单质的熔点逐渐降低
b.元素X所在族,随着原子序数递增,对应简单离子的还原性逐渐增强
c.元素Y所在族,随着原子序数递增,对应氢化物的沸点逐渐升高
d.元素Z所在族,随着原子序数递增,最高氧化物对应水化物的酸性逐渐增强
(4)Z单质与足量Y单质反应,生成物的电子式为______,已知生成1mol该产物将伴随393.51kJ的热量变化,写出该反应的热化学方程式______.
查看习题详情和答案>>
| 元素 | W | X | Y | Z |
| 原子半径 | 186pm | 99pm | 66pm | 77pm |
| 核外电子 | 有4种能级不同的电子 | 最外层有7种运动状态不同的电子 | 核外电子占有5个轨道 | 有2个未成对电子 |
| 单质 部分 性质 | 密度:0.97g?cm-3 熔点:97.8℃ 能导电 | 沸点:-34.0℃ 不能导电 | 密度:1.43g?L-1 沸点:-183.0℃ 不能导电 | 熔点:3550℃ 能导电 |
(1)元素W在周期表中的位置______,根据性质描述,元素Z的单质是______(写名称),上述元素的简单离子中半径最小的是______(写离子符号).
(2)短周期主族元素中,元素X以及与其相邻元素的气态氢化物的稳定性由强到弱顺序是:______(用化学式表示).
(3)同族元素单质及其化合物在许多性质上都存在着递变规律.下列有关说法正确的是______(选填序号).
a.元素W所在族,随着原子序数递增,单质的熔点逐渐降低
b.元素X所在族,随着原子序数递增,对应简单离子的还原性逐渐增强
c.元素Y所在族,随着原子序数递增,对应氢化物的沸点逐渐升高
d.元素Z所在族,随着原子序数递增,最高氧化物对应水化物的酸性逐渐增强
(4)Z单质与足量Y单质反应,生成物的电子式为______,已知生成1mol该产物将伴随393.51kJ的热量变化,写出该反应的热化学方程式______.
查看习题详情和答案>>
下表是部分短周期元素的原子半径及主要化合价,根据表中的信息,判断下面叙述正确的是( )
|
查看习题详情和答案>>
下表为部分短周期元素化合价及相应氢化物沸点的数据:
已知:①A与D可形成化合物AD2、AD3,可用于制备强酸甲;②B与D可形成化合物BD、BD2,可用于制备强酸乙.
请回答:
(1)表中属于第三周期元素的是
(2)写出H的最高价氧化物的电子式:
 ,比较A、D、G三种简单阴离子的半径大小:
,比较A、D、G三种简单阴离子的半径大小:
r(
(3)由表中D元素和氢元素的原子按1:1组成的常见液态化合物的稀溶液易被催化分解,可使用的催化剂为(填序号)
a.MnO2b.FeCl3 c.Na2SO3 d.KMnO4
(4)分子组成为ADG2的物质在水中会强烈水解,产生使品红溶液褪色的无色气体和一种强酸.该反应的化学方程式是:
(5)工业生产强酸乙时可用纯碱溶液处理尾气,该反应如下:BD+BD2+Na2CO3=2
①横线上某盐的化学式应为
(6)请设计一个实验方案,使得铜和稀的强酸甲反应,得到蓝色溶液和氢气,在答题卡指定位置绘出实验装置图,标出必要的说明即可
 .
.
查看习题详情和答案>>
| 元素性质 | 元素编号 | |||||||
| A | B | C | D | E | F | G | H | |
| 氢化物的沸点(℃) | -60.7 | -33.4 | -111.5 | 100 | -87.7 | 19.54 | -84.9 | -161.5 |
| 最高化合价 | +6 | +5 | +4 | +5 | +7 | +4 | ||
| 最低化合价 | -2 | -3 | -4 | -2 | -3 | -1 | -1 | -4 |
请回答:
(1)表中属于第三周期元素的是
ACEG
ACEG
(用表中元素编号填写).(2)写出H的最高价氧化物的电子式:


r(
S2-
S2-
)>r(Cl-
Cl-
)>r(O2-
O2-
) (用元素符号表示)(3)由表中D元素和氢元素的原子按1:1组成的常见液态化合物的稀溶液易被催化分解,可使用的催化剂为(填序号)
ab
ab
.a.MnO2b.FeCl3 c.Na2SO3 d.KMnO4
(4)分子组成为ADG2的物质在水中会强烈水解,产生使品红溶液褪色的无色气体和一种强酸.该反应的化学方程式是:
SOCl2+H2O=SO2+2HCl
SOCl2+H2O=SO2+2HCl
.(5)工业生产强酸乙时可用纯碱溶液处理尾气,该反应如下:BD+BD2+Na2CO3=2
NaNO2
NaNO2
+CO2①横线上某盐的化学式应为
NaNO2
NaNO2
;②每产生44.8L(标准状况)CO2,被吸收尾气的质量是152
152
g.(6)请设计一个实验方案,使得铜和稀的强酸甲反应,得到蓝色溶液和氢气,在答题卡指定位置绘出实验装置图,标出必要的说明即可

