网址:http://m.1010jiajiao.com/timu3_id_53661[举报]
I.关于反应物之间的定量关系的研究:
(1)已知反应:2I-+2Fe3+=I2+2Fe2+,向100mL,0.1moL?L-1的FeI2溶液中通入0.01mol Cl2,该反应的离子方程式为
(2)298K时,Mg(OH)2的溶度积常数Ksp=5.6×10-12,将物质的量浓度均为2×10-4mol?L-1的氯化镁溶液和氢氧化钠溶液等体积混合,能否产生氢氧化镁沉淀?
Ⅱ,关于反应速率、限度的研究:
近段时间,全国范围内的雾霾天气严重影响了人们的身体健康.环境问题越来越受到人们的重视.汽车尾气中含有较多的NO和CO,两种气体均会使人体中毒.以CO为例,其中毒原理是相同温度下CO与血红蛋白的结合能力远远大于氧气与血红蛋白的结合能力,反应如下:CO+HbO2?O2+HbCO(HbO2表示氧合血红蛋白).
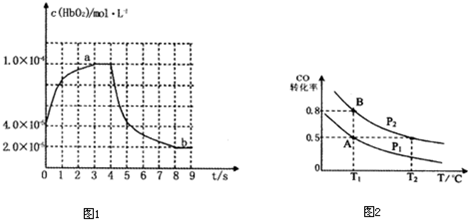
如图表示HbO2浓度随时间的变化:曲线a表示向血样中通入氧气后的变化;曲线b表示在第4s时通入CO和O2混合气体后的变化.
(3)前3s以HbO2表示的平均反应速率为
(4)37℃时,CO+HbO2?O2+HbCO,该反应的平衡常数K=220,资料显示HbCO的浓度达到HbO2浓度的0.022倍,就会导致人体智力受损.据此,通过计算可知,当吸入的CO与O2浓度之比大于或等于
| 1 |
| 10000 |
| 1 |
| 10000 |
(5)一氧化碳、氢气既是重要的能源,也可以催化还原NO等消除污染,还可以在一定条件下制取CH3OH.已知
N2(g)+O2(g)=2NO((g)△H=+180.5kJ?mol-1
2H2(g)+O2(g)=2H2O(1)△H=-571.6kJ?mol-1
H2O(g)=H2O(1)△H=-44kJ?mol-1
写出H2与NO反应生成N2和水蒸气的热化学方程式
(6)在一容积可变的密闭容器中充入10mol CO和20molH2,在催化剂存在时反应生成甲醇:CO(g)+2H2(g)?CH3OH(g),CO的平衡转化率随温度(T)、压强(P)的变化如右图所示,当达到平衡状态A时,容器的体积为10L.如反应开始时仍充入10mol CO和20mol H2,则在平衡状态B时容器的体积V(B)=
(1)某学习小组欲制备少量的氨水.供选用的试剂有:①NH4Cl ②(NH4)2CO3.提供的装置如下:
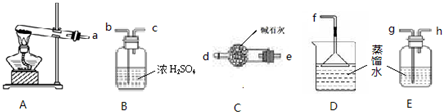
请回答下列问题:
①装置A试管内发生反应的化学方程式为
| ||
| ||
②从提供的仪器中选择并组装一套本实验的合理、简洁装置,按气流方向连接顺序为(用图中标注的导管口符号表示)a→
(2)氨在氧气中燃烧,生成水和一种单质.
已知:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ?mol-1
2H2(g)+O2(g)=2H2O(l)△H=-572kJ?mol-1
试写出氨在氧气中燃烧生成液态水和气态单质的热化学方程式
(3)在一定条件下,将1molN2和3molH2混合于一个10L的密闭容器中发生反应N2+3H2
| 催化剂 |
| 高温高压 |
①该反应的平衡常数表达式
| c2(NH3) |
| c(N2)?c3(H2) |
| c2(NH3) |
| c(N2)?c3(H2) |
②从反应开始到平衡时,N2的反应速率v(N2)=
③H2的转化率为
(4)为检验氨气与酸反应得到的某种常见氮肥的成分,某同学进行了以下实验:①加热氮肥样品产生气体,其中一种气体能使湿润的红色石蕊试纸变蓝,另一种气体能使澄清石灰水变浑浊.②取少量该氮肥样品溶于水,并加入少量BaCl2溶液,没有明显变化.由此可知该氮肥的主要成分可能是
A.NH4Cl B.(NH4)2CO3 C.NH4HCO3 D.NH4NO3.
氨既是实验室中常用试剂,也是工业上重要原料.
(1)某学习小组欲制备少量的氨水.供选用的试剂有:①NH4Cl ②(NH4)2CO3.提供的装置如下:

请回答下列问题:
①装置A试管内发生反应的化学方程式为______
②从提供的仪器中选择并组装一套本实验的合理、简洁装置,按气流方向连接顺序为(用图中标注的导管口符号表示)a→______.
(2)氨在氧气中燃烧,生成水和一种单质.
已知:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ?mol-1
2H2(g)+O2(g)=2H2O(l)△H=-572kJ?mol-1
试写出氨在氧气中燃烧生成液态水和气态单质的热化学方程式______.
(3)在一定条件下,将1molN2和3molH2混合于一个10L的密闭容器中发生反应N2+3H2 2NH3,5min后达到平衡,平衡时氨的体积分数为25%.
2NH3,5min后达到平衡,平衡时氨的体积分数为25%.
①该反应的平衡常数表达式______.
②从反应开始到平衡时,N2的反应速率v(N2)=______.
③H2的转化率为______.
(4)为检验氨气与酸反应得到的某种常见氮肥的成分,某同学进行了以下实验:①加热氮肥样品产生气体,其中一种气体能使湿润的红色石蕊试纸变蓝,另一种气体能使澄清石灰水变浑浊.②取少量该氮肥样品溶于水,并加入少量BaCl2溶液,没有明显变化.由此可知该氮肥的主要成分可能是______.
A.NH4Cl B.(NH4)2CO3 C.NH4HCO3 D.NH4NO3.
查看习题详情和答案>>
向容积为2 L的密闭容器中充人2 mol A气体和1 mol B气体,在一定条件下发生如下反应:2A(g)+B(g) 3C(g);经2 s后达到平衡,测得C气体的浓度为0.6 mol·L-1。下列说法中正确的是
①用物质A表示该反应的平均反应速率为0.2 mol·L-1·s-1
②用物质B表示该反应的平均反应速率为0.2 mol·L-1·s-1
③平衡时物质A与B的转化率相等
④平衡时物质B的浓度为0.2 mol·L-1
⑤其他条件不变,向容器中再加入1 molC气体,达到新平衡时,C的体积分数不变
A.①②③ B.①③⑤ C.②④⑤ D.①④⑤
【解析】考查可逆反应的有关计算。这种类型的试题往往采用三段式,即
2A(g)+B(g) 3C(g)
起始量(mol) 2 1 0
转化量(mol) 0.8 0.4 1.2
平衡量(mol) 1.2 0.6 1.2
所以用物质A表示该反应的平均反应速率为
用物质B表示该反应的平均反应速率为
平衡时物质A与B的转化率分别为![]() 、
、
平衡时物质B的浓度为![]()
加入1mol的C就相当于加入2/3molA和1/3molB,因为反应前后体积不变,此时A和B的比值仍然满足2︰1,所以平衡是等效的。
查看习题详情和答案>>
向容积为2 L的密闭容器中充人2 mol A气体和1 mol B气体,在一定条件下发生如下反应:2A(g)+B(g)  3C(g);经2 s后达到平衡,测得C气体的浓度为0.6 mol·L-1。下列说法中正确的是
3C(g);经2 s后达到平衡,测得C气体的浓度为0.6 mol·L-1。下列说法中正确的是
①用物质A表示该反应的平均反应速率为0.2 mol·L-1·s-1
②用物质B表示该反应的平均反应速率为0.2 mol·L-1·s-1
③平衡时物质A与B的转化率相等
④平衡时物质B的浓度为0.2 mol·L-1
⑤其他条件不变,向容器中再加入1 molC气体,达到新平衡时,C的体积分数不变
A.①②③ B.①③⑤ C.②④⑤ D.①④⑤
【解析】考查可逆反应的有关计算。这种类型的试题往往采用三段式,即
2A(g)+B(g)  3C(g)
3C(g)
起始量(mol) 2 1 0
转化量(mol) 0.8 0.4 1.2
平衡量(mol) 1.2 0.6 1.2
所以用物质A表示该反应的平均反应速率为
用物质B表示该反应的平均反应速率为
平衡时物质A与B的转化率分别为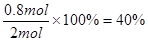 、
、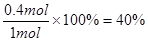
平衡时物质B的浓度为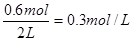
加入1mol的C就相当于加入2/3molA和1/3molB,因为反应前后体积不变,此时A和B的比值仍然满足2︰1,所以平衡是等效的。
查看习题详情和答案>>