网址:http://m.1010jiajiao.com/timu3_id_5119[举报]
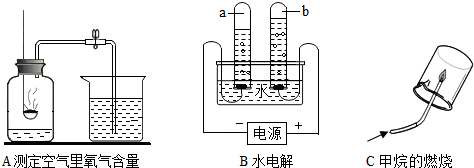
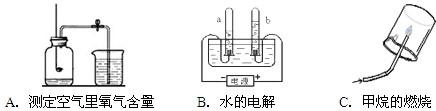
[探究1]研究常见物质组成.A、B、C都是教材上研究物质组成的实验.
(1)导致A实验测定结果偏小的可能原因有
(2)B实验的目的是
①确定水的组成;②研究水的导电性;③研究水分子的运动.
(3)C实验通过验证反应产物并根据化学反应前后
[探究2]研究气体的制取、性质和收集
根据下列实验装置图,回答问题:
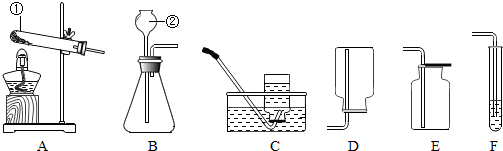
(1)写出标有序号的仪器名称:①
(2)小红将A与C相连,用高锰酸钾制取氧气,反应方程式为
实验操作有:a.停止加热b.固定试管c.将导管从水槽中取出d.装药品和放棉花e.加热,收集氧气.上述过程中缺少的一步操作是
(3)实验室制取二氧化碳气体,应选择的发生装置为
(4)化学兴趣小组的同学在研究氨气的性质时,做了下面两个实验:
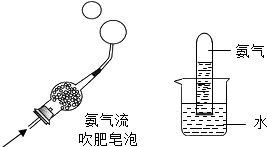
根据上述实验现象,写出氨气的两点性质
(5)若用A装置进行木炭还原氧化铜实验,还需与F装置相连.F装置内应盛放的药品是
通过化学实验可以认识物质的组成、性质与制取.
[探究1]研究常见物质组成.A、B、C都是教材上研究物质组成的实验.
(1)导致A实验测定结果偏小的可能原因有______(举一例).
(2)B实验的目的是______(选择下列正确的序号填空)
①确定水的组成;②研究水的导电性;③研究水分子的运动.
(3)C实验通过验证反应产物并根据化学反应前后______种类不变来推断甲烷的组成.
[探究2]研究气体的制取、性质和收集
根据下列实验装置图,回答问题:
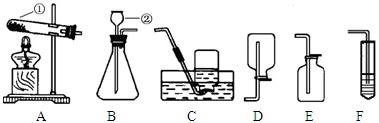
(1)写出标有序号的仪器名称:①______,②______;
(2)小红将A与C相连,用高锰酸钾制取氧气,反应方程式为______,
实验操作有:a.停止加热b.固定试管c.将导管从水槽中取出d.装药品和放棉花e.加热,收集氧气.上述过程中缺少的一步操作是______.
(3)实验室制取二氧化碳气体,应选择的发生装置为______,收集装置应选______.发生反应的化学方程式为______.
(4)化学兴趣小组的同学在研究氨气的性质时,做了下面两个实验:

根据上述实验现象,写出氨气的两点性质______、______.
(5)若用A装置进行木炭还原氧化铜实验,还需与F装置相连.F装置内应盛放的药品是______.实验结束后,小明同学先用弹簧夹将连接A、F装置的橡皮管夹住,然后熄灭酒精灯,这样做除了能防止倒吸外,还具有的作用是______.
查看习题详情和答案>>
【探究1】研究常见物质组成。A、B、C都是教材上研究物质组成的实验。
(1)导致A实验测定结果偏小的可能原因有 (举一例)。
(2)B实验的目的是 (选择下列正确的序号填空)
①确定水的组成 ②研究水的导电性 ③研究水分子的运动
(3)C实验通过验证反应产物并根据化学反应前后 种类不变来推断甲烷的组成。


(5)小红将A与C相连,用高锰酸钾制取氧气, 反应方程式为 ,实验操作有:a.停止加热 b.固定试管 c.将导管从水槽中取出 d.装药品和放棉花 e.加热,收集氧气。上述过程中缺少的一步操作是 。
(6)实验室制取二氧化碳气体,应选择的发生装置为 ,收集装置应选 。发生反应的化学方程式为 。
(7)化学兴趣小组的同学在研究氨气的性质时,做了下面两个实验:

(8)若用A装置进行木炭还原氧化铜实验,还需与F装置相连。F装置内应盛放的药品是 。实验结束后,小明同学先用弹簧夹将连接A、F装置的橡皮管夹住,然后熄灭酒精灯,这样做除了能防止倒吸外,还具有的作用是 。
氢化钙(CaH2)是一种常用的储氢材料,也是登山运动员常用的能源提供剂.
[资料在线]
Ⅰ.金属钙的活动性很强,遇水即刻剧烈反应生成氢氧化钙,同时产生一种气体.
Ⅱ.氢化钙要密封保存,一旦接触到水就发生反应,放出氢气.
Ⅲ.用氢气与金属钙加热的方法可制得氢化钙.
Ⅳ.白色的无水硫酸铜粉末吸水后会变蓝.
[探究一:定性分析]
(1)对于“金属钙与水反应生成的气体”有如下猜想:甲.氧气,乙.氢气
你支持________(填“甲”、“乙”)观点,理由是________.
(2)CaH2中氢元素的化合价是________,写出CaH2与水反应的化学方程式________;
(3)登山运动员常携带氢化钙作为能源提供剂,与携带氢气相比,其优点是________;
(4)用氢气与金属钙加热可得到氢化钙,以下是反应装置图.
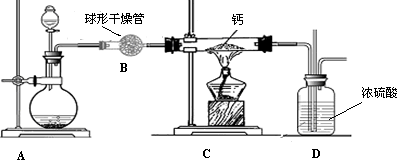
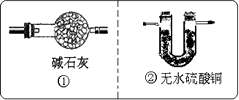
装置A中装有锌粒和稀硫酸,请写出其反应的化学方程式________,装置B中装有无水氯化钙,其作用是________,若要证明进入C装置中的氢气已经干燥,在B、C之间应连接下图中的哪个装置:________(填①或②),现象是________.
(5)制备CaH2实验结束后,某同学取少量产物,小心加入水中,观察到有气泡冒出,在溶液中滴入酚酞后显红色.该同学据此判断:上述实验确有CaH2生成.你认为是否正确________(填“是”或“否”);原因是________.
[探究二:产物定量测定]
测定原理:根据金属钙、氢化钙都能与水反应生成气体的原理,采用测定气体的体积的方法.
(1)取氢化钙样品与水反应,利用下图装置测定生成的气体体积时,在________即进行收集(填字母).
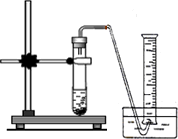
A.气泡连续均匀时
B.刚开始有气泡时
(2)利用该装置,测得的气体体积总是会偏小,同学讨论后采用下图装置测定气体体积.该装置的优点是________,如何实现A中的水与B中样品接触而发生反应________.

(3)称取46 mg所制得的氢化钙样品,注射器D开始时活塞停留在10 mL刻度处,反应结束后充分冷却,活塞最终停留57.04 mL刻度处.试通过计算求出样品中氢化钙的纯度(即氢化钙在样品中的质量分数)是________.(设该条件下每11.2 mL氢气的质量为1 mg)
[反思提高]
(1)上述实验在学校的实验室内,通过托盘天平等称量工具________(填“能”、“不能”)完成.
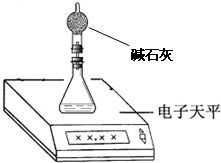
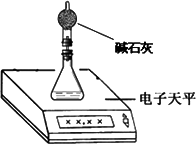
(2)测量小组利用电子天平,采用如下图所示方法以反应前后失去的质量来求算纯度,结果纯度的测定值偏________.
【资料在线】
Ⅰ.金属钙的活动性很强,遇水即刻剧烈反应生成氢氧化钙,同时产生一种气体.
Ⅱ.氢化钙要密封保存,一旦接触到水就发生反应,放出氢气.
Ⅲ.用氢气与金属钙加热的方法可制得氢化钙.
Ⅳ.白色的无水硫酸铜粉末吸水后会变蓝.
探究一:定性分析
(1)对于“金属钙与水反应生成的气体”有如下猜想:甲.氧气,乙.氢气你支持
(2)CaH2中氢元素的化合价是
(3)登山运动员常携带氢化钙作为能源提供剂,与携带氢气相比,其优点是
(4)用氢气与金属钙加热可得到氢化钙,以下是反应装置图.
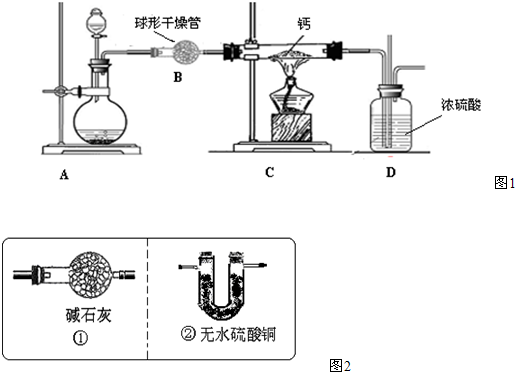
装置A 中装有锌粒和稀硫酸,请写出其反应的化学方程式
(5)制备CaH2实验结束后,某同学取少量产物,小心加入水中,观察到有气泡冒出,在溶液中滴入酚酞后显红色.该同学据此判断:上述实验确有CaH2生成.你认为是否正确
探究二:产物定量测定
测定原理:根据金属钙、氢化钙都能与水反应生成气体的原理,采用测定气体的体积的方法.
(1)取氢化钙样品与水反应,利用图1装置测定生成的气体体积时,在
A.气泡连续均匀时
B.刚开始有气泡时
(2)利用该装置,测得的气体体积总是会偏小,同学讨论后采用图2装置测定气体体积.该装置的优点是
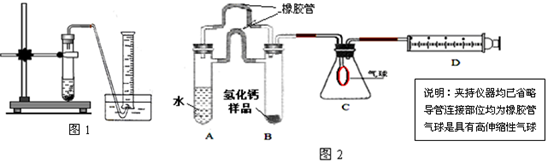
(3)称取46mg 所制得的氢化钙样品,注射器D开始时活塞停留在10mL刻度处,反应结束后充分冷却,活塞最终停留57.04mL刻度处.试通过计算求出样品中氢化钙的纯度(即氢化钙在样品中的质量分数)是
反思提高:
(1)上述实验在学校的实验室内,通过托盘天平等称量工具
(2)测量小组利用电子天平,采用如下图所示方法以反应前后失去的质量来求算纯度,结果纯度的测定值偏