摘要:简述为:有弱才水解.无弱不水解 越弱越水解.弱弱都水解 谁强显谁性.等强显中性 具体为:1.正盐溶液 ①强酸弱碱盐呈酸性 ②强碱弱酸盐呈碱性 ③强酸强碱盐呈中性 ④弱酸碱盐不一定 如 NH4CN CH3CO2NH4 NH4F 碱性 中性 酸性 取决于弱酸弱碱 相对强弱
网址:http://m.1010jiajiao.com/timu3_id_51056[举报]
(12分)
通常,硅不与水反应,然而,弱碱性水溶液能使一定量的硅溶解,生成Si(OH)4。
1-1 已知反应分两步进行,试用化学方程式表示上述溶解过程。
早在上世纪50年代就发现了CH5+的存在,人们曾提出该离子结构的多种假设,然而,直至1999年,才在低温下获得该离子的振动-转动光谱,并由此提出该离子的如下结构模型:氢原子围绕着碳原子快速转动;所有C-H键的键长相等。
1-2 该离子的结构能否用经典的共价键理论说明?简述理由。
1-3 该离子是( )。
A.质子酸 B.路易斯酸 C.自由基 D.亲核试剂
2003年5月报道,在石油中发现了一种新的烷烃分子,因其结构类似于金刚石,被称为“分子钻石”,若能合成,有可能用做合成纳米材料的理想模板。该分子的结构简图如下:
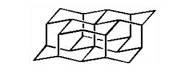
1-4 该分子的分子式为 ;
1-5 该分子有无对称中心?
1-6 该分子有几种不同级的碳原子?
1-7 该分子有无手性碳原子?
1-8 该分子有无手性?
查看习题详情和答案>>