网址:http://m.1010jiajiao.com/timu3_id_49576[举报]
(1)我们常用的一种甲醇燃料电池,是以甲醇与氧气的反应为原理设计的,其电解质溶液是KOH溶液。写出该电池负极的电极反应式_______________。
(2)下图为常用笔记本电脑所用甲醇质子交换膜燃料电池的结构示意图。该装置中________(填“a”或“b”)为电池的正极, 已知任何反应都具有一定的可逆性。该甲醇质子交换膜燃料电池在实际工作中,各反应物、生成物均以气态的形式存在且反应也具有一定可逆性,即其反应原理可表示为 2CH3OH(g)+3O2(g)
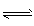 2CO2(g)+4H2O(g),试写出该条件下反应的平衡常数(K)___________ ; 在电脑的使用过程中,电池的温度往往因为各种原因会升高,试判断温度升高时该反应的平衡常数(K)____________(填增大、减小、不变),其反应的正反应速率 ___________(填增大、减小、不变);温度升高_________(填有利或不利于)电池将化学能转化为电能。
2CO2(g)+4H2O(g),试写出该条件下反应的平衡常数(K)___________ ; 在电脑的使用过程中,电池的温度往往因为各种原因会升高,试判断温度升高时该反应的平衡常数(K)____________(填增大、减小、不变),其反应的正反应速率 ___________(填增大、减小、不变);温度升高_________(填有利或不利于)电池将化学能转化为电能。 
①2CH3OH(l)+3O2(g)===2CO2(g)+4H2O(g) ΔH1=-1 275.6 kJ·mol-1
②2CO(g)+O2(g)===2CO2(g) ΔH2=-566.0 kJ·mol-1
③H2O(g)===H2O(l) ΔH3=-44.0 kJ·mol-1
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:__________。
II:某温度下,向密闭容器中充入2.0 mol CO和1.0mol H2O,发生反应:
CO(g)+H2O(g)
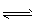 CO2(g)+H2(g)。 CO的转化率随时间变化关系如图,回答下列问题:
CO2(g)+H2(g)。 CO的转化率随时间变化关系如图,回答下列问题: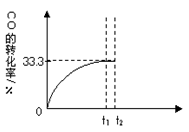
A.该反应的反应物混合后很不稳定
B.该反应一旦发生将在很短的时间内完成
C.该反应体系达到平衡时至少有一种反应物的百分含量很小
D.该反应一定是放热反应
E.该反应使用催化剂意义不大
(5)t2时刻向平衡体系中再通入1.0 mol H2O(g),t3时刻重新建立平衡,请在原坐标图中将改变这一条件后CO的转化率的变化趋势表示出来,必须注明再次建立平衡后CO的转化率。
碳和碳的化合物在生产生活实际中应用广泛.运用化学反应原理研究碳的氧化物的性质具有重要意义.
(1)常温下,碳酸在水中的电离常数Ka1=4.2×10-7,Ka2=5.6×10-11;次氯酸在水中的电离常数K=4.7×10-8.写出向“84消毒液”(主要成分为氯化钠和次氯酸钠)中通入二氧化碳发生反应的离子方程式________;
(2)下图为常用笔记本电脑所用的甲醇质子交换膜燃料电池的结构示意图.电池总反应为2CH3OH+3O2![]() 2CO2+4H2O.该装置放电时________(填“a”或“b”)为电池的负极,其电极反应式为________;
2CO2+4H2O.该装置放电时________(填“a”或“b”)为电池的负极,其电极反应式为________;

(3)CO具有还原性,某化学研究小组为证明CO具有还原性,设计了如图所示的实验装置.

已知
:C+H2O CO+H2 CO+H2O
CO+H2 CO+H2O CO2+H2
CO2+H2 C+CO2
C+CO2试回答下列问题:
①装置B中最适宜的试剂是________,必须用装置C吸收气体中的水蒸气的理由是________;
②根据该实验中的________现象,可证明
CO具有还原性;③若要根据装置
F中石灰水变浑浊的现象准确确认CO具有还原性,则应在上图装置与________之间(填字母标号)连接下图中的________装置(选填序号).
(16分)碳和碳的化合物在生产生活实际中应用广泛。运用化学反应原理研究碳的氧化物的性质具有重要意义。
(1)常温下,碳酸在水中的电离常数Ka1=4.2×10-7 ,Ka2=5.6×10-11;次氯酸在水中的电离常数Ka=4.7×10-8。写出向“84消毒液”(主要成分为氯化钠和次氯酸钠)中通入二氧化碳发生反应的离子方程式 ;
(2)上图为常用笔记本电脑所用的甲醇质子交换膜燃料电池的结构示意图。电池总反应为2CH3OH+3O22CO2+4H2O。该装置放电时 (填“a”或“b”)为电池的负极,其电极反应式为 ;
(3)CO具有还原性,某化学研究小组为证明CO具有还原性,设计了如图所示的实验装置。
已知:C + H2OCO+H2 CO + H2O
CO2 + H2 C + CO2
2CO
试回答下列问题:
① 装置B中最适宜的试剂是 ,必须用装置C吸收气体中的水蒸气的理由是 ;
② 根据该实验中的 现象,可证明CO具有还原性;
③ 若要根据装置F中石灰水变浑浊的现象准确确认CO具有还原性,则应在上图装置 与 之间(填字母标号)连接下图中的 装置(选填序号)。
查看习题详情和答案>>
(16分)碳和碳的化合物在生产生活实际中应用广泛。运用化学反应原理研究碳的氧化物的性质具有重要意义。
(1)常温下,碳酸在水中的电离常数Ka1=4.2×10-7,Ka2=5.6×10-11;次氯酸在水中的电离常数Ka = 4.7×10-8。写出向“84消毒液”(主要成分为氯化钠和次氯酸钠)中通入二氧化碳发生反应的离子方程式 ;
4.7×10-8。写出向“84消毒液”(主要成分为氯化钠和次氯酸钠)中通入二氧化碳发生反应的离子方程式 ;
(2)上图为常用笔记本电脑所用的甲醇质子交换膜燃料电池的结构示 意图。电池总反应为2CH3OH+3O2
意图。电池总反应为2CH3OH+3O2 2CO2+4H2O。该装置放电时 (填“a”或“b”)为电池的负极,其电极反应式为 ;
2CO2+4H2O。该装置放电时 (填“a”或“b”)为电池的负极,其电极反应式为 ;
(3)CO具有还原性,某化学研究小组为证明CO具有还原性,设计了如图所示的实验装置。
已知:C + H2O CO+H2 CO + H2O
CO+H2 CO + H2O CO2 +
CO2 +  H2 C + CO2
H2 C + CO2 2CO
2CO
试回答下列问题:
①装置B中最适宜的试剂是 ,必须用装置C吸收气体中的水蒸气的理由是 ;
②根据该实验中的 现象,可证明CO具有还原性;
③若要根据装置F中石灰水变浑浊的现象准确确认CO具有还原性,则应在上图装置 与 之间(填字母标号)连接下图中的 装置(选填序号)。
(16分)碳和碳的化合物在生产生活实际中应用广泛。运用化学反应原理研究碳的氧化物的性质具有重要意义。
(1)常温下,碳酸在水中的电离常数Ka1=4.2×10-7 ,Ka2=5.6×10-11;次氯酸在水中的电离常数Ka =4.7×10-8。写出向“84消毒液”(主要成分为氯化钠和次氯酸钠)中通入二氧化碳发生反应的离子方程式 ;

(2)上图为常用笔记本电脑所用的甲醇质子交换膜燃料电池的结构示意图。电池总反应为2CH3OH+3O2 2CO2+4H2O。该装置放电时 (填“a”或“b”)为电池的负极,其电极反应式为
;
2CO2+4H2O。该装置放电时 (填“a”或“b”)为电池的负极,其电极反应式为
;
(3)CO具有还原性,某化学研究小组为证明CO具有还原性,设计了如图所示的实验装置。

已知:C + H2O CO+H2 CO + H2O
CO+H2 CO + H2O CO2 + H2 C + CO2
CO2 + H2 C + CO2 2CO
2CO
试回答下列问题:
① 装置B中最适宜的试剂是 ,必须用装置C吸收气体中的水蒸气的理由是 ;
② 根据该实验中的 现象,可证明CO具有还原性;
③ 若要根据装置F中石灰水变浑浊的现象准确确认CO具有还原性,则应在上图装置 与 之间(填字母标号)连接下图中的 装置(选填序号)。

查看习题详情和答案>>