摘要: 实验室中用CO还原磁铁矿(主要成分为Fe3O4)得到铁.设计的实验装置如下, 高温 (1)开始实验时.A装置中首先要进行的操作是通一氧化碳(填“加热 或“通一氧化碳 ) (2)CO还原Fe304的化学方程式为 Fe3O4+4CO==3Fe+4CO2. (3)B装置的作用是检验是否有二氧化碳气体生成. (4)为分离A装置中反应排出的一氧化碳和二氧化碳.某同学设计了如下装置(固定装置已略去.a.b为活塞): 当关闭活塞b.打开活塞a时.可分离得到CO .然后关闭活塞a.再打开活塞b.又可分离得到CO2 28某固体混合物M.可能含有Na2SO4.NaCl.NaNO3.NaOH中的一种或几种.某 同学为确定固体混合物M的可能组成.设计了下列实验: 根据上述实验.回答下列问题: (1)混合物M中一定不含NaOH.一定含Na2SO4. (2)上述实验不能肯定混合物M中是否含有NaCl.原因是在滴加BaCl2溶液时引入了Cl-.如果要确认混合物M中是否含有NaCl.实验操作步骤是重新取样.加水溶解.滴加过量的Ba(NO3)2溶液.静置后取上层清液.再滴加硝酸酸化的AgNO3溶液.若有白色沉淀生成.则混合物M中肯定含NaCl.反之则不含.
网址:http://m.1010jiajiao.com/timu3_id_4953[举报]
实验室中用CO还原磁铁矿(主要成分为Fe3O4)得到铁,设计的实验装置如下:

(1)开始实验时,A装置中首先要进行的操作是______________(填“加热”或“通一氧化碳”)。
(2)CO还原Fe3O4的化学方程式为______________________。
(3)B装置的作用是______________________。
(4)为分离A装置中反应排出的一氧化碳和二氧化碳,某同学设计了如下装置(固定装置已略去,a、b为活塞):
(2)CO还原Fe3O4的化学方程式为______________________。
(3)B装置的作用是______________________。
(4)为分离A装置中反应排出的一氧化碳和二氧化碳,某同学设计了如下装置(固定装置已略去,a、b为活塞):

当关闭活塞b,打开活塞a时,可分离得到__________,然后关闭活塞a,再打开活塞b,又可分离得到_______。
查看习题详情和答案>>
实验室中用CO还原磁铁矿(主要成分为Fe3O4)得到铁,设计的实验装置如下;

(1)开始实验时,A装置中首先要进行的操作是________(填“加热”或“通一氧化碳”)
(2)CO还原Fe3O4的化学方程式为________.
(3)B装置的作用是________.
(4)为分离A装置中反应排出的一氧化碳和二氧化碳,某同学设计了如下装置(固定装置已略去,a、b为活塞):

当关闭活塞b,打开活塞a时,可分离得到________,然后关闭活塞a,再打开活塞b,又可分离得到________
实验室中用CO还原磁铁矿(主要成分为Fe3O4)得到铁,设计的实验装置如下;
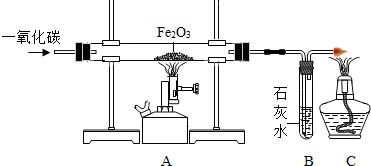
(1)开始实验时,A装置中首先要进行的操作是 (填“加热”或“通一氧化碳”).
(2)CO还原Fe304的化学方程式为 .
(3)B装置的作用是 .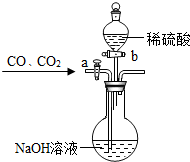
(4)为分离A装置中反应排出的一氧化碳和二氧化碳,某同学设计了如图装置(固定装置已略去,a、b为活塞):当关闭活塞b,打开活塞a时,可分离得到 ,然后关闭活塞a,再打开活塞b,又可分离得到 .
查看习题详情和答案>>

(1)开始实验时,A装置中首先要进行的操作是
(2)CO还原Fe304的化学方程式为
(3)B装置的作用是

(4)为分离A装置中反应排出的一氧化碳和二氧化碳,某同学设计了如图装置(固定装置已略去,a、b为活塞):当关闭活塞b,打开活塞a时,可分离得到
 实验室中用CO还原磁铁矿(主要成分为四氧化三铁)得到铁,设计的实验装置如图.
实验室中用CO还原磁铁矿(主要成分为四氧化三铁)得到铁,设计的实验装置如图.
