摘要:以下离子方程式正确的是 A. 氧化铁溶于氢碘酸:Fe2O3+6H+ = 2Fe3++3H2O B. 等物质的量的KHCO3和Ba(OH)2的溶液混合:HCO3-+Ba2++OH- = BaCO3↓+H2O C. NaHSO3溶液显酸性是因为:HSO3- = SO32-+ H+ D. 硫化钠水溶液呈碱性的原因:S2-+2H2O H2S↑+2OH-
网址:http://m.1010jiajiao.com/timu3_id_48154[举报]
 (2008?佛山一模)(1)合成氨工业对化学工业和国防工业具有重要意义.工业合成
(2008?佛山一模)(1)合成氨工业对化学工业和国防工业具有重要意义.工业合成氨的原理是:N2+3H2
| 20-50MPa | 500℃、铁触煤 |
①X的化学式为
NH3
NH3
;②图中条件选定的主要原因是(选填字母序号)
BC
BC
;A.升高温度、增大压强均有利于氨的合成
B.铁触媒在该温度时活性大
C.工业生产受动力、材料、设备等条件的限制
③改变反应条件,会使平衡发生移动.图2表示随条件改变,氨气的百分含量的变化趋势.当横坐标为压强时,变化趋势正确的是(选填字母序号)
c
c
,当横坐标为温度时,变化趋势正确的是(选填字母序号)a
a
.(2)常温下氨气极易溶于水,其水溶液可以导电.
④用方程式表示氨气溶于水且显弱碱性的过程:
NH3+H2O?NH3?H2O?NH4++OH-
NH3+H2O?NH3?H2O?NH4++OH-
;⑤氨水中水电离出的c(OH-)
<
<
10-7 mol?L-1(填写“>”、“<”或“=”);⑥将相同体积、相同物质的量浓度的氨水和盐酸混合后,溶液中离子浓度由大到小依次为
c(Cl-)>c(NH4+)>c(H+)>c(OH-)
c(Cl-)>c(NH4+)>c(H+)>c(OH-)
. (2009?佛山一模)10℃时,在烧杯中加入0.1mol/L的 NaHCO3溶液400mL,加热,测得该溶液的pH发生如下变化:
(2009?佛山一模)10℃时,在烧杯中加入0.1mol/L的 NaHCO3溶液400mL,加热,测得该溶液的pH发生如下变化:| 温度(℃) | 10 | 20 | 30 | 50 | 70 |
| pH | 8.3 | 8.4 | 8.5 | 8.9 | 9.4 |
HCO3-+H2O?H2CO3+OH-
HCO3-+H2O?H2CO3+OH-
;(2)乙同学认为,溶液pH升高的原因是NaHCO3受热分解,生成了Na2CO3,并推断Na2CO3的水解程度
大于
大于
(填“大于”或“小于”)NaHCO3;(3)丙同学认为,要确定上述哪种说法合理,只要把加热后的溶液冷却到10℃后再测定溶液pH,若pH
=
=
8.3(填“>”、“<”或“=”),说明甲正确,若pH>
>
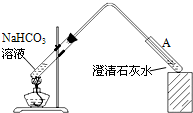
8.3(填“>”、“<”或“=”),说明乙正确;(4)丁同学设计如下实验方案对甲、乙同学的解释进行判断:
实验装置如图,加热煮沸NaHCO3溶液,发现试管A中产生沉淀,说明
乙
乙
(填“甲”或“乙”)推测正确;(5)将一定体积0.1mol/L的 NaHCO3溶液置于烧杯中加热至微沸(溶液体积不变),测其pH为9.8;将烧杯冷却至室温,过一段时间(溶液体积不变)测得pH为10.1.据此资料可以判断
乙
乙
(填“甲”或“乙”)推测正确,原因是溶液冷却至室温后pH大于8.4,说明此实验过程中溶液有新物质生成
溶液冷却至室温后pH大于8.4,说明此实验过程中溶液有新物质生成
. (2008?佛山一模)盐酸、硫酸和硝酸是中学阶段常见的“三大酸”.请就“三大酸”与金属铜反应的情况,回答下列问题:
(2008?佛山一模)盐酸、硫酸和硝酸是中学阶段常见的“三大酸”.请就“三大酸”与金属铜反应的情况,回答下列问题:(1)我们知道,稀盐酸与铜不反应,但向稀盐酸中加入H2O2后,则可使铜溶解.该反应的化学方程式为
Cu+H2O2+2HCl=CuCl2+2H2O
Cu+H2O2+2HCl=CuCl2+2H2O
.某同学未加入氧化剂,而是将它设计成一个电解装置,也能使铜很快溶于稀盐酸.请在方格中画出该装置:(2)在一定体积的18mol?L-1的浓硫酸中加入过量的铜片,加热使之反应,被还原的硫酸是0.9mol,则该硫酸的实际体积
大于
大于
(填大于、等于或小于)100mL.有同学提出:若使剩余的铜片继续溶解,可向其中加入硝酸盐,可行吗?可行
可行
(填“可行”或“不可行”).如果可行,用离子方程式说明原因;如果不可行,此问可以不填3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
.(3)将等质量的铜片分别与等体积、过量的浓硝酸和过量的稀硝酸反应,所得到的溶液前者呈绿色,后者呈蓝色,某同学提出可能是Cu2+浓度不同引起的,你同意这种看法吗?
不同意
不同意
(填“同意”或“不同意”),原因是等质量的铜片与等体积、过量的浓硝酸、稀硝酸反应,所得溶液中Cu2+的浓度基本相等
等质量的铜片与等体积、过量的浓硝酸、稀硝酸反应,所得溶液中Cu2+的浓度基本相等
.另一同学提出溶液呈“绿色”是溶液中Cu2+与NO2共存的结果,请你设计实验探究此说法正确与否,请简述实验方案、实验现象及由此得出的结论:将一定量的NO2通入铜片与稀硝酸反应后的溶液中,若溶液呈绿色,则该同学的结论正确,反之,不正确
将一定量的NO2通入铜片与稀硝酸反应后的溶液中,若溶液呈绿色,则该同学的结论正确,反之,不正确
.