摘要:已知反应: ①101KPa时.2C(s)+O2,△H=-221kJ/mol ②稀溶液中.H+(aq)+OH-(aq)=H2O(l),△H=-57.3kJ/mol下列结论正确的是( ) A.碳的燃烧热大于110.5kJ/mol B.①的反应热为221kJ/mol C.稀硫酸与稀NaOH溶液反应的中和热为-57.3kJ/mol D.稀醋酸与稀NaOH溶液反应生成1mol水.放出57.3KJ热量
网址:http://m.1010jiajiao.com/timu3_id_47985[举报]
 已知反应3A(g)+2B(g)?C(g)+4D(g);△H<0,如图中a、b表示一定条件下,D的体积分数随时间t的变化情况.若要使曲线b变为曲线a,可采取的措施是( )
已知反应3A(g)+2B(g)?C(g)+4D(g);△H<0,如图中a、b表示一定条件下,D的体积分数随时间t的变化情况.若要使曲线b变为曲线a,可采取的措施是( )①增大B的浓度
②升高反应温度
③缩小反应容器的体积加压
④加入催化剂.
查看习题详情和答案>>
 已知反应X(g)+Y(g)?nZ(g)△H<0,将X和Y 以一定比例混合通入2L密闭容器中进行反应,各物质的浓度随时间的改变如图所示.下列说法正确的是( )
已知反应X(g)+Y(g)?nZ(g)△H<0,将X和Y 以一定比例混合通入2L密闭容器中进行反应,各物质的浓度随时间的改变如图所示.下列说法正确的是( )| A、反应方程式中n=2 | B、该反应的△S>0 | C、10min时,曲线发生变化的原因是增大压强 | D、0~5min内,平均反应速率v(X)=0.04mol?L-1?min-1 |
已知反应:
Na2S2O3+2HCl=2NaCl+S↓+SO2↑+H2O
2Na2S+Na2SO3+6HCl=6NaCl+3S↓+3H2O
2Na2S+Na2S2O3+6HCl=6NaCl+4S↓+3H2O
某样品A由①Na2SO4②NaCl ③Na2S ④Na2SO3⑤Na2S2O3 五种物质中的三种混合而成.取一定量的样品A,投入到0.300L 1.00mol/L 的稀盐酸中,充分反应后,滤去不溶物B,将所得的溶液稀释到1.00L,测得其pH=1,蒸干此溶液,最终得到纯净物C.结合所学知识,解答下列问题:
(1)样品A中一定没有的物质
(2)若测得C的质量为W克,且样品A中一定含有NaCl,则W值的范围
(3)若样品A与盐酸完全反应,同时在标准状况下还收集到224ml的H2S气体(设产生的气体全部逸出),则样品A中的Na2S的质量为
查看习题详情和答案>>
Na2S2O3+2HCl=2NaCl+S↓+SO2↑+H2O
2Na2S+Na2SO3+6HCl=6NaCl+3S↓+3H2O
2Na2S+Na2S2O3+6HCl=6NaCl+4S↓+3H2O
某样品A由①Na2SO4②NaCl ③Na2S ④Na2SO3⑤Na2S2O3 五种物质中的三种混合而成.取一定量的样品A,投入到0.300L 1.00mol/L 的稀盐酸中,充分反应后,滤去不溶物B,将所得的溶液稀释到1.00L,测得其pH=1,蒸干此溶液,最终得到纯净物C.结合所学知识,解答下列问题:
(1)样品A中一定没有的物质
①
①
(填序号)(2)若测得C的质量为W克,且样品A中一定含有NaCl,则W值的范围
W>11.7
W>11.7
(3)若样品A与盐酸完全反应,同时在标准状况下还收集到224ml的H2S气体(设产生的气体全部逸出),则样品A中的Na2S的质量为
5.46
5.46
g.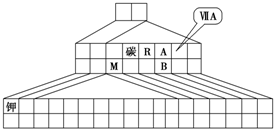 如图是元素周期表的另一种画法--三角形元素周期表的一部分,图上标有第ⅦA族和碳、钾两种元素的位置.
如图是元素周期表的另一种画法--三角形元素周期表的一部分,图上标有第ⅦA族和碳、钾两种元素的位置.回答下列问题:
(1)请在图中将过渡元素所在的位置涂黑.
(2)工业上用于冶炼M的化学方程式为
2Al2O3
4Al+3O2
| ||
2Al2O3
4Al+3O2
.
| ||
(3)M和R组成化合物MR的超细粉末被广泛应用于大规模集成电路生产等领域.其制取原理是用M的氧化物、R的单质与碳单质在高温下反应,已知反应中三种物质的物质的量之比为1:1:3,该反应的化学方程式为
Al2O3+N2+3C
2AlN+3CO
| ||
Al2O3+N2+3C
2AlN+3CO
,反应中
| ||
N2
N2
作氧化剂.(4)图中A、B两元素形成的离子B2A8-2中,B元素呈现最高价,B原子位于由A原子组成的四面体的中心,且所有原子的最外层电子均满足8电子结构.该离子可能具有的化学性质是
氧化性
氧化性
,依据是离子结构中存在-O-O-(部分氧元素呈-1价亦可)
离子结构中存在-O-O-(部分氧元素呈-1价亦可)
.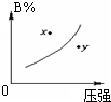 已知反应mA(s)+nB(g)?pC(g)△H<0,在一定温度下达到平衡时B的体积分数(B%)与压强的关系如图所示,下列判断错误的是( )
已知反应mA(s)+nB(g)?pC(g)△H<0,在一定温度下达到平衡时B的体积分数(B%)与压强的关系如图所示,下列判断错误的是( )