摘要:18. A.已知A.B.C.D.E都是周期表中前四周期的元素.它们的核电荷数A<B<C<D<E.其中A.B.C是同一周期的非金属元素.化合物DC的晶体为离子晶体.D的二价阳离子与C的阴离子具有相同的电子层结构.AC2为非极性分子.B.C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高.E的原子序数为24.ECl3能与B.C的氢化物形成六配位的配合物.且两种配体的物质的量之比为2∶1.三个氯离子位于外界.请根据以上情况.回答下列问题:(答题时.A.B.C.D.E用所对应的元素符号表示) (1)A.B.C的第一电离能由小到大的顺序为 . (2)B的氢化物的分子空间构型是 .其中心原子采取 杂化. (3)写出化合物AC2的电子式 ,一种由B.C组成的化合物与AC2互为等电子体.其化学式为 . (4)E的核外电子排布式是 .ECl3形成的配合物的化学式为 . (5)B的最高价氧化物对应的水化物的稀溶液与D的单质反应时.B被还原到最低价.该反应的化学方程式是 . B.醇与氢卤酸反应是制备卤代烃的重要方法.实验室制备溴乙烷和1-溴丁烷的反应如下: NaBr+H2SO4HBr+NaHSO4 ① R-OH+HBrR-Br+H2O ② 可能存在的副反应有:醇在浓硫酸的存在下脱水生成烯和醚.Br-被浓硫酸氧化为Br2等.有关数据列表如下, 乙醇 溴乙烷 正丁醇 1-溴丁烷 密度/g·cm-3 0.7893 1.4604 0.8098 1.2758 沸点/℃ 78.5 38.4 117.2 101.6 请回答下列问题: (1)溴乙烷和1-溴丁烷的制备实验中.下列仪器最不可能用到的是 . a.圆底烧瓶 b.量筒 c.锥形瓶 d.布氏漏斗 (2)溴代烃的水溶性 (填“大于 .“等于 或“小于 ),其原因是 . (3)将1-溴丁烷粗产品置于分液漏斗中加水.振荡后静置.产物在 (填“上层 .“下层 或“不分层 ). (4)制备操作中.加入的浓硫酸必需进行稀释.起目的是 . a.减少副产物烯和醚的生成 b.减少Br2的生成 c.减少HBr的挥发 d.水是反应的催化剂 (5)欲除去溴代烷中的少量杂质Br2.下列物质中最适合的是 . a.NaI b.NaOH c.NaHSO3 d.KCl (6)在制备溴乙烷时.采用边反应边蒸出产物的方法.其有利于 ,但在制备1-溴丁烷时却不能边反应边蒸出产物.其原因是 .
网址:http://m.1010jiajiao.com/timu3_id_47333[举报]
Ⅰ﹑化合物A的分子式为C3H6O2,有下列转化关系:F 能发生银镜反应.

(1)A的名称
(2)B的结构简式是
(3)D中含有的官能团是
(4)写出C+E→F的化学反应方程式
Ⅱ﹑阿斯匹林的结构简式如图所示:

(5)请写出阿斯匹林与NaOH溶液在加热条件下反应的化学方程式

(6)将其水解产物加酸酸化后得到产物A,已知A的同分异构体中具有以下性质:
①滴加FeCl3溶液时,溶液变成紫色,②能与银氨溶液反应生成银单质,③苯环上有2个取代基;则符合条件的 A的同分异构体有
查看习题详情和答案>>

(1)A的名称
乙酸甲酯
乙酸甲酯
(2)B的结构简式是
CH3COOH
CH3COOH
(3)D中含有的官能团是
醛基
醛基
(写名称)(4)写出C+E→F的化学反应方程式
HCOOH+CH3OH
HCOOCH3+H2O
| 浓硫酸 |
| △ |
HCOOH+CH3OH
HCOOCH3+H2O
| 浓硫酸 |
| △ |
Ⅱ﹑阿斯匹林的结构简式如图所示:

(5)请写出阿斯匹林与NaOH溶液在加热条件下反应的化学方程式


(6)将其水解产物加酸酸化后得到产物A,已知A的同分异构体中具有以下性质:
①滴加FeCl3溶液时,溶液变成紫色,②能与银氨溶液反应生成银单质,③苯环上有2个取代基;则符合条件的 A的同分异构体有
3
3
种. A、B、C、D均为常见物质,相互之间的关系如图所示.“-”表示两种物质间能发生反应,“→”表示物质间的转化关系,部分反应物或生成物以及反应条件已略去).
A、B、C、D均为常见物质,相互之间的关系如图所示.“-”表示两种物质间能发生反应,“→”表示物质间的转化关系,部分反应物或生成物以及反应条件已略去).(1)若A、C是气体,且常温下,A是气体、C是固体、D是温室气体,则
①D的电子式是


②已知C(s)+A(g)=D(g)△H=-393.5kJ/mol;
2B(g)+A(g)=2D(g)△H=-566.0kJ/mol;
则2C(s)+A(g)=2B(g) 的反应热△H=
-221
-221
kJ/mol.(2)若A是一种可溶性碱,B是一种可溶性盐,B在工业上可用于制造玻璃,则
①D的化学式可能是
CaCO3或CO2
CaCO3或CO2
;②将少量的C溶液滴入A溶液反应的离子方程式是
HCO3-+Ba2++OH-=BaCO3↓+H2O
HCO3-+Ba2++OH-=BaCO3↓+H2O
.(3)若A是一种一元酸,B、C、D都是金属,D是亮红色固体,且B、C在A的浓溶液中钝化,则由A的浓溶液与C、D组成的原电池电极反应式是负极:
Cu-2e-=Cu2+
Cu-2e-=Cu2+
;正极:2NO3-+2e-+4H+=2NO2↑+2H2O
2NO3-+2e-+4H+=2NO2↑+2H2O
. A.已知A、B、C、D、E是短周期中的五种元素,它们的原子序数依次增大.A和B可形成常见化合物BA4,一个BA4分子中电子总数为10;C原子的最外层电子数是核外电子总数的
A.已知A、B、C、D、E是短周期中的五种元素,它们的原子序数依次增大.A和B可形成常见化合物BA4,一个BA4分子中电子总数为10;C原子的最外层电子数是核外电子总数的| 3 |
| 4 |
(1)D与E两元素相比较,非金属性较强的是
氯
氯
(填元素名称),请你自选试剂设计实验验证该结论(说明试剂、简单操作、实验现象)将Cl2通入Na2S溶液(或氢硫酸)中,有浅黄色沉淀生成,说明Cl的非金属性比S强
将Cl2通入Na2S溶液(或氢硫酸)中,有浅黄色沉淀生成,说明Cl的非金属性比S强
;(2)A、C、D间可形成甲、乙两种微粒,它们均为负一价双原子阴离子且甲有18个电子,乙有l0个电子,则甲与乙反应的离子方程式为
HS-+OH-═S2-+H2O
HS-+OH-═S2-+H2O
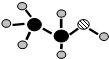
;(3)由A、B、C三种元素组成的化合物的球棍结构如图:,试写出利用植物秸秆生产这种物质的化学方程式
(C6H10O5)n+nH2O
nC6H12O6
| 催化剂 |
| △ |
(C6H10O5)n+nH2O
nC6H12O6
、| 催化剂 |
| △ |
C6H12O6
2CH3CH2OH+2CO2↑
| 一定条件 |
C6H12O6
2CH3CH2OH+2CO2↑
.| 一定条件 |
 现有A、B、C、D、E、F六种短周期主族元素,它们的原子序数依次增大,D与E同主族,且D的氢化物常温时为液态.A、B的最外层电子数之和与C的最外层电子数相等,A分别与B、C、D形成电子总数相等的分子.
现有A、B、C、D、E、F六种短周期主族元素,它们的原子序数依次增大,D与E同主族,且D的氢化物常温时为液态.A、B的最外层电子数之和与C的最外层电子数相等,A分别与B、C、D形成电子总数相等的分子.(1)C的元素符号是
N
N
;B的最高价氧化物的电子式为

第三周期第ⅦA族
第三周期第ⅦA族
.(2)B、C、D元素的氢化物的沸点由商到低的顺序为
H2O>NH3>CH4
H2O>NH3>CH4
(用化学式表示).(3)将足量D的单质通入到A2E的溶液中,反应的化学方程式为
2H2S+O2=2S↓+2H2O
2H2S+O2=2S↓+2H2O
(4)最近意大利罗马大学的FuNvio Cacace等人获得了极具理论研究意义的C4气态分子.C4分子结构如图所示,已知断裂1molC-C吸收l67KJ的热量,生成1mol C≡C放出942KJ热量.试写出由C4气态分子变成C2气态分子的热化学方程式:
N4(g)=2N2(g)△H=-882kJ/mol
N4(g)=2N2(g)△H=-882kJ/mol
.(5)某盐x(C2A6F2)的性质与CA4F类似,是离子化合物,其水溶液因分步水解而呈弱酸性.
①盐x显酸性原因(用离子方程式表示)
N2H62++H2O?[N2H5?H2O]++H+
N2H62++H2O?[N2H5?H2O]++H+
.②写出足量金属镁加入盐x的溶液中产生H2的记学方程式为
Mg+N2H6Cl2=MgCl2+N2H4+H2↑
Mg+N2H6Cl2=MgCl2+N2H4+H2↑
.