摘要: 王水能将极难溶的 HgS 溶解.反应产物包括HgCl42-.SO2. NO.请写出这个反应的离子方程式: .
网址:http://m.1010jiajiao.com/timu3_id_435067[举报]
Ⅰ.用尿素、氢氧化钠和水作为溶剂,预冷至零下12℃,能将极难溶解的纤维素溶化为粘液.武汉大学张俐娜教授因此而荣获美国2011年度安塞姆?佩恩奖.
(1)尿素[CO(NH2)2]中元素原子半径最大的原子结构示意图为 ;能说明氧元素原子比氮元素原子得电子能力强的事实是 (填选项).
A.在NO2中氧元素显负价,氮元素显正价
B.H2O的热稳定性比NH3的稳定
C.常温下H2O是液态而NH3是气态
D.O2比N2易液化
(2)尿素在土壤中的脲酶作用下会水解生成碳酸铵或碳酸氢铵,若与碱性肥料混合施用,会造成氮元素损失,请用离子方程式解释其原因 ;
已知:20℃时,H2CO3:Ka1=4.2×10-7;Ka2=5.6×10-11;NH3?H2O:Kb=1.7×10-5
碳酸氢铵溶液中HCO-3、NH+4,OH-、H+四种离子浓度由大到小是 (填选项).
A.c(HCO3-)c(NH4+)c(OH-)c(H+)
B.c(NH4+)c(HCO3-)c(OH-)c(H+)
C.c(HCO3-)c(NH4+)c(H+)c(OH-)
D.c(NH4+)c(HCO3-)c(H+)c(OH-)
Ⅱ.NaNO2外观酷似食盐,误食会中毒.
(3)在酸性条件下,NaNO2与KI按物质的量1:1恰好完全反应,I-被氧化为I2.写出此反应的离子方程式 .
(4)工业废水中含少量NO-2,可用电解法将NO-2转换为N2除去.N2将在 极生成,写出NO-2在酸性条件下转化为N2的电极反应式 .
查看习题详情和答案>>
(1)尿素[CO(NH2)2]中元素原子半径最大的原子结构示意图为
A.在NO2中氧元素显负价,氮元素显正价
B.H2O的热稳定性比NH3的稳定
C.常温下H2O是液态而NH3是气态
D.O2比N2易液化
(2)尿素在土壤中的脲酶作用下会水解生成碳酸铵或碳酸氢铵,若与碱性肥料混合施用,会造成氮元素损失,请用离子方程式解释其原因
已知:20℃时,H2CO3:Ka1=4.2×10-7;Ka2=5.6×10-11;NH3?H2O:Kb=1.7×10-5
碳酸氢铵溶液中HCO-3、NH+4,OH-、H+四种离子浓度由大到小是
A.c(HCO3-)c(NH4+)c(OH-)c(H+)
B.c(NH4+)c(HCO3-)c(OH-)c(H+)
C.c(HCO3-)c(NH4+)c(H+)c(OH-)
D.c(NH4+)c(HCO3-)c(H+)c(OH-)
Ⅱ.NaNO2外观酷似食盐,误食会中毒.
(3)在酸性条件下,NaNO2与KI按物质的量1:1恰好完全反应,I-被氧化为I2.写出此反应的离子方程式
(4)工业废水中含少量NO-2,可用电解法将NO-2转换为N2除去.N2将在
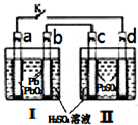 飞机、汽车、拖拉机、坦克,都是用蓄电池作为照明光源是典型的可充型电池,总反应式为:
飞机、汽车、拖拉机、坦克,都是用蓄电池作为照明光源是典型的可充型电池,总反应式为:Pb+PbO2+4H++2SO42-
| ||
| 充电 |
(1)当K闭合时,a电极的电极反应式是
PbO2+2e-+4H++SO42-=PbSO4+2H2O
PbO2+2e-+4H++SO42-=PbSO4+2H2O
;放电过程中SO42-向b
b
极迁移.当K闭合一段时间后,再打开K,Ⅱ可单独作为原电池使用,此时c电极的电极反应式为Pb-2e-+SO42-=PbSO4
Pb-2e-+SO42-=PbSO4
.(2)铅的许多化合物,色彩缤纷,常用作颜料,如铬酸铅是黄色颜料,碘化铅是金色颜料(与硫化锡齐名),室温下碘化铅在水中存在如下平衡:PbI2(S)?Pb2+(aq)+2I-(aq).
①该反应的溶度积常数表达式为Ksp=
c(Pb2+)?c2(I-)
c(Pb2+)?c2(I-)
.②已知在室温时,PbI2的溶度积Ksp=8.0×10-9,则100mL 2×10-3mol/L的碘化钠溶液中,加入100mL2×10-2mol/L的硝酸铅溶液,通过计算说明是否能产生PbI2沉淀
Qc=10-2?(10-3)2=10-8>Ksp,能产生PbI2沉淀
Qc=10-2?(10-3)2=10-8>Ksp,能产生PbI2沉淀
.③探究浓度对碘化铅沉淀溶解平衡的影响
该化学小组根据所提供试剂设计两个实验,来说明浓度对沉淀溶解平衡的影响.
提供试剂:NaI饱和溶液、NaCl饱和溶液、FeCl3饱和溶液、PbI2饱和溶液、PbI2悬浊液;
信息提示:Pb2+和Cl-能形成较稳定的PbCl42-络离子.
请填写下表的空白处:
| 实验内容 | 实验方法 | 实验现象及原因分析 |
| ①碘离子浓度增大对平衡的影响 | 取PbI2饱和溶液少量于一支试管中,再加入少量NaI饱和溶液, 取PbI2饱和溶液少量于一支试管中,再加入少量NaI饱和溶液, |
溶液中出现黄色浑浊. 原因是溶液中c(I-)增大,使Qc大于了pbI2的Ksp 溶液中出现黄色浑浊. 原因是溶液中c(I-)增大,使Qc大于了pbI2的Ksp |
| ②铅离子浓度减小对平衡的影响 | 取PbI2悬浊液少量于一支试管中,再加入少量NaCl饱和溶液 取PbI2悬浊液少量于一支试管中,再加入少量NaCl饱和溶液 |
黄色浑浊消失 原因是形成PbCl42-,导致溶液中c(Pb2+)减小,使Qc小于了pbI2的Ksp 黄色浑浊消失 原因是形成PbCl42-,导致溶液中c(Pb2+)减小,使Qc小于了pbI2的Ksp |
| ③ 铅离子和碘离子浓度都减小对平衡的影响 铅离子和碘离子浓度都减小对平衡的影响 |
在PbI2悬浊液中加入少量FeCl3饱和溶液 | PbI2 +2Fe3++4Cl-=PbCl42-+2Fe2++I2 PbI2 +2Fe3++4Cl-=PbCl42-+2Fe2++I2 |
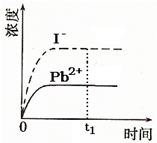 ④已知室温下PbI2的Ksp=8.0×10-9,将适量PbI2固体溶于 100mL水中至刚好饱和,该过程中Pb2+和I-浓度随时间变化关系如图(饱和PbI2溶液中c(I-)=0.0025mol?L-1).若t1时刻在上述体系中加入100mL.、0.020mol?L-1 NaI 溶液,画出t1时刻后Pb2+和I-浓度随时间变化关系图.
④已知室温下PbI2的Ksp=8.0×10-9,将适量PbI2固体溶于 100mL水中至刚好饱和,该过程中Pb2+和I-浓度随时间变化关系如图(饱和PbI2溶液中c(I-)=0.0025mol?L-1).若t1时刻在上述体系中加入100mL.、0.020mol?L-1 NaI 溶液,画出t1时刻后Pb2+和I-浓度随时间变化关系图.⑤至于碳酸铅,早在古代就被用作白色颜料.考古工作者发掘到的古代壁画或泥俑,其中人脸常是黑色的.经过化学分析和考证,证明这黑色的颜料是铅的化合物--硫化铅(已知PbCO3的
Ksp=1.46×10-13,PbS的Ksp=9.04×10-29)试分析其中奥妙
PbCO3的Ksp=1.46×10-13 >PbS的Ksp=9.04×10-29 故PbCO3与S2-接触时,转化为更难溶的黑色的PbS了
PbCO3的Ksp=1.46×10-13 >PbS的Ksp=9.04×10-29 故PbCO3与S2-接触时,转化为更难溶的黑色的PbS了
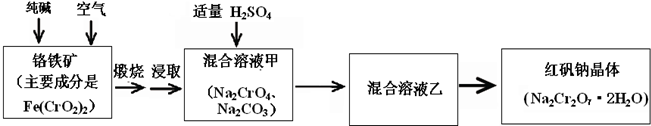
.(2012?朝阳区二模)重铬酸钠俗称红矾钠(Na2Cr2O7?2H2O)是重要的化工产品和强氧化剂.工业制备的流程如下:
请回答:
(1)已知Fe(CrO2)2中铬元素是+3价,则Fe(CrO2)2中铁元素是
(2)化学上可将某些盐写成氧化物的形式,如Na2SiO3可写成Na2O?SiO2,则Fe(CrO2)2可写成
(3)煅烧铬铁矿时,矿石中难溶的Fe(CrO2)2生成可溶于水的Na2CrO4,反应化学方程式如下:
4Fe(CrO2)2+8Na2CO3+7O2=2Fe2O3+8Na2CO4+8CO2
为了加快该反应的反应速率,可采取的措施是
(4)已知CrO42-在不同的酸性溶液中有不同的反应,如:
2CrO42-+2H+=Cr2O72-+H2O;
3CrO42-+4H+=Cr3O102-+2H2O
①往混合溶液甲中加入硫酸必须适量的原因是
②混合溶液乙中溶质的化学式是
(5)+3、+6价铬都有很强的毒性,+6价铬的毒性更高,可诱发肺癌和鼻咽癌,所以制取红矾钠后的废水中含有的Cr2O72-必须除去.
工业上可用电解法来处理含Cr2O72-的废水,如图为电解装置示意图(电极材料分别为铁和石墨).通电后,Cr2O72-在b极附近转变为Cr3+,一段时间后Cr3+最终可在a极附近变成Cr(OH)3沉淀而被除去.
a电极的电极反应式是
查看习题详情和答案>>

请回答:
(1)已知Fe(CrO2)2中铬元素是+3价,则Fe(CrO2)2中铁元素是
+2
+2
价.(2)化学上可将某些盐写成氧化物的形式,如Na2SiO3可写成Na2O?SiO2,则Fe(CrO2)2可写成
FeO?Cr2O3
FeO?Cr2O3
.(3)煅烧铬铁矿时,矿石中难溶的Fe(CrO2)2生成可溶于水的Na2CrO4,反应化学方程式如下:
4Fe(CrO2)2+8Na2CO3+7O2=2Fe2O3+8Na2CO4+8CO2
为了加快该反应的反应速率,可采取的措施是
粉碎矿石、升高温度
粉碎矿石、升高温度
.(4)已知CrO42-在不同的酸性溶液中有不同的反应,如:
2CrO42-+2H+=Cr2O72-+H2O;
3CrO42-+4H+=Cr3O102-+2H2O
①往混合溶液甲中加入硫酸必须适量的原因是
少量不能除尽Na2CO3等杂质,过量会生成Na2Cr3O10等副产物
少量不能除尽Na2CO3等杂质,过量会生成Na2Cr3O10等副产物
.②混合溶液乙中溶质的化学式是
Na2Cr2O7和Na2SO4
Na2Cr2O7和Na2SO4
.(5)+3、+6价铬都有很强的毒性,+6价铬的毒性更高,可诱发肺癌和鼻咽癌,所以制取红矾钠后的废水中含有的Cr2O72-必须除去.

工业上可用电解法来处理含Cr2O72-的废水,如图为电解装置示意图(电极材料分别为铁和石墨).通电后,Cr2O72-在b极附近转变为Cr3+,一段时间后Cr3+最终可在a极附近变成Cr(OH)3沉淀而被除去.
a电极的电极反应式是
2H++2e-=H2↑
2H++2e-=H2↑
,b电极附近反应的离子方程式是Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O
Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O
.从能源地质国际研讨会上传出讯息:可燃冰是水与天然气相互作用形成的晶体物质,主要存在于海洋大陆架中及冰山底部,据测定,1体积固体可燃冰能释放200体积甲烷气体.由此判断下列说法不正确的是( )
查看习题详情和答案>>
重铬酸钠俗称红矾钠(Na2Cr2O7·2H2O)是重要的化工产品和强氧化剂。工业制备的流程如下:

请回答:
(1)已知Fe(CrO2)2中铬元素是+3价,则Fe(CrO2)2中铁元素是____价。
(2)化学上可将某些盐写成氧化物的形式,如Na2SiO3可写成Na2O·SiO2,则Fe(CrO2)2可写成____。
(3)煅烧铬铁矿时,矿石中难溶的Fe(CrO2)2生成可溶于水的Na2CrO4,反应化学方程式如下:

为了加快该反应的反应速率,可采取的措施是____。
(4)已知CrO42—在不同的酸性溶液中有不同的反应,如:

①往混合溶液甲中加入硫酸必须适量的原因是____。
②混合溶液乙中溶质的化学式是____。
(5)+3、+6价铬都有很强的毒性,+6价铬的毒性更高,可诱发肺癌和鼻咽癌,所以制取红矾钠后的废水中含有的Cr2O72—必须除去。工业上可用电解法来处理含Cr2O72—的废水,下图为电解装置示意图(电极材料分别为铁和石墨)。通电后,Cr2O72—在b极附近转变为Cr3+,一段时间后Cr3+最终可在a极附近变成Cr(OH)3沉淀而被除去。

a电极的电极反应式是 ,
b电极附近反应的离子方程式是 。
查看习题详情和答案>>